
酸、碱、盐是有广泛用途的重要化合物。某化学活动小组的同学围绕这几类化合物进行了一系列的探究活动。
(1)同学们打开盛浓盐酸和浓硫酸试剂瓶的瓶盖,立即就能把它们区分开来,这是为什么?
(2)下图是某试剂瓶标签上的内容。要把30 g这种浓硫酸稀释为40%的硫酸,需要水的质量为 g。

(3)熟石灰是一种重要的碱,在工农业生产和日常生活中都有十分广泛的应用。工业上首先是用大理石(主要成分碳酸钙)高温煅烧来制取生石灰,然后再用生石灰与水反应来制取熟石灰。请你写出有关反应的化学方程式。
(4)为探究一瓶氢氧化钠固体的变质情况,同学们进行了如下实验。
①取少量该固体样品置于试管中,向其中加入一种无色溶液,发现有气泡产生,说明该样品中含有碳酸钠,由此可确定该固体已发生变质。则无色溶液可能是 。

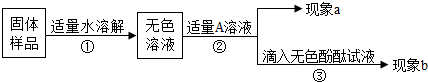
②为探究该固体中是否还有未变质的氢氧化钠,同学们又进行了如下表所示的实验。已知碳酸钠的水溶液呈碱性,它的存在会对氢氧化钠的检验造成干扰。请根据上表部分物质的溶解性表(20℃)所提供的信息,将下表填写完整。
|
实验目的 |
实验操作 |
现象 |
结论或化学方程式 |
|
除去碳酸钠
|
取少量该固体样品溶于水配成溶液,滴加适量的氯化钡溶液,充分反应后过滤 |
有白色沉淀生成
|
有关反应的化学方程式为
|
|
检验是否含有氢氧化钠 |
在滤液中滴加酚酞溶液 |
|
该样品中含有氢氧化钠 |
(5)若73 g质量分数为20%的盐酸与127g氢氧化钠溶液恰好完全中和,试计算反应后所得溶液中溶质的质量分数。
(1)瓶口出现白雾的是浓盐酸,因为浓盐酸有挥发性。(1分)
(2)43.5(1分);
(3)CaCO3高温CaO + CO2↑;(1分);CaO + H2O =Ca(OH)2。(1分)
(4)①盐酸(或硫酸等)(1分)②
|
实验操作 |
现象 |
结论或化学方程式 |
|
|
|
Na2CO3 +BaCl2=BaCO3↓+2NaCl(1分) |
|
|
酚酞溶液变红色(1分) |
|
(5)11.7%
【解析】
试题分析:(1)因为浓盐酸有挥发性,打开盛浓盐酸和浓硫酸试剂瓶的瓶盖,盛浓盐酸的瓶口出现白雾,而盛浓硫酸的瓶口没有白雾,所以立即就能把它们区分开来;
(2)设需要水的质量为x,则有:30g×98%=(30g+x)×40% 解得:x=43.5g
(3)碳酸钙高温煅烧制取生石灰,生石灰与水反应制取熟石灰的化学方程式为:
CaCO3高温CaO + CO2↑; CaO+H2O═Ca(OH)2;
(4)①因为氢氧化钠变质会变成碳酸钠,而碳酸钠和稀盐酸或稀硫酸反应会产生二氧化碳气体,所以向样品中加入稀盐酸或稀硫酸,如果有气泡产生,说明该样品已经变质;②除去碳酸钠可用氯化钡溶液,使碳酸钠转化为碳酸钡沉淀除去;除去碳酸钠后再检验样品中是否有氢氧化钠,有酚酞试液即可,若酚酞变红色,说明有氢氧化钠;
(5)解:设反应后,生成氯化钠的质量为x。
HCl + NaOH =NaCl + H2O(1分)
36.5 58 .5
73 g×20% x
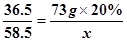
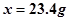 (1分)
(1分)
反应后所得溶液中溶质的质量分数为
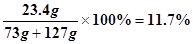 (1分 )
(1分 )
考点:酸、碱、盐的鉴别;物质除杂;反应方程式的相关计算
点评:此题是一道探究实验题,其中包括问答、计算等题目,此题步骤非常多,知识覆盖面很大,由于做起此题来比较繁琐,所以对于大部分学生来说属于难题。


科目:初中化学 来源: 题型:
 18、酸、碱、盐是有广泛用途的重要化合物.
18、酸、碱、盐是有广泛用途的重要化合物.查看答案和解析>>
科目:初中化学 来源: 题型:
 酸、碱、盐是有广泛用途的重要化合物.某化学活动小组的同学围绕这几类化合物进行了一系列的探究活动.
酸、碱、盐是有广泛用途的重要化合物.某化学活动小组的同学围绕这几类化合物进行了一系列的探究活动.查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
| 浓硫酸(分析纯) 化学式:H2SO4 相对分子质量:98 密度:1.84g/cm3 质量分数:98% |
| 阳离子\阴离子 | OH- | NO3- | Cl- | SO42- | CO32- |
| H+ | 溶、挥 | 溶、挥 | 溶 | 溶、挥 | |
| Na+ | 溶 | 溶 | 溶 | 溶 | 溶 |
| Ba2+ | 溶 | 溶 | 溶 | 不溶 | 不溶 |
| 实验目的 | 实验操作 | 现象 | 结论或化学方程式 |
除去碳酸钠 |
取少量该固体样品溶于水配成溶液,滴加适量的 充分反应后过滤 |
有白色沉淀生成 |
有关反应的化学方程式为 |
| 检验是否含有氢氧化钠 | 在滤液中滴加酚酞溶液 | 该样品中含有氢氧化钠 |
查看答案和解析>>
科目:初中化学 来源:2011年河南省开封市中考化学一模试卷(解析版) 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com