
【题目】现有![]() 的
的![]() 溶液,请按照下面要求计算:
溶液,请按照下面要求计算:
![]() 上述溶液中所含溶质的质量为______。
上述溶液中所含溶质的质量为______。
![]() 上述溶液与足量
上述溶液与足量![]() 的盐酸反应,最多可生成
的盐酸反应,最多可生成![]() 多少克______?
多少克______?
![]() 向106g上述溶液中逐滴加入
向106g上述溶液中逐滴加入![]() 的盐酸并不断搅拌,此时发生的反应为:
的盐酸并不断搅拌,此时发生的反应为:![]() ;当
;当![]() 全部转化为
全部转化为![]() 后,再加入盐酸才开始放出
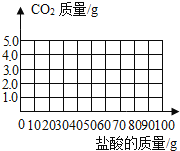
后,再加入盐酸才开始放出![]() 请在图中画出产生气体的曲线______。
请在图中画出产生气体的曲线______。
![]() 另取
另取![]() 溶液边搅拌边加入
溶液边搅拌边加入![]() 的盐酸,有关反应物与生成物的量如表格:
的盐酸,有关反应物与生成物的量如表格:
物质 |
| HCl | x | NaCl |
|
|
质量 |
|
|
|
|
| m |
则x是______;![]() ______。
______。
【答案】![]()
![]()
![]()
![]()
【解析】
(1)根据溶质质量![]() 溶液质量
溶液质量![]() 溶质质量分数,故106g溶液中所含溶质的质量
溶质质量分数,故106g溶液中所含溶质的质量![]() 。
。
(2)设生成二氧化碳的质量为x,消耗的盐酸溶液中溶质的质量为a,则有
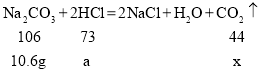
![]()
![]()
解得![]() ,
,![]()
答:最多可生成![]() 的质量为
的质量为![]() 。
。
(3)设将碳酸钠全部转化为碳酸氢钠需要盐酸溶液中溶质的质量为y
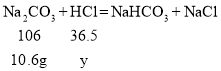
![]()
解得![]()
所以将碳酸钠全部转化为碳酸氢钠需要盐酸溶液的质量为:![]() ,
,
由第![]() 题解得的结果知,将碳酸钠全部转化为二氧化碳消耗盐酸溶液的质量为:
题解得的结果知,将碳酸钠全部转化为二氧化碳消耗盐酸溶液的质量为:![]() ,生成的CO2质量为4.4g。
,生成的CO2质量为4.4g。
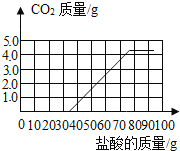
故产生二氧化碳气体的曲线为:
(4)根据表格提供的数据,结合化学方程式:
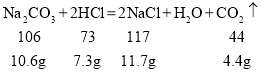
可知,生成![]() 二氧化碳,需完全反应碳酸钠的质量是
二氧化碳,需完全反应碳酸钠的质量是![]() ,生成氯化钠的质量是
,生成氯化钠的质量是![]() 。因此题目中给出的碳酸钠有一部分转化生成了碳酸氢钠和氯化钠,故x为
。因此题目中给出的碳酸钠有一部分转化生成了碳酸氢钠和氯化钠,故x为![]() 。碳酸钠和HCl是反应物,碳酸氢钠、氯化钠、二氧化碳和水是生成物,根据质量守恒定律可得
。碳酸钠和HCl是反应物,碳酸氢钠、氯化钠、二氧化碳和水是生成物,根据质量守恒定律可得![]() ,
,![]() 。
。


 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案科目:初中化学 来源: 题型:
【题目】同学们都比较喜欢吃披萨,披萨是一种以面粉为主要原料,辅以蔬菜、水果、肉类等制成的食物。请回答下列问题:

(1)如图这款披萨的辅料有火腿、虾仁、 蓝莓、西红柿等,其中面饼主要为人体提供的营养素是①_____(水除外)。蓝莓富含的营养素的作用是②__________, 预防疾病,③___________。
(2)盛披萨的平底铁锅用完后,需要洗净晾干,原因是①___________。铁锅手柄的最外层使用木头或热固性塑料,目的是②_________。
(3)种植西红柿时发现其抗病虫害能力弱,且叶片发黄,可以施加________(填一种化肥的化学式)来解决。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】已知某盐在不同温度下的溶解度如下表所示。若把溶质质量分数为22%的该盐溶液由50℃逐渐冷却,则开始析出晶体的温度范围是_____。
温度/℃ | 0 | 10 | 20 | 30 | 40 |
溶解度/g/100g水 | 11.5 | 15.1 | 19.4 | 24.4 | 37.6 |
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为了测定某含杂质7%的黄铜(主要含铜锌)样品中铜的质量分数(杂质中不含铜、锌元素,杂质不溶于水,不与其他物质反应,受热也不分解),某化学小组进行了如下实验:
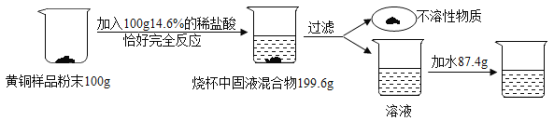
(1)用质量分数为36.5%的浓盐酸配制100g 14.6%的稀盐酸,需要水的质量是__________。
(2)该黄铜样品中铜的质量分数是多少?________
(3)向过滤后所得滤液中加入87.4g水,则最终所得溶液中溶质的质量分数是多少?_______
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】空气、水和金属都是人类重要的资源。
(1)下列各项中,属于我国![]() 环境空气质量标准
环境空气质量标准![]() 基本监控项目的是______。
基本监控项目的是______。
A、SO2浓度 B、O2浓度 C、N2浓度 D、H2O浓度
(2)在实验室中要测定空气中氧气的含量,设计实验原理时要考虑哪些因素?______、______。![]() 答出两条即可
答出两条即可![]()
(3)水曾被误认为是一种“元素”。下列实验能证明水是由氢、氧两种元素组成的是______
A.水的电解 B.水的蒸发 C.氢气在氧气中燃烧 D.水的净化
(4)人们常说的“五金”是指:金、银、铜、铁、锡。根据所学知识回答:
① “真金不怕火炼”是指金即使在高温下也不与______反应。
②铁制容器不能用来盛放农药波尔多液![]() 主要成分是硫酸铜和氢氧化钙
主要成分是硫酸铜和氢氧化钙![]() ,用化学方程式表示其原因______。
,用化学方程式表示其原因______。
③写出一种防止铁制品生锈的具体方法______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某地一辆满载浓硫酸的罐车翻到,导致25t溶质的质量分数为98%的浓硫酸泄漏,并向路基两边蔓延,接到报警后消防官兵立即赶来并用石灰浆(主要成分为氢氧化钙)中和硫酸解除了险情。请回答:
(1)25t溶质的质量分数为98%的浓硫酸中含H2SO4的质量为_______;
(2)计算:中和泄漏的硫酸,理论上需要多少吨氢氧化钙_______;
(3)处理一定量的硫酸,理论上既可用m1吨的氢氧化钙粉末,也可选用m2吨的氧化钙粉末,还可用m3吨碳酸钙粉末,则m1、m2、 m3的数值大小关系为_______________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室有甲、乙两瓶久置的氢氧化钠固体,某学习小组为了研究其变质情况,进行了如下实验:(电子秤示数单位为g)
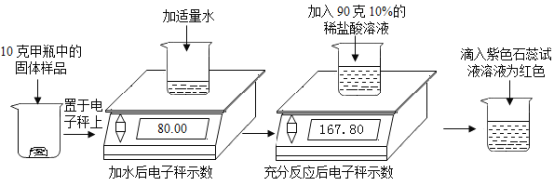
(1)上述实验中产生的二氧化碳气体质量为__________g。
(2)计算甲瓶固体样品中碳酸钠的质量分数_______。
(3)滴入紫色石蕊溶液后溶液为红色,说明反应后溶液呈______性。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】现有一种铜和氧化亚铁的混合物样品。为测定该样品中氧化亚铁的含量,某学生取20.0g此样品置于烧瓶中,分四次加入密度为1.22g/cm3的硫酸并做相关记录。关数据记录如下表:
加硫酸的序号 | 加入硫酸的体积/mL | 剩余固体的质量/g |
1 | 20.0 | 16.0 |
2 | 20.0 | 12.0 |
3 | 20.0 | 8.0 |
4 | 20.0 | 8.0 |
试计算:
(1)10.0g此样品中铜的质量_____。
(2)样品中氧化亚铁的质量分数_____。
(3)所用硫酸溶液溶质的质量分数_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图为硫酸钠和氯化钠的溶解度曲线。下列说法正确的是( )
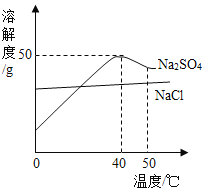
A.两种物质的溶解度都随温度的升高而增大
B.50℃的Na2SO4饱和溶液降到40℃时有晶体析出
C.可用降温结晶的方法提纯含少量Na2SO4的NaCl
D.40℃时,Na2SO4饱和溶液的质量分数大于NaCl饱和溶液的质量分数
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com