
【题目】现有一种铜和氧化亚铁的混合物样品。为测定该样品中氧化亚铁的含量,某学生取20.0g此样品置于烧瓶中,分四次加入密度为1.22g/cm3的硫酸并做相关记录。关数据记录如下表:
加硫酸的序号 | 加入硫酸的体积/mL | 剩余固体的质量/g |
1 | 20.0 | 16.0 |
2 | 20.0 | 12.0 |
3 | 20.0 | 8.0 |
4 | 20.0 | 8.0 |
试计算:
(1)10.0g此样品中铜的质量_____。
(2)样品中氧化亚铁的质量分数_____。
(3)所用硫酸溶液溶质的质量分数_____。
 七彩题卡口算应用一点通系列答案
七彩题卡口算应用一点通系列答案科目:初中化学 来源: 题型:
【题目】请根据如图所示的实验过程和提供的数据(步骤②产生的气体全部逸出),回答下列问题:
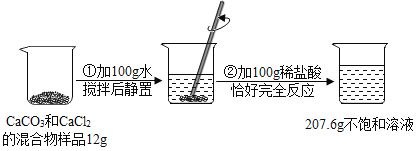
(1)计算原混合物样品中CaCl2的质量__________。
(2)计算稀盐酸中溶质质量__________。
(3)计算恰好反应后的溶液的溶质质量分数__________(结果保留至0.1%)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】现有![]() 的
的![]() 溶液,请按照下面要求计算:
溶液,请按照下面要求计算:
![]() 上述溶液中所含溶质的质量为______。
上述溶液中所含溶质的质量为______。
![]() 上述溶液与足量
上述溶液与足量![]() 的盐酸反应,最多可生成
的盐酸反应,最多可生成![]() 多少克______?
多少克______?
![]() 向106g上述溶液中逐滴加入
向106g上述溶液中逐滴加入![]() 的盐酸并不断搅拌,此时发生的反应为:
的盐酸并不断搅拌,此时发生的反应为:![]() ;当
;当![]() 全部转化为
全部转化为![]() 后,再加入盐酸才开始放出
后,再加入盐酸才开始放出![]() 请在图中画出产生气体的曲线______。
请在图中画出产生气体的曲线______。
![]() 另取
另取![]() 溶液边搅拌边加入
溶液边搅拌边加入![]() 的盐酸,有关反应物与生成物的量如表格:
的盐酸,有关反应物与生成物的量如表格:
物质 |
| HCl | x | NaCl |
|
|
质量 |
|
|
|
|
| m |
则x是______;![]() ______。
______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为测定某氮肥中硫酸铵的纯度(即质量分数)是否与如图所示标签相符,小林取一定量该氮肥样品于烧杯中配成溶液,与足量氯化钡溶液反应,记录有关数据如下表:

反应前 | 反应后 | |
烧杯和样品 溶液总质量 | 氯化钡溶 液质量 | 过滤后烧杯和溶液总质量 (滤液的损失忽略不计) |
45 g | 55 g | 76.7 g |
[反应的化学方程式为(NH4)2SO4+BaCl2=BaSO4↓+2NH4Cl,其他成分能溶于水但不参加反应]
(1)反应共生成BaSO4的质量为____________g。
(2)若所取氮肥样品的质量为15g,试通过计算确定该氮肥中硫酸铵的纯度是否与标签相符________。(请写出计算过程)
(3)反应前后,溶液中硫元素的质量________(选填“不变”“增大”或“减小”)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是浙江大学实验室制备出的世界最轻材料“全碳气凝胶”即“碳海绵”。“碳海绵”具备高弹性和强吸附性,主要成分是石墨烯和碳纳米管。

(1)石墨烯和碳纳米管都属_____(填“单质”或“化合物”)。
(2)碳海绵由碳原子构成,碳原子的结构示意图为_____,则碳原子的核电荷数为_____。
(3)请推测石墨烯可能具有的一条化学性质:_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室制取气体所需的装置如下图所示。请回答以下问题:

(1)仪器a的名称是_____;用高锰酸钾制取氧气时,所选用的发生装置是_____(填字母序号,下同);收集装置是C或_____。
(2)用大理石与稀盐酸制取二氧化碳时,所选用的发生装置是_____,该装置还可用于制氢气,其反应的化学方程式为_____。
(3)乙炔又称电石气,是一种无色、无味、密度跟空气接近、不溶于水的气体;工业上常用它燃烧产生的高温来切割和焊接金属;实验室用电石(固体)与水反应制取乙炔。你认为制取乙炔应选择的发生装置是_____;收集装置是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】用化学用语填空:
(1)乙醇的化学式 _____;
(2)3个金原子 _____;
(3)氯化铁中铁元素的化合价_____。
(4)美国科学家在宇宙中发现了氢元素的一种新粒子(H3+)。一个H3+中含有_____个质子,_____个电子。
查看答案和解析>>
科目:初中化学 来源: 题型:
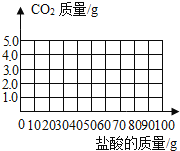
【题目】硝酸钾(KNO3)和氯化钾(KCl)的溶解度曲线如图所示:
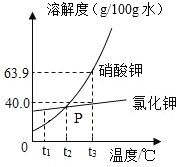
① t1 ℃时,氯化钾的溶解度____________(填“>”、“=”或“<”)硝酸钾的溶解度。
②硝酸钾的溶解度随温度的升高而____________(填“增大”或“减小”)。
③P 点是硝酸钾和氯化钾的两条曲线的交点,其含义是____________。
④若硝酸钾中混有少量氯化钾,提纯硝酸钾采取的方法是____________。
⑤将 t3 ℃时氯化钾的饱和溶液70.0g稀释成溶质质量分数为20.0%的氯化钾溶液,需加水____________g。查阅相关物质的密度后,在实验室完成该实验,通常需要 仪器除烧杯、 胶头滴管外 ,还需____________(填字母标号) 。
A 电子天平
B 药匙
C 量筒
D 玻璃棒
⑥现有 t2 ℃时硝酸钾饱和溶液 m1 g 和氯化钾饱和溶液 m2 g。不考虑水的蒸发,一定成立的是____________(填字母标号)。
A 两溶液中溶质的质量分数相等
B 分别升温至t3 ℃,所得溶液均为不饱和溶液
C 分别降温到t1 ℃,析出 KNO3的质量大于析出 KCl 的质量
D 保持t2 ℃不变,分别加入等质量的水,混匀后所得溶液中溶质的质量分数相等
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】请根据下图所示的实验过程和提供的数据(假设步骤②产生的气体全部逸出),回答下列问题:
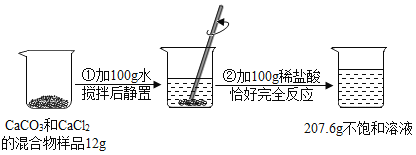
(1)发生反应的化学方程式为___________;
(2)求解12g样品中碳酸钙质量(X)的比例式为____________;
(3)原固体混合物中二者质量的最简整数比为___________ ;
(4)配制上述实验所需的稀盐酸,需要溶质质量分数为36.5﹪的浓盐酸的质量是___________;
(5)在②反应后的溶液中蒸发_____g水,才能得到溶质质量分数为10﹪的氯化钙溶液。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com