
| ||
| ||
| ||
| 2.4g | ||
|
| 2.4g | ||
|
| ||


科目:初中化学 来源: 题型:
实验课上,为检验镁条能否在N2中燃烧,兴趣小组展开如下探究:
【查阅资料】氮化镁(Mg3N2)是一种淡黄色固体,能和水反应,生成Mg(OH)2和NH3;
【实验步骤】
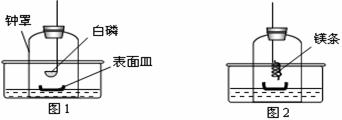
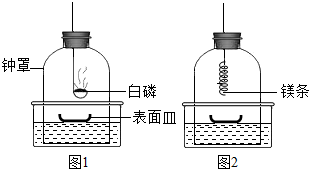
①将足量白磷在空气中点燃后,迅速伸入钟罩内,塞紧橡皮塞(图1);
②待钟罩内水面不再变化时,向水槽中加水,使水槽中液面与钟罩内液面相平;
③打开橡皮塞,将燃着的螺旋状镁条迅速伸入钟罩内,塞紧橡皮塞(图2);
④待钟罩内水面不再变化时,观察钟罩内壁及表面皿中固体颜色,取少量固体加入水中。
【分析】
(1)步骤①中足量白磷在钟罩内燃烧的目的是 ▲ ;
(2)步骤②中加水的目的是 ▲ ;
(3)步骤③中镁条绕城螺旋状的目的是 ▲ ;镁条剧烈燃烧,反应的化学方程式
为 ▲ ;
(4)步骤④中钟罩内壁及表面皿中出现淡黄色固体。加入水中,产生白色浑浊及能使湿润红色石蕊试纸变 ▲ 色的气体,反应的化学方程式为 ▲ ;
【结论】
镁能在N2中燃烧,并生成Mg3N2。
(5)请你判断:2.40g镁条在某密闭容器中完全燃烧,所得固体质量可能为 ▲ ;
[相对分子质量 —— Mr(MgO)∶40、 Mr(Mg3N2)∶100]
A.3.33g B.4.00g C.3.93g D.3.96g
查看答案和解析>>
科目:初中化学 来源:2013年江苏省扬州中学树人学校中考化学二模试卷(解析版) 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:
实验课上,为检验镁条能否在N2中燃烧,兴趣小组展开如下探究:
【查阅资料】氮化镁(Mg3N2)是一种淡黄色固体,能和水反应,生成Mg(OH)2和NH3;
【实验步骤】
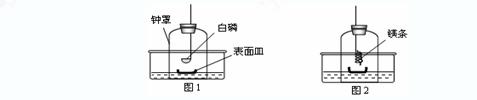
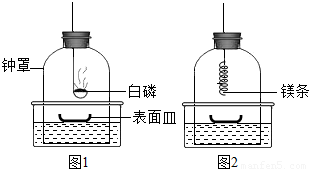
①将足量白磷在空气中点燃后,迅速伸入钟罩内,塞紧橡皮塞(图1);
②待钟罩内水面不再变化时,向水槽中加水,使水槽中液面与钟罩内液面相平;
③打开橡皮塞,将燃着的螺旋状镁条迅速伸入钟罩内,塞紧橡皮塞(图2);
④待钟罩内水面不再变化时,观察钟罩内壁及表面皿中固体颜色,取少量固体加入水中。
【分析】
(1)步骤①中足量白磷在钟罩内燃烧的目的是 ;
(2)步骤②中加水的目 的是 ;
的是 ;
(3)步骤③中镁条绕成螺旋状的目的是 ;镁条剧烈燃烧,反应的化学方程式
为 ;
(4)步骤④中钟罩内壁及表面皿中出现淡黄色固体。该固体加入水中反应的化学方程式为 ;
【结论】镁能在N2中燃烧,并生成Mg3N2。
(5)请你判断:2.40g镁条在空气中完全燃烧,所得固体质量可能为 (假设镁条只与氮气、氧气反应) A.3.33g B.4.00g C.3.93g D.3.96g
查看答案和解析>>
科目:初中化学 来源: 题型:
实验课上,为检验镁条能否在N2中燃烧,兴趣小组展开如下探究:
【查阅资料】氮化镁(Mg3N2)是一种淡黄色固体,能和水反应,生成Mg(OH)2和NH3;
【实验步骤】
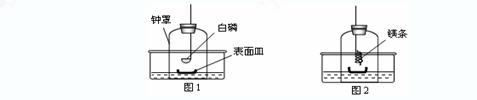
①将足量白磷在空气中点燃后,迅速伸入钟罩内,塞紧橡皮塞(图1);
②待钟罩内水面不再变化时,向水槽中加水,使水槽中液面与钟罩内液面相平;
③打开橡皮塞,将燃着的螺旋状镁条迅速伸入钟罩内,塞紧橡皮塞(图2);
④待钟罩内水面不再变化时,观察钟罩内壁及表面皿中固体颜色,取少量固体加入水中。
【分析】
(1)步骤①中足量白磷在钟罩内燃烧的目的是 ;
(2)步骤②中加水的目 的是 ;
的是 ;
(3)步骤③中镁条绕成螺旋状的目的是 ;镁条剧烈燃烧,反应的化学方程式
为 ;
(4)步骤④中钟罩内壁及表面皿中出现淡黄色固体。该固体加入水中反应的化学方程式为 ;
【结论】镁能在N2中燃烧,并生成Mg3N2。
(5)请你判断:2.40g镁条在空气中完全燃烧,所得固体质量可能为 (假设镁条只与氮气、氧气反应) A.3.33g B.4.00g C.3.93g D.3.96g
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com