
【题目】下列为配制100g质量分数为10.6%的碳酸钠溶液的实验,请填写实验步骤以及步骤中的问题:
(1)计算:碳酸钠的质量为___g,水为___g.
(2)___:用托盘天平称量,碳酸钠应放在左盘
(3)___:用量筒来量取所需的水
(4)溶解:若称量的碳酸钠中含有水分,则所配制的溶液的质量分数会___(填“偏大”、“偏小”或“无影响”)
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:
【题目】化学与生活息息相关,请你用化学知识回答以下生活中的问题
(1)碘酒是家庭常备药,碘酒中的溶剂是_____(写化学式)。
(2)炎热的夏季自行车车胎容易爆裂,从微观角度分析原因是_____。
(3)铝制品抗腐蚀性能很好,原理是_____(用化学方程式表示)
(4)现有①黄瓜②豆腐③馒头④鸡蛋,其中富含蛋白质的是_____(填序号)。
(5)用盐酸将铁制品表面的铁锈除去的化学方程式是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】探究石灰石与浓盐酸反应产生的气体不能使饱和石灰水变浑浊的原因
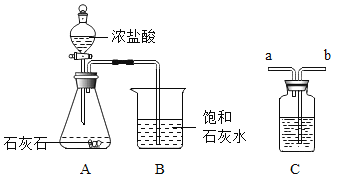
查阅资料:Na2CO3与CO2、H2O反应生成可溶于水的NaHCO3;NaHCO3与HCl反应,与CO2不反应。
①写出装置A中的一种仪器名称______。
②反应中装置B内没有变浑浊,用化学方程式解释原因______。
③为证明CO2确实能与石灰水反应,在A、B装置之间增加C装置,装置的连接顺序是A→___B(填“a”b”);其中盛放的试剂合理的是___(填选项序号)。
Ⅰ.浓硫酸;Ⅱ.NaOH溶液;Ⅲ.饱和Na2CO3溶液;Ⅳ.饱和NaHCO3溶液
④改进实验装置后,装置B中饱和石灰水变浑浊了,写出装置B中发生的化学方程式____。
⑤石灰石与稀盐酸反应(杂质不与稀盐酸反应),固体质量减少12.5g,则生成二氧化碳气体___mol(通过化学方程式计算)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是甲、乙、丙三种固体物质的溶解度曲线,请回答:
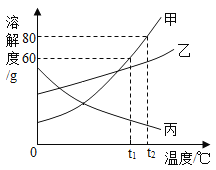
(1)0℃时,三种物质中溶解度最小的是________;
(2)将t1℃时甲、乙、丙三种物质的饱和溶液分别升温到t2℃,有固体析出的是______;
(3)t2℃时,将一定量甲物质加入100g水中完全溶解,再降温到t1℃,析出甲物质15g,则t2℃时,加入甲物质的质量是______g。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】将海水进行处理后获得精盐水.海水中,除氯化钠外,还含有氯化镁、氯化钙、硫酸钠等杂质.其处理的主要流程如下:
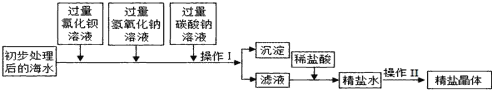
(1)加入过量BaCl2溶液发生反应的化学方程式是___
(2)加入碳酸钠溶液的目的是___.Na2CO3与BaCl2顺序颠倒则最后所得的精盐水中还含有____(填名称)
(3)操作Ⅱ的名称是___,其中玻璃棒的作用是____
(4)向滤液中滴加适量稀盐酸的目的是____
(5)沉淀的成分有(填化学式)___、___、___、___
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】我国化学家侯德榜发明了联合制碱法,其生产纯碱和副产品氯化铵的工艺流程如图1所示:
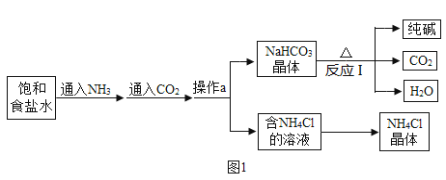
请回答下列问题:
(1)写出反应I的化学方程式:_____,含NH4Cl的溶液得到NH4Cl晶体的过程是加热浓缩、_____、过滤。
(2)上述工艺流程中可循环利用的物质是_____。
(3)铵盐水吸收二氧化碳后生成碳酸氢钠和氯化铵,碳酸氢钠首先结晶析出,原因是_____。
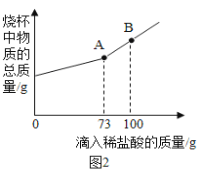
(4)某制碱厂制出的Na2CO3含有NaCl,取12g该样品放入烧杯中,逐渐滴加溶质质量分数为10%的稀盐酸,烧杯中物质的总质量与所滴入稀盐酸的质量关系曲线如图2所示,请计算样品中Na2CO3的质量分数(结果保留1位小数)_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图为硝酸钾的溶解度曲线.

(1)硝酸钾的溶解度随温度升高而_____;
(2)20℃时,向100g水中加入55g硝酸钾,充分溶解后得到的溶液(填“是”或“不是”)_____饱和溶液,其原因是_____;再将温度升高到40℃,该溶液中溶质的质量分数(填“不变”、“变大”或“变小”)_____.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学是一门以实验为基础的科学,请根据要求回答问题。
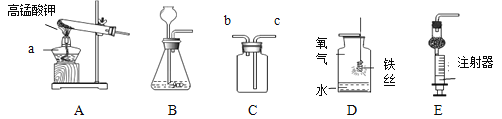
(1)仪器a的名称是______。
(2) 实验室用装置A制取O2时应做的改进为______。装置D中水的作用是______。
(3)实验室制取O2、H2均可选择______(填装置序号)作为气体的发生装置。实验室制取CO2的化学方程式为______,若用装置C收集CO2,验满的方法是______。用装置E制取CO2时,使反应停止的操作是______。
(4)N2在加热和催化剂条件下能与 H2化合生成NH3,如图为制取少量NH3的装置。
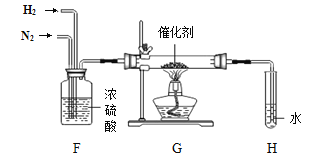
①检验有NH3生成的操作是______。
②N2和H2反应的化学方程式为______。
③已知:同温同压下,气体的体积比等于分子数之比。图中F装置的作用有三点:一是干燥N2和H2;二是使N2和H2充分混合;三是______,从而提高N2和H2的利用率。
④实验共消耗0.4g H2,若H2由锌和溶质质量分数为20%的稀硫酸反应产生,求消耗的稀硫酸的质量______。(写出解题过程)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com