
| 实验步骤 | 实验现象 | 结论 | 解释 |
| 蜡烛里一定含有氢元素 | |||
| 蜡烛里一定含有碳元素 |
| 步骤 | 现象 | 结论 | 解释 |
| 点燃一根蜡烛.在蜡烛的火焰上方罩一个冷而干燥的烧杯 | 烧杯内壁出现水珠 | 蜡烛燃烧后生成了水,所以蜡烛的成分里含有氢元素; | 水中含有氢元素和氧元素,二氧化碳中含有碳元素和氧元素,根据质量守恒定律可推测出蜡烛中一定含有碳元素和氢元素. |
| 将上述的烧杯立即倒转过来,倒人澄清的石灰水,振荡 | 澄清的石灰水变浑浊 | 蜡烛燃烧后生成了二氧化碳,所以蜡烛的成分里含有碳元素 |
| 步骤 | 现象 | 结论 | 解释 |
| 点燃一根蜡烛.在蜡烛的火焰上方罩一个冷而干燥的烧杯 | 烧杯内壁出现水珠 | 蜡烛燃烧后生成了水,所以蜡烛的成分里含有氢元素; | 水中含有氢元素和氧元素,二氧化碳中含有碳元素和氧元素,根据质量守恒定律可推测出蜡烛中一定含有碳元素和氢元素. |
| 将上述的烧杯立即倒转过来,倒入澄清的石灰水,振荡 | 澄清的石灰水变浑浊 | 蜡烛燃烧后生成了二氧化碳,所以蜡烛的成分里含有碳元素 |


科目:初中化学 来源: 题型:
 25、“在学校的元旦联欢会上,某同学表演了‘水能生火’的魔术.他向包有过氧化钠(Na2O2)粉末的脱脂棉上滴水,脱脂棉燃烧起来.”小颖看到这段话后非常感兴趣,她和同学们一起对该问题进行了一系列的探究.
25、“在学校的元旦联欢会上,某同学表演了‘水能生火’的魔术.他向包有过氧化钠(Na2O2)粉末的脱脂棉上滴水,脱脂棉燃烧起来.”小颖看到这段话后非常感兴趣,她和同学们一起对该问题进行了一系列的探究.| 实验步骤 | 实验现象 | 实验结论 |
向反应后的试管内滴加稀盐酸 |
没有气泡生成 |
生成物中没有CO32- |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
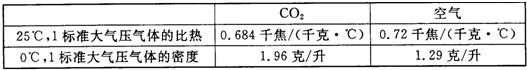
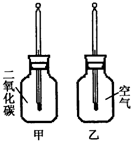
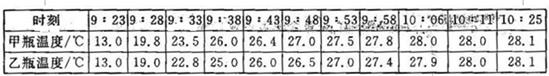
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
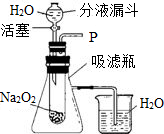 “在学校的元旦联欢会上,某同学表演了‘水能生火’的魔术.他向包有过氧化钠(Na2O2)粉末的脱脂棉上滴水,脱脂棉燃烧起来.”
“在学校的元旦联欢会上,某同学表演了‘水能生火’的魔术.他向包有过氧化钠(Na2O2)粉末的脱脂棉上滴水,脱脂棉燃烧起来.”| 实验步骤 | 实验现象 | 实验结论 |
| 生成物中没有CO32- |
| 实验序号 | 实验方案 | 实验现象 |
| 1 | 将水滴入盛有过氧化钠固体的试管中,配制成溶液,用带火星的木条检验生成的气体 | 反应激烈,有大量气体产生,并能使木条复燃 |
| 2 | 取三份实验1所得溶液分装于三支试管中是进行如下实验: ①第一份中加入紫色石蕊试液 ②第二份中加入无色酚酞试液 ③第三份中先加水再加入无色酚酞试液 |
①溶液变蓝且长时间不褪色 ②溶液显红色,半分钟内褪色 ③溶液显红色,半分钟内褪色 |
| 3 | ①称取3.9g过氧化钠固体,逐滴加入约50mL水. ②待不再产生气体,10min以后,加入用小纸片包好的MnO2,迅速塞紧双孔塞,轻轻摇动反应器,纸包自动散开,MnO2与溶液开始接触. |
①测得氧气体积为185mL左右 ②又产生大量氧气,至反应完全以后,又测得产生了374mL氧气(两次测定条件均相同) |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
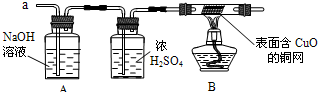
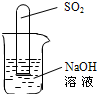
| 实验过程 | 实验现象 | 实验结论 |
| 在一支试管中加入5ml5%的H2O2溶液,然后滴入适量的FeCl3溶液,把带火星的木条伸入试管. | 试管中有大量的气泡产生,伸入的带火星的木条复燃 |
FeCl3溶液可以催化分解H2O2 |
| 实验过程 | 实验现象 | 实验结论 |
| 向盛有5ml5%的H2O2溶液的试管中加入少量的HCl,并把带火星的木条伸入试管 | 无明显现象 | 起催化作用的不是Cl- |
| 向盛有5ml5%的H2O2溶液的试管中加入少量的 Fe(NO3)3溶液 ,并把带火星的木条伸入试管 |
试管中有大量气泡产生,带火星的木条复燃 |
起催化作用的是Fe3+ |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
| 实验方案 | 实验现象 | 结论 |
| 方案一:向盛有10mL 5% H2O2溶液的试管中加入2g 氧化铁粉末,将一根带火星的木条放在试管口,观察现象. | 有大量气泡产生,带火星木条复燃 有大量气泡产生,带火星木条复燃 |
甲同学结论成立. |
| 方案二:向盛有10mL 5% H2O2溶液的试管中加入 铁 铁 粉末,将一根带火星的木条放在试管口,观察现象. |
无现象 | 乙同学结论 不成立 不成立 .(填“成立”或“不成立”) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com