

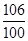 =
=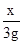 ,x=3.18g
,x=3.18g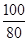 =
=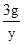 ,y=2.4g
,y=2.4g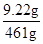 ×100%=2%.
×100%=2%.

科目:初中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:初中化学 来源:不详 题型:单选题
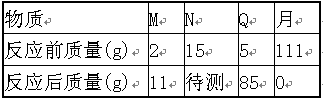
| A.该反应属于化合反应 |
| B.待测物质N的质量为22g |
| C.该反应属于分解反应 |
| D.反应中M、N、Q、R四种物质质量比为9:37:80:111 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:初中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:初中化学 来源:不详 题型:计算题
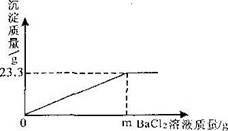
查看答案和解析>>
科目:初中化学 来源:不详 题型:推断题
| | 第一份 | 第二份 | 第三份 | 第四份 |
| 加入CaCl2溶液的质量/g | 10 | 20 | 30 | 40 |
| 生成沉淀的质量/g | 4 | 8 | 10 | 10 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:单选题
| A.用10mL的量筒量取9.0mL水 |
| B.用向下排空气法收集纯净的氢气 |
| C.用托盘天平称取10.58g碳酸钠粉末 |
| D.用150mL酒精和50mL水精确配制200mL医用消毒酒精 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com