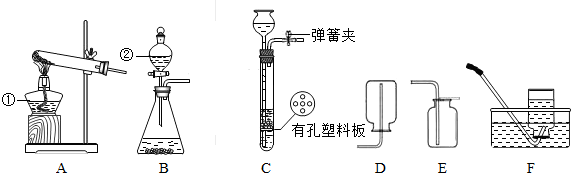
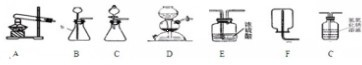
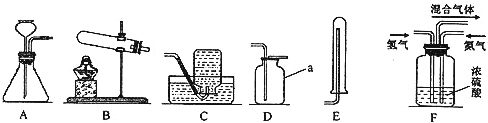
解:(1)颈比较长的仪器叫长颈漏斗;收集气体的仪器是集气瓶;
(2)反应物是高锰酸钾,生成物是锰酸钾、二氧化锰和氧气,用观察法配平,反应条件是加热,氧气后面标上上升符号;由于氧气不易溶于水,可以用排水法收集,密度比空气大可以用向上排空气法收集;发现收集到的氧气呈红色是因为高锰酸钾制氧气在试管口没放棉花团,高锰酸钾颗粒随着气流进入导管,进入集气瓶,使气体呈红色;
(3)实验室制取二氧化碳用碳酸钙和稀盐酸,反应物是碳酸钙和盐酸,生成物是氯化钙、水、二氧化碳,用观察法配平,二氧化碳后面标上上升符号;C装置如果打开开关,从长颈漏斗中稀盐酸流入试管,与碳酸钙接触,反应开始进行,关闭开关由于二氧化碳出不来了,试管内压强越来越大,把盐酸又压回到长颈漏斗内,使盐酸与碳酸钙分离,反应停止,所以能控制反应的发生和停止;由于二氧化碳能溶于水,不能用排水法收集,密度比空气大用向上排空气法收集;
(4)①由实验室常用加热氯化铵和氢氧化钙固体混合物的方法制取氨气,可知反应需要加热,发生装置选择有酒精灯的,氨气密度比空气小,用向下排空气法收集,极易溶于水不能用排水法收集;制取氨气的反应物是氯化铵和氢氧化钙写在箭头的左边,生成物是氯化钙、水和氨气写在箭头的右边,反应条件是加热写在箭头的上边;
②利用G装置做氨气合成实验,好处有将氮气和氢气干燥除去其中的水分;能使氮气和氢气充分混合;没有参加反应的氮气或氢气可以收集起来循环使用,所以起到了提高氮气和氢气的利用率效果.
故答案为:(1)长颈漏斗;集气瓶;(2)2KMnO
4 
K
2MnO
4+MnO
2+O
2↑;DE;高锰酸钾制氧气在试管口没放棉花团,高锰酸钾颗粒随着气流进入导管,进入集气瓶;(3)碳酸钙;稀盐酸;CaCO
3+2HCl═CaCl
2+H
2O+CO
2↑;能控制反应的发生和停止;E;(4)①BF;氯化铵+氢氧化钙

氯化钙+水+氨气;②没有参加反应的氮气或氢气可以收集起来循环使用.
分析:(1)熟记常见仪器的名称;(2)根据方程式的书写,氧气的密度和溶解性,高锰酸钾制取氧气的注意事项考虑本题;(3)根据实验室制取二氧化碳的药品,方程式的书写,A和C装置的不同点和二氧化碳的性质考虑本题;(4)①根据制取氨气的反应条件和文字表达式的写法考虑;②根据G装置的特点考虑.
点评:解答本题关键是要熟悉常见仪器的名称,知道收集装置、发生装置的选择方法,知道实验室制取氧气和二氧化碳的反应原理,知道文字表达式的书写方法,知道两种装置比较出不同点来再分析其优点.

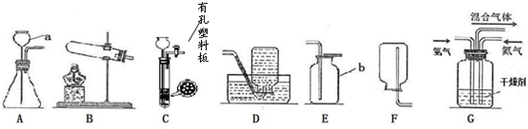
 NH3) 实验室模拟合成氨气的流程如下:
NH3) 实验室模拟合成氨气的流程如下: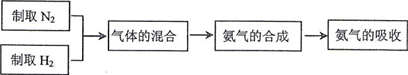
 K2MnO4+MnO2+O2↑;DE;高锰酸钾制氧气在试管口没放棉花团,高锰酸钾颗粒随着气流进入导管,进入集气瓶;(3)碳酸钙;稀盐酸;CaCO3+2HCl═CaCl2+H2O+CO2↑;能控制反应的发生和停止;E;(4)①BF;氯化铵+氢氧化钙
K2MnO4+MnO2+O2↑;DE;高锰酸钾制氧气在试管口没放棉花团,高锰酸钾颗粒随着气流进入导管,进入集气瓶;(3)碳酸钙;稀盐酸;CaCO3+2HCl═CaCl2+H2O+CO2↑;能控制反应的发生和停止;E;(4)①BF;氯化铵+氢氧化钙 氯化钙+水+氨气;②没有参加反应的氮气或氢气可以收集起来循环使用.
氯化钙+水+氨气;②没有参加反应的氮气或氢气可以收集起来循环使用.