
 ��ͼ��ʾ�ǹ���a��b��c�������ʵ��ܽ�����¶ȱ仯������ͼ������ͼʾ�ش�
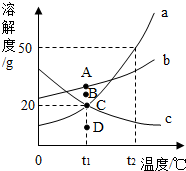
��ͼ��ʾ�ǹ���a��b��c�������ʵ��ܽ�����¶ȱ仯������ͼ������ͼʾ�ش����� ���ݹ�����ܽ�����߿��ԣ��ٲ��ij������һ���¶��µ��ܽ�ȣ��Ӷ�ȷ�����ʵ��ܽ��ԣ��ڱȽϲ�ͬ������ͬһ�¶��µ��ܽ�ȴ�С���Ӷ��жϱ�����Һ�����ʵ����������Ĵ�С�����ж����ʵ��ܽ�����¶ȱ仯�ı仯������Ӷ��ж�ͨ�����½ᾧ���������ᾧ�ķ����ﵽ�ᴿ���ʵ�Ŀ�ģ�
��� �⣺��ͨ�������ܽ�����߿�֪����ͼ�У��ܽ�ȵ�λӦ�ø�Ϊ��g/100gˮ��
��ͨ�������ܽ�����߿�֪�����¶����ߣ������������ܽ�ȱ�С����c��t2��ʱ��a��b��c�������ʵ��ܽ����С�����˳����a��b��c��
��t2��ʱ��a���ʱ�����Һ�����������ǣ�$\frac{50g}{150g}$��100%=33.3%��
��t1��ʱ��a���ʵ��ܽ�����b��c���ʵ��ܽ����ȣ���������ͼ�б�ǵ�A��B��C��D�ĸ��㣬���ĸ����б�ʾa��b��c�������ʵ���Һ������������ȵĵ㣬������CD��
��a���ʵ��ܽ�����¶ȵ�Ӱ��ϴ�c���ʵ��ܽ�����¶ȵ����߶���С��������ͬѧ����c��ȫ��ȥ��������ҺΪa��c�Ļ����Һ�����ɺ����ù�����Ϊ����
�ʴ�Ϊ����g/100gˮ��
��c��a��b��c��
��t33.3%��
��CD��
����ͬѧ����c��ȫ��ȥ��������ҺΪa��c�Ļ����Һ�����ɺ����ù�����Ϊ����
���� �����ѶȲ��Ǻܴ���Ҫ�����˹�����ܽ����������ʾ�����壬�����ݹ�����ܽ�������������ص����⣬�Ӷ������������⡢��������������


 ѧ�����νӽ̲��Ͼ���ѧ������ϵ�д�
ѧ�����νӽ̲��Ͼ���ѧ������ϵ�д� Сѧ������ҵϵ�д�
Сѧ������ҵϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ��ʵ | ���� | |
| A | �������£�ʪ�·��������� | ���ӵ��˶��������¶����{���ӿ� |
| B | �Ȼ��ƹ��岻���� | �Ȼ��ƹ�����û�������ƶ������� |
| C | CO��CO2�Ļ�ѧ���ʲ�ͬ | ���ӹ��ɲ�ͬ |
| D | ϡ�����ϡ���ᶼ��ʹ��ɫʯ����ɫ | ��Һ�ж������������ |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Fe2O3+H2SO4��FeSO4+H2O | B�� | K2CO3+HCl��2KCl+H2CO3 | ||
| C�� | Al��OH��3+3HCl��2AlCl3+3H2O | D�� | 2Fe+H2SO4��Fe2��SO4��3+H2�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� |  �������� �������� | B�� |  �������� �������� | ||
| C�� |  �ߺ����� �ߺ����� | D�� |  ���϶��� ���϶��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
 ��ͼ��������β����ת��������β�����ж���CO��NO����ת��Ϊ������ ��ʾ��ͼ��������˵����ȷ���ǣ�������
��ͼ��������β����ת��������β�����ж���CO��NO����ת��Ϊ������ ��ʾ��ͼ��������˵����ȷ���ǣ�������| A�� | �˷�ӦΪ�û���Ӧ | |
| B�� | ͼ�������������ֲ�ͬ���� | |
| C�� | ԭ���ڻ�ѧ�仯ǰ����Ŀ�Dz��ı�� | |
| D�� | �μӷ�Ӧ�����ַ��ӵĸ�����Ϊ2��3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ʵ�����ø��������ȡ���� 2KMnO4$\frac{\underline{\;\;��\;\;}}{\;}$K2MnO4+MnO2+O2�� �ֽⷴӦ | |
| B�� | ��˿��������ȼ�� 4Fe+3O2$\frac{\underline{\;��ȼ\;}}{\;}$2Fe2O3���Ϸ�Ӧ | |
| C�� | ��¯����ԭ�� Fe2O3+3CO$\frac{\underline{\;����\;}}{\;}$2Fe+3CO2 ���ֽⷴӦ | |
| D�� | ��ͭƬͶ��������ϡ������ Cu+2HCl=CuCl2+H2�� �û���Ӧ |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com