
【题目】往10g硫酸和硫酸铜的混合溶液中,逐滴加入溶质质量分数为10%的氢氧化钠溶液,所得溶液的质量和加入的氢氧化钠溶液质量关系如图所示。下列说法错误的是( )
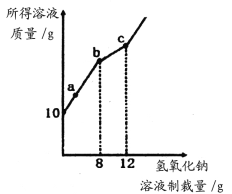
A.a点时溶液中有3种溶质
B.b点时溶液中水的质量为15.78g
C.c点时溶液的pH=7
D.原混合溶液中硫酸铜的质量分数为16%
【答案】D
【解析】
硫酸和氢氧化钠反应生成硫酸钠和水,硫酸铜和氢氧化钠反应生成硫酸钠和氢氧化铜蓝色沉淀。
A、氢氧化钠先和硫酸反应生成硫酸钠和水,a点时溶液中溶质为硫酸钠、氢氧化钠、硫酸铜3种溶质,故A正确;
B、氢氧化钠和硫酸、硫酸铜反应的化学方程式及其质量关系为
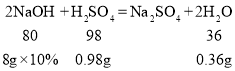
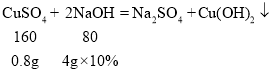
则10g硫酸和硫酸铜的混合溶液中水的质量为![]() ,b点反应时生成水的质量为0.36g,则b点时溶液中水的质量为
,b点反应时生成水的质量为0.36g,则b点时溶液中水的质量为![]() ,8g氢氧化钠溶液中水的质量为8g-8g×10%=7.2g,则b点溶液中水的质量为7.2g+8.58g=15.78g,故B正确;
,8g氢氧化钠溶液中水的质量为8g-8g×10%=7.2g,则b点溶液中水的质量为7.2g+8.58g=15.78g,故B正确;
C、c点时氢氧化钠和硫酸、硫酸铜刚好完全反应,溶液的pH=7,故C正确;
D、原混合溶液中硫酸铜的质量分数为![]() 。故D不正确。故选D。
。故D不正确。故选D。


科目:初中化学 来源: 题型:
【题目】ZnSO4饱和溶液的溶质质量分数随温度变化的曲线如图所示。下列说法正确的是
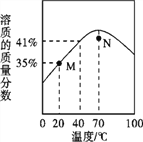
A. N点对应的ZnSO4溶液升温或降温均都可能析出晶体
B. M点对应的ZnSO4溶液是不饱和溶液
C. ZnSO4饱和溶液的溶质质量分数随温度升高而增大
D. 40℃时,ZnSO4的溶解度为41g
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为除去食盐水中 CaCl2、MgCl2、Na2SO4 杂质,某化学小组设计了如下方案:
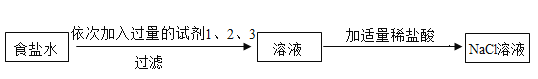
(1)过滤用到的玻璃仪器有烧杯、漏斗和_____。
(2)分别写出试剂 1、2、3 的化学式_____。
(3)最后所得溶液中 NaCl 的质量大于原混合溶液中 NaCl 的质量,写出一个可使NaCl 质量增加的化学方程式_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某学习小组的同学前往当地的石灰石矿区进行调查,他们取了若干块矿石样品,对样品中的碳酸钙的质量分数进行检测,采用了以下的办法:取用12. 0g这种石灰石样品,把40.0g稀盐酸分四次加入,测量过程所得数据见下表(杂质不溶于水,不与盐酸反应)。
序号 | 第一次 | 第二次 | 第三次 | 第四次 |
加入稀盐酸质量(g) | 10.0 | 10.0 | 10.0 | 10.0 |
剩余固体质量(g) | 8.0 | m | 2.0 | 2.0 |
请计算: (1) 表中的m的数值应为_____;
(2)样品中的碳酸钙的质量分数是_____;
(3)产生二氧化碳的总质量是多少?_____
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列是初中化学中的三个实验,请根据你所学的知识回答:
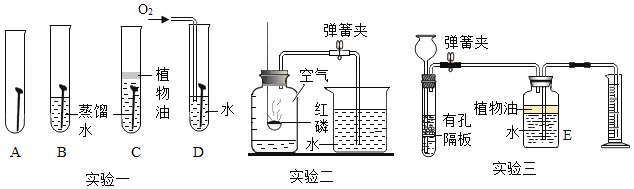
(1)实验一中的四个试管中,铁钉最易生锈的是_____(填字母序号)。由此说明铁钉生锈是_____共同作用的结果。常在铁制品表面镀一层金属铝以达到防锈的目的,其原因是_____(用化学方程式表示)
(2)实验二中红磷燃烧的化学方程式为_____。若将集气瓶和烧杯中的水换成_____溶液,则用木炭也可代替红磷测定出空气中氧气的含量。
(3)某同学欲用实验三这套装置制取并测量产生二氧化碳气体的体积,则他需准备的化学药品是_____(填药品名称)。用E来测量生成二氧化碳的体积,其中在水面上放一层植物油的目的是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图是实验室制取气体的部分装置,请回答:
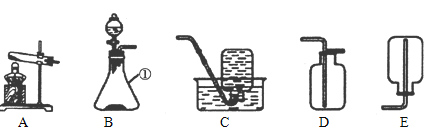
(1)图中仪器①的名称是_________。装置B中使用分液漏斗的优点是________。
(2)实验室用高锰酸钾制取氧气可选用的发生装置是______(填序号);发生反应的化学方程式为___________________。
(3)小组同学对带火星的木条复燃是否需要纯氧产生疑问,开展如下实验:
集气瓶编号 | 1 | 2 | 3 | 4 |
集气瓶中氧气的含量% | 30 | 40 | 50 | 60 |
带火星的木条 | 亮 | 很亮 | 复燃 | 复燃 |
①该小组同学收集氧气时应该选用收集装置是________(填序号)。
②设置4组实验,且每次用同一根木条插入相同的深度,这样做的目的是________。
③欲探究木条复燃所需氧气含量更精确的数值,请写出简要实验方案______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】物质的组成、结构、性质与制备
(1)物质的组成和结构决定了物质的性质。请你利用已有的化学知识完成下表并填空
物质的名称(或俗称) | 构成物质的微粒符号 | 体现物质化学性质的变化(用方程式表示,写一个即可) |
_________ | Na+、OH- | _________ |
乙醇 | _________ | _________ |
铜 | _________ | _________ |
上表你列举的体现物质化学性质的反应中,包含的基本反应类型有______。
(2)利用物质的性质可以检验或鉴别物质。实验室有一瓶失去标鉴的溶液,为了鉴别其是稀盐酸还是氯化镁溶液,小组同学选用不同的试剂进行实验,都将其鉴别了出来。
可供选择的试剂:银片、生锈的铁钉、块状石灰石、二氧化碳、硝酸银溶液、澄清的石灰水
请按要求填写下表(只填写检验过程中可观察到明显现象的化学变化方程式)
检验过程中发生化学变化的方程式 | 运用物质的性质 |
_________ | 盐能与某些碱反应 |
_________ | _________ |
_________ | _________ |
(3)利用物质的性质可通过化学变化制备物质胆矾(CuSO4·5H2O)在工农业生产中有广泛的用途。实验室利用废旧电池的铜棒(主要含铜和锌)为原料制备胆矾。实验流程如图所示:查阅资料:氧化锌能溶于氢氧化钠溶液。
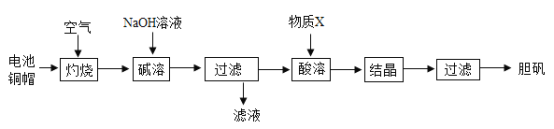
①废旧电池钢帽的表面常有油污,可用洗洁精预先除去,洗洁精在除去油污的过程中起____________作用。
②“碱溶”步骤中,为加快反应速率可采取多种措施,如搅拌、______、______等。
③“酸溶”时,发生反应的化学方程式是_____________。
④试写出胆况在工农业生产中的一种用途_______________.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】氢气是一种理想的新能源,具有广阔的开发前景。铁酸锌(ZnFe2O4)可用于循环分解水制氢气,其反应可表示为:
![]() ;
;![]()
(1) ZnFe2O4中Fe的化合价为___________。
(2)该循环制氢中不断消耗的物质是___________。
(3)氢气作为新能源,有不污染环境、热值大、原料来源丰富等优点,但目前并没有被广泛应用,你认为主要原因是_______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为了测定一瓶硫酸铜溶液的溶质质量分数,取出50克该溶液,向其中逐滴加入溶质质量分数为16%的氢氧化钠溶液,反应过程中生成沉淀的质量与所用氢氧化钠溶液质量的关系如图所示:
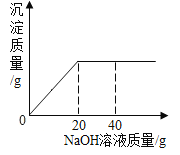
请你仔细分析此关系图,并进行计算。
(1)当滴入氢氧化钠溶液_____克时,硫酸铜与氢氧化钠恰好完全反应。
(2)计算此硫酸铜溶液中溶质的质量分数为_________(写出计算过程)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com