
(6分)氨气(NH3)是一种无色有刺激性气味的气体,极易溶于水,它的水溶液称为氨水,显碱性。氨气在化学工业中用途很广泛,例如制化肥、制纯碱等。近年来,氨气还用于环境治理。
(1)“候氏制碱法”的两步主要反应原理可表示为:① NH3+CO2 +H2O+NaCl = NaHCO3↓+NH4Cl,
② 2NaHCO3 Na2CO3+ H2O + CO2↑。其中,NaHCO3属于 (“酸”、“碱”或“盐”),反应②属于 反应,Na2CO3的俗名叫 。
Na2CO3+ H2O + CO2↑。其中,NaHCO3属于 (“酸”、“碱”或“盐”),反应②属于 反应,Na2CO3的俗名叫 。
(2)在细菌作用下,用氨处理含甲醇的工业废水,使其变为无毒的N2和CO2,从而清除对环境的污染,有关的反应为:6NH3 + 5CH3OH + 12B = 3N2↑+ 5CO2↑+ 19H2O,其中B物质的化学式是_______。
(3)氨气可以被硫酸吸收,生成可以用作氮肥的硫酸铵,该反应的化学方程式为:2NH3+H2SO4 = (NH4)2SO4。若用盐酸吸收氨气,则反应的化学方程式为: 。
(1)盐 分解 纯碱或苏打 (2)O2 (3)NH3 + HCl = NH4Cl
解析试题分析:(1)NaHCO3是于金属离子钠离子和碳酸氢根离子构成,属于盐。反应②属于是由碳酸氢钠一种物质生成碳酸钠、水和二氧化碳三种物质的反应,所以应为分解反应,Na2CO3的俗名叫纯碱或苏打。
(2)根据质量守恒定律可知,反应前后原子的种类和数目均不发生变化。
即12B中含24个氧原子,则B为O2; 反应前的原子个数 反应后的原子个数 原子个数差值 N 6 6 0 H 38 38 0 O 5 29 24 C 5 5 0
(3)根据氨气和硫酸的反应可知,二者发生的为化合反应,且生成铵盐。所以若用盐酸吸收氨气,则反应的化学方程式为:NH3 + HCl = NH4Cl。
考点:物质的分类、基本反应类型、物质的俗名、化学式的推导、化学方程式的书写


科目:初中化学 来源: 题型:填空题
(6分)归纳总结对比分析是学习化学常用的科学方法,如图所示:两圆重迭的区域表示它们的共同特征(相似点),重迭区域以外的部分表示它们的独有特征(不同点)
(1)观察A图,从组成角度写出与上图区域①相对应的适当内容
。(填一点)
(2)观察B图,写出符合②的酸的化学性质
、 .(填两点)还可看出酸和碱都能与某些盐发生反应,请你写出既能与盐酸反应,又能与熟石灰发生化学反应一种盐的化学式为 。
(3)观察C图,从物质分类上写出符合④⑤的物质的化学式 、 。
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
(4分)
沐溪学校的环保小组准备调查研究纸厂附近的水源污染状况,进行下列实验:
(1)你认为在设计方案时拟定的水样采集点应为 。
A.上游居民区用水处 B.下游居民区用水处
C.造纸厂排污处 D.三处都选
(2)如果测得纸厂向沐溪河中排放废液的pH为8,则废液呈 性,该污水中不可能含有大量的离子是 。
A. H+ B.OH- C.Na+ D.CO32-
(3)如果用下列方法判断废液的酸碱性,得出的结论中错误的是 。
A.滴入无色酚酞溶液,溶液变红色,则该废液显碱性
B.滴入紫色石蕊溶液,溶液变蓝色,则该废液显碱性
C.通入二氧化碳气体,溶液无明显变化,则该废液显碱性
D.用试管取废液少许,滴入硫酸铜溶液,有蓝色沉淀生成,则该废液显碱性
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
二氧化碳与氢氧化钠溶液作用没有明显的现象,某同学设计了如下图所示的实验装置(A、B是气球)。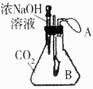
(1)若该装置气密性良好,则将氢氧化钠溶液滴入锥形瓶中可观察到什么现象?______________________________________________,
试解释产生此现象的原因。
______________________________________________。
(2)氯气(C12)是一种有刺激性气味,有毒的气体,氯气可与水反应:C12+H2O=HCl+HCIO(次氯酸)。若将锥形瓶中的CO2气体换成氯气,也可产生上述现象。试写出氯气与氢氧化钠溶液发生反应的化学方程式。
___________________________________________________________________。
(3)若想使装置中产生的现象与(1)中的现象相反,则胶头滴管和锥形瓶中应分别装入什么药品(写出一组即可)_________________________________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
下面图A和图B是学习盐酸化学性质时产生的图像。请根据有关信息,按要求回答问题: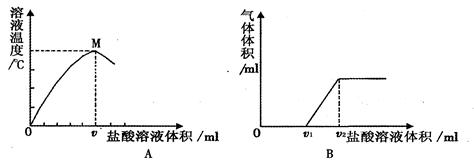
(1)图A是将稀盐酸慢慢滴入装有氢氧化钠溶液的保温仪器中,用温度计测出其中溶液的温度,溶液温度随加入稀盐酸质量增加而发生变化关系图。图中M的意义是 ;所加盐酸体积大于vmL后,温度下降的原因是 。
(2)图B是向碳酸钠溶液中逐滴加入盐酸时产生的气体的体积图像,该图像说明向碳酸钠溶液中加入盐酸时反应分两步完成。第一步,当加入盐酸的体积在0~vlmL时无气泡产生,此时发生的反应是Na2CO3+HCl=NaHCO3+NaCl;第二步,当加入盐酸的体积大于v1mL后,产生气体,反应的化学方程式为NaHCO3+HCl=NaCl+CO2↑+H2O。当所加盐酸的体积等于v1mL时,溶液的pH 7;当所加盐酸体积大于v2mL时,溶液中的溶质是 。
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
“白铁皮”具有较强的耐腐蚀性,是生产中常用的金属材料之一。镀锌层犹如铁皮的保护层,这层膜的厚度是判断镀层质量的重要指标。某研究性学习小组为了测定镀锌铁皮镀锌层的厚度,设计了下面的实验方案。
(1)讨论:在铁皮表面镀锌是为了 。(填字母)
a 锌没有铁活泼,镀在铁的表面可防止生锈
b 锌比铁活泼,并且在空气中容易形成致密的氧化膜,防止生锈
(2)甲同学的方案是:如图1,将镀锌铁皮浸泡在盐酸中,先用盐酸将镀锌铁皮表面的锌反应掉,通过测量因产生气体而形成差量计算出锌的质量,然后再计算得到锌层的厚度。但是乙同学回顾起上课时老师演示的“用足量盐酸除铁锈”的实验现象,马上对甲同学的方案的可行性提出了异议,乙同学的理由是 。
(3)乙同学查阅资料:ZnCl2、FeCl2都能与NaOH溶液反应,生成难溶于水Zn(OH)2和
Fe(OH)2,而Zn(OH)2既可以溶于酸也可以溶于碱,Fe(OH)2则只能溶于酸,于是设计了如下方案:
步骤②中加入足量氢氧化钠的目的是 。
(4)丙同学设计通过测量镀锌铁皮与酸反应产生气体的体积来计算锌层的厚度,他设计了如图2所示装置。其中仪器A中盛放的是镀锌铁皮,仪器B中盛放的是稀硫酸。
①选择用稀硫酸而不用浓盐酸的原因是 。
②检查量气装置气密性:连接好装置,关闭弹簧夹,从量气管注水,若观察到 ,说明该量气装置气密性良好。
③若分液漏斗上方不连接导管a,则测出气体体积会 (选填“偏小”、“偏大”或“没有影响”)。
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
(8分)归纳总结是化学学习的常用方法,下图是对生成物质A的反应关系的归纳与整理。
请回答下列问题:
(1)写出A的化学式: ,反应③
的基本厦应类型是 。
(2)写出反应⑤的化学方程式:
。
该反应在医疗上的用途是: 。
(3)反应⑥能够进行的原因是 。
(4)请根据上图的反应关系,总结出盐酸化学性质。(任写2点)
、 。
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
某同学把自制的一种黄色花汁,分别滴加到下列不同的试剂中,并记录观察到的现象如下表所示。
| 试剂 | 稀盐酸 | 食醋 | 蔗糖水 | 蒸馏水 | 肥皂水 | 烧碱溶液 | 石灰水 |
| 颜色 | 红 | 红 | 黄 | 黄 | 绿 | 绿 | 绿 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
化学就在我们身边,我们的衣、食、住、行都离不开化学。例如,澳网赛冠军李娜所穿的运动服是由棉纤维和合成纤维混合纺织的,这样的运动服应具备的优点有(1) (至少答三点);李娜所使用的球拍是由碳纤维制成的,它属于(2) 材料;运动员要有良好的身体素质,每天需要食用一定量的牛奶、蔬菜和面包等,这些食物中能为人体提供能量的营养素是(3) 。蔬菜所提供的主要营养素(除水外)的作用是(4) ;绿叶蔬菜在生长过程中出现了叶片的边缘发黄的症状,可以施加一定量的农家肥(5) ,可改变上述症状。硝酸铵是一种常用的氮肥,受猛烈撞击时易爆炸分解成两种空气中较多的气体和一种常见液体,请写出反应的化学方程式(6) ,该反应前后氮元素的化合价分别为(7) 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com