
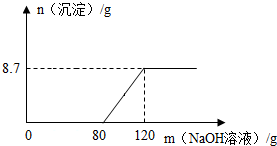
 做完氢氧化钠与稀硫酸中和反应的实验后,兴趣小组的同学对反应后溶液中的溶质成分产生了兴趣,请你于他们一起进行以下探究.
做完氢氧化钠与稀硫酸中和反应的实验后,兴趣小组的同学对反应后溶液中的溶质成分产生了兴趣,请你于他们一起进行以下探究.| 实验操作 | 实验现象 | 实验结论 | |
| 乙同学 实验 | 取中和反应后的溶液少许于试管中,将表面反复打磨后的铝片放入试管内的溶液中 | 铝片逐渐溶解,并有大量气泡冒出,收集气体点燃,火焰呈淡蓝色 | 猜想(2)成立 |
| 丙同学 实验 | 取中和反应后的溶液少许于试管中,向试管内滴加几滴无色酚酞试液 | 无色溶液变成红色 | 猜想(3)成立 |
分析 氢氧化钠和稀硫酸恰好完全反应时,溶质是硫酸钠,稀硫酸过量时,溶质是硫酸钠和硫酸,氢氧化钠过量时,溶质是硫酸钠和氢氧化钠;铝能和稀硫酸反应生成硫酸铝和氢气,能和氢氧化钠反应生成偏铝酸钠和氢气,氢气燃烧时发出淡蓝色火焰;稀硫酸显酸性,不能使酚酞试液变色,氢氧化钠溶液显碱性,能使酚酞试液变红色;
解答 解::【作出猜想】丁同学认为溶液中的溶质有Na2SO4、NaOH和H2SO4三种物质,如果NaOH和H2SO4同时存在则发生综合反应,故丁同学的猜想一定不成立;故填:丁;
【实验验证】实验过程如下表所示:
| 实验操作 | 实验现象 | 实验结论 | |
| 乙同学 实验 | 取中和反应后的溶液少许于试管中,将表面反复打磨后的铝片放入试管的溶液中 | 铝片逐渐溶解,并有大量气泡冒出,收集气体点燃,火焰呈淡蓝色 | 猜想Ⅱ成立 |
| 丙同学 实验 | 取中和反应后的溶液少许于试管中,向试管中滴加几滴无色酚酞试液 | 溶液变红色 | 猜想Ⅲ成立 |
点评 实验现象是物质之间相互作用的外在表现,因此要学会设计实验、观察实验、分析实验,为揭示物质之间相互作用的实质奠定基础.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:选择题
| A. | 复方篙甲醚属于氧化物 | |
| B. | 复方篙甲醚由47个原子构成 | |
| C. | 复方篙甲醚的相对分子质量为298g | |
| D. | 复方篙甲醚中各原子的个数比是16:26:5 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
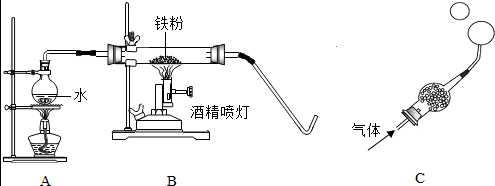
| 常见铁的氧化物 | FeO | Fe2O3 | Fe3O4 |
| 颜色、状态 | 黑色粉末 | 红棕色粉末 | 黑色晶体 |
| 能否被磁铁吸引 | 否 | 否 | 能 |
| 能否与盐酸反应 | 能 | 能 | 能 |
| 实验操作 | 实验现象及结论 |
取少量黑色固体于试管中,加入足量的稀盐酸 | 若固体全部溶解,没有气泡冒出,则猜想二正确;若固体全部溶解,有气泡冒出,则猜想一正确. |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 氧化物中含有氧元素,但含有氧元素的化合物不一定是氧化物 | |
| B. | 单质是由同种元素组成,但同种元素组成的物质不一定是单质 | |
| C. | 酸中都含有氢元素,只要含有氢元素的物质都是酸 | |
| D. | 中和反应一定是复分解反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
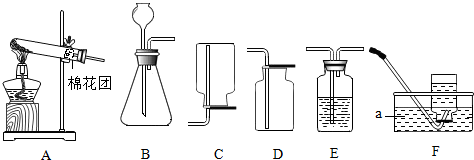
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
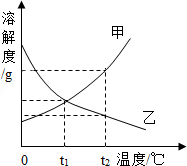 甲乙两种固体物质的溶解度曲线如图所示,若分别将100g甲乙的饱和溶液从t2℃降温到t1℃,对所得溶液的叙述正确的是( )
甲乙两种固体物质的溶解度曲线如图所示,若分别将100g甲乙的饱和溶液从t2℃降温到t1℃,对所得溶液的叙述正确的是( )| A. | 溶质质量分数:甲>乙 | B. | 所含溶剂质量:甲>乙 | ||
| C. | 溶液质量:甲>乙 | D. | 甲乙都是饱和溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
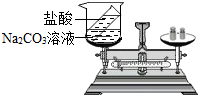 验证质量定律:有人设计如图所示的实验来验证质量守恒定律,把装有稀盐酸的小试管放入盛有碳酸钠溶液的烧杯中,将将烧杯放到托盘天平上,用砝码平衡.取下烧杯并将其倾斜,使两种溶液混合反应,再把烧杯放到天平上,观察天平是否平衡.
验证质量定律:有人设计如图所示的实验来验证质量守恒定律,把装有稀盐酸的小试管放入盛有碳酸钠溶液的烧杯中,将将烧杯放到托盘天平上,用砝码平衡.取下烧杯并将其倾斜,使两种溶液混合反应,再把烧杯放到天平上,观察天平是否平衡.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com