
分析 (1)根据氧化铁与足量一氧化碳充分反应的化学方程式和氧化铁的质量,列出比例式,就可计算出需要一氧化碳的质量.根据反应开始需要通一段时间的一氧化碳将玻璃管内空气排净进行分析.
(2)根据化学反应前后元素的种类和质量不变解答.
解答 解:
(1)设需要一氧化碳的质量为x.生成铁的质量为y
3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2
84 160 112
x 40g y
$\frac{84}{x}=\frac{160}{40g}$
x=21g;
$\frac{160}{40g}=\frac{112}{y}$
y=28g
反应开始需要通一段时间的一氧化碳将玻璃管内的空气排净,防止一氧化碳和空气的混合气加热发生爆炸,所以若要还原40g氧化铁,需要一氧化碳的质量大于21g;
(2)理论上可制得的硫酸亚铁晶体(FeSO4•7H2O)的质量=28g÷$\frac{56}{56+32+16×3+7×(1×2+16)}×$100%=131g
答案:
(1)C;
(2)理论上可制得的硫酸亚铁晶体(FeSO4•7H2O)的质量为131g.
点评 本题主要考查学生运用化学方程式综合分析和解决实际问题的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.


科目:初中化学 来源: 题型:实验探究题
 小乐发现切过咸菜的铁质菜刀很容易生锈,她猜测可能是咸菜中的盐水加快了铁的锈蚀,于是它设计了如图所示的实验:
小乐发现切过咸菜的铁质菜刀很容易生锈,她猜测可能是咸菜中的盐水加快了铁的锈蚀,于是它设计了如图所示的实验:
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
 全球近140个国家将在2020年前禁止生产和出口含汞产品,如荧光灯、化妆品、血压计等.关于汞元素的相关信息正确的是( )
全球近140个国家将在2020年前禁止生产和出口含汞产品,如荧光灯、化妆品、血压计等.关于汞元素的相关信息正确的是( )| A. | 汞的化学式为Hg | B. | 汞原子的质量为200.6g | ||
| C. | 汞原子的中子数是80 | D. | 汞为非金属元素 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
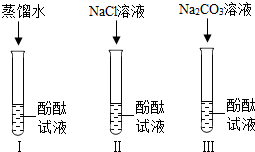 实验小组同学在实验中发现Na2CO3溶液能使酚酞试液变红色.于是他们进行了以下实验探究:
实验小组同学在实验中发现Na2CO3溶液能使酚酞试液变红色.于是他们进行了以下实验探究:查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
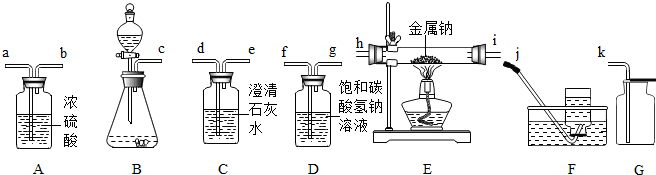
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
 2015年8月为了纪念抗日战争暨世界反法西斯战争胜利70周年,中国人民银行发行纪念币一套,其中面值100元的纪念币中含有0.25盎司的金.从微观角度分析,构成金的微粒是( )
2015年8月为了纪念抗日战争暨世界反法西斯战争胜利70周年,中国人民银行发行纪念币一套,其中面值100元的纪念币中含有0.25盎司的金.从微观角度分析,构成金的微粒是( )| A. | 原子 | B. | 分子 | C. | 离子 | D. | 质子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com