
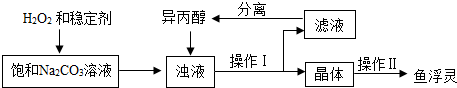
| 温度范围/℃ | 5~10 | 10~15 | 15~20 | 20~25 |
| 活性氧含量/% | 13.94 | 14.02 | 15.05 | 14.46 |
| “鱼浮灵”的产率/% | 85.49 | 85.78 | 88.38 | 83.01 |
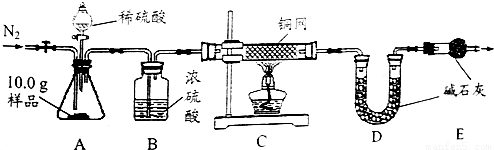
分析 (1)二氧化锰是过氧化氢分解的催化剂,氧气能使带火星的木条复燃;
(2)二氧化碳能使带澄清石灰水变浑浊,此反应可检验二氧化碳的存在;
(3)实验中加入稳定剂的作用是为防止过碳酸钠分解而失效;根据反应物、生成物,书写化学方程式;
(4)根据表中数据可以看出,在15℃~20℃时,活性氧含量最高,鱼浮灵产率最高;
(5)实验前通氮气是为了除去装置内的空气,以防测定值偏高;实验后还要继续通氮气是为了使残留在装置中的气体全部被吸收;
(6)若先滴入稀硫酸,后加热铜网,将使部分氧气散逸,计算时过氧化氢相对含量偏小,碳酸钠相对含量偏大,导致x:y的值偏大;
(7)装置B的作用是干燥气体,防止水分进入D装置使测定值偏大;同时便于观察和控制气流速度以使反应充分进行;
(8)C装置中铜网增重1.2g,则说明生成氧气的质量为1.2g,氧气质量占样品的百分数(活性氧含量)为12%大于10.5%而小于13%,属于合格品;由氧气质量可计算过氧化氢质量为2.55g;D装置增重2.2g说明生成二氧化碳2.2g,计算反应的碳酸钠质量为5.3g,则可得:106x:34y=5.3g:2.55g,故解得x:y=2:3.
解答 解:
(1)由结论“说明有O2生成”,再根据:氧气能使带火星的木条复燃,则填复燃;
(2)根据题目中信息“将产生的气体通入澄清石灰水中,出现浑浊现象”,再根据:二氧化碳能使带澄清石灰水变浑浊,则此题结论为有 CO2(或二氧化碳)生成.
(3)实验中加入稳定剂的作用是为防止H2O2分解(或防止过碳酸钠分解)而失效;稳定剂中的氯化镁MgCl2与硅酸钠Na2SiO3发生复分解反应,能生成氯化钠和难溶的硅酸镁,覆盖在过碳酸钠表面起保护作用,其化学方程式为MgCl2+Na2SiO3=MgSiO3↓+2NaCl.
(4)由表中数据可以看出,在15℃~20℃时,活性氧含量最高,鱼浮灵产率最高,所以最好在该温度范围内制备鱼浮灵.
(5)实验前通氮气一段时间,加热铜网至红热后,再缓慢滴入过量稀硫酸,直至A中样品完全反应是为了除去装置内的氧气,以防测定值偏高;实验后还要继续通氮气是为了使残留在装置中的气体全部被装置吸收;
(6)根据【组成测定】利用如图装置进行产品中活性氧含量测定和过碳酸钠(xNa2CO3•yH2O2)组成的测定.若先滴入稀硫酸,后加热铜网,将使部分氧气散逸,计算时过氧化氢相对含量偏小,碳酸钠相对含量偏大,导致x:y的值偏大;
(7)装置B的作用是干燥气体,防止水分进入D装置使测定值偏大;同时便于观察和控制气流速度以使反应充分进行,故选①②;
(10)C装置中铜网增重1.2g,则说明生成氧气的质量为1.2g,氧气质量占样品的百分数(活性氧含量)为$\frac{1.2g}{10g}$=12%大于10.5%而小于13%,“资料中鱼浮灵中活性氧含量≥13.0%是一等品,≥10.5%是合格品”,故此产品属于合格品;
因为生成氧气的质量为1.2g,则设需要过氧化氢的质量为x.
2H2O2~O2↑
68 32
x 1.2g
则$\frac{68}{x}$=$\frac{32}{1.2g}$
解得x=2.55g,故由氧气质量可计算过氧化氢质量为2.55g.
因为D装置增重2.2g说明生成二氧化碳2.2g,则设需要碳酸钠质量为y.
Na2CO3~CO2
106 44
y 2.2g
则$\frac{106}{y}$=$\frac{44}{2.2g}$
解得y=5.3g,故计算反应的碳酸钠质量为5.3g,
根据“产品中活性氧含量测定和过碳酸钠(xNa2CO3•yH2O2)组成”,则可得:106x:34y=5.3g:2.55g,故解得x:y=2:3.
故答案为:
(1)复燃;(2)CO2(或二氧化碳);
(1)复燃
(2)CO2
(3)防止过碳酸钠分解而无效 或 防止过氧化氢分解; MgCl2+Na2SiO3=MgSiO3↓+2NaCl
(4)15~20
(5)使残留在装置中的气体全部被吸收
(6)偏大
(7)①②
(8)2:3
点评 本题主要考查学生运用所学化学知识综合分析和解决实际问题的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.


 小天才课时作业系列答案
小天才课时作业系列答案 一课四练系列答案
一课四练系列答案 黄冈小状元满分冲刺微测验系列答案
黄冈小状元满分冲刺微测验系列答案 新辅教导学系列答案
新辅教导学系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 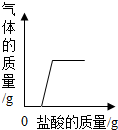 在部分变质的NaOH溶液中滴加稀盐酸 | |
| B. | 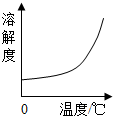 O2的溶解度受温度影响的变化曲线 | |
| C. |  等质量的Mg粉和Fe粉与足量同浓度的稀盐酸反应 | |
| D. | 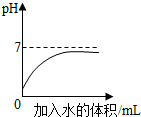 硫酸溶液稀释过程中pH的变化曲线 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 只有③ | B. | 只有①③ | C. | 只有②③ | D. | ①②③ |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 5g | B. | 10g | C. | 30g | D. | 40g |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
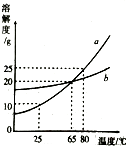 如图为a、b两物质的溶解度曲线,据图回答:
如图为a、b两物质的溶解度曲线,据图回答:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com