
【题目】小苏打和食盐是厨房中常用物质。现有一包白色固体,可能由 NaHCO3 和 NaCl 中的一种或两种组成。某科学小组同学展开了系列拓展性研究。
(一)定性
(实验目的)确定白色固体的组成
(实验方案)

(实验结论)该白色固体由_____组成;
(1)实验步骤①中选用稀硝酸而不用稀盐酸的原因是_____;
(2)实验步骤②中生成白色沉淀的化学反应方程式为_____。
(二)定量分析
(实验目的)测定该白色固体中 NaHCO3 的质量分数
(实验方案)用气体法测定样品中 NaHCO3 的质量分数。实验装置如下:
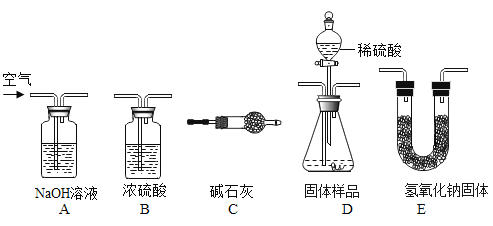
(1)用上述装置完成本实验,装置的连接顺序是 A→_____→_____→_____→C(填装置的字母编号,不重复使用);
(2)D 装置中发生反应的化学方程式为_____;
(3)如果没有经过 A 装置而直接通入空气,会使测量结果_____(填“变大”、“变小”或“不变”);
(4)C 装置的作用是_____;
(5)D 装置中的反应完全后,称量前,还需要进行的实验操作是_____。
【答案】NaHCO3 和 NaCl 防止带入氯离子,对氯化钠的检验造成干扰 CO2+Ca(OH)2=CaCO3↓+H2O D B E 2NaHCO3+H2SO4=Na2SO4+2CO2↑+2H2O 变大 防止空气中的二氧化碳和水蒸气进入装置造成实验误差 A 装置中继续通入空气
【解析】
(一)定性
实验结论:样品与过量的硝酸反应生成气体,气体能与澄清石灰水产生白色沉淀,说明样品中存在碳酸氢钠;
样品与过量硝酸反应生成溶液中加入硝酸银溶液,产生白色沉淀,氯化钠与硝酸银反应生成氯化银沉淀和硝酸钠,说明样品中存在氯化钠。该白色固体由NaHCO3 和 NaCl组成;
(1)实验步骤④中选用稀硝酸而不用稀盐酸的原因是稀盐酸中含有氯离子,影响对氯化钠的检验;
(2)实验步骤②中生成白色沉淀,是因为氢氧化钙与二氧化碳反应生成碳酸钙和水,反应的化学反应方程式为:CO2+Ca(OH)2=CaCO3↓+H2O;
(二)定量分析
(1)用上述装置完成本实验,装置的连接顺序是A(除去空气中二氧化碳)→D(反应生成二氧化碳)→B(吸收水蒸气)→E(吸收二氧化碳)→C(防止二氧化碳和水蒸气进入E装置)故填:D→B→E;
(2)D装置中碳酸氢钠和稀硫酸反应生成硫酸钠、水和二氧化碳,发生反应的化学方程式为:2NaHCO3+H2SO4=Na2SO4+2CO2↑+2H2O;
(3)如果没有经过A装置而直接通入空气,会导致测定的二氧化碳质量判断,从而使测量结果变大;
(4)C装置的作用是防止空气中的二氧化碳和水蒸气进入装置造成实验误差;
(5)D装置中的反应完全后,称量前,还需要进行的实验操作是继续通入空气,使反应生成的二氧化碳全部被氢氧化钠吸收。


 课时掌控随堂练习系列答案
课时掌控随堂练习系列答案 一课一练一本通系列答案
一课一练一本通系列答案 浙江之星学业水平测试系列答案
浙江之星学业水平测试系列答案科目:初中化学 来源: 题型:
【题目】某校化学兴趣小组在查阅资料时发现:可燃物燃烧需要的最低氧含量数据如下表。
可燃物名称 | 蜡烛 | 木炭 | 棉花 | 红磷 | 白磷 |
最低氧含量/% | 16 | 14 | 8 | 8.8 | 3.2 |
请结合数据回答下列问题:
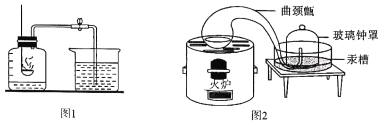
(1)图1为教材中测量空气中氧气体积分数的实验装置图,请写出集气瓶中发生的化学反应程式:___________。结合数据,你认为红磷适合于测量空气中氧气的体积分数吗?并说明你的理由:_________。但实验过程中又确实看到进来的水的体积约占集气瓶内容积的1/5,其原因可能是________。
(2)图2是拉瓦锡的实验装置,回看拉瓦锡的实验,选择汞的优点有_________(填序号,多选)。
A 实验过程没有污染
B 生成的化合物加热分解后又得到汞和氧气
C 在汞槽中起到液封作用
D 能将密闭装置内空气中的氧气几乎耗尽
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是某同学探究二氧化碳性质的实验,请回答:
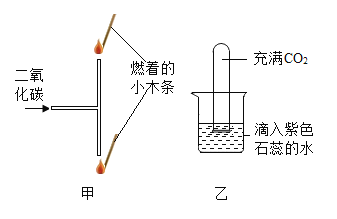
(1)依据二氧化碳_____________的性质设计甲实验,观察到的现象应该是________ 。
(2)乙实验,将充满CO2的试管倒扣在滴有紫色石蕊溶液的蒸馏水中,一段时间后,观察到的现象是________,请解释产生此现象的原因____________,并写出反应的化学方程式__________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学实验是学习化学的基础。请根据下列装置图回答问题。
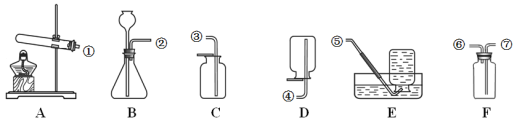
(1)实验室可以利用加热醋酸钠固体和氢氧化固体的混合物来制取甲烷,则选择的发生装置是__________(填字母代号);收集某种气体能用 C、D、E 装置中的 D 收集,则该气体具备的物理性质是___________。
(2)实验室制备 CO2 的药品是_______________;若用装置 B 和 F 制备并收集 CO2,则接口②应与 ___________;(填接口序号)相连;
(3)若制备并收集干燥的二氧化碳,需要的装置是_______________(从 A~F 中选填),需要的干燥剂 是_______________。将二氧化碳气体通入到氢氧化钠溶液中的化学方程式为______________,继续向上述反应后的溶液中,加入氯化钡溶液现象是_______________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据如图所示溶解度曲线判断,下列说法正确的是( )
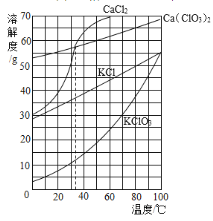
A. 20℃时,将10 g KClO3加入100 g水中,溶液质量为110 g
B. 30℃时,KCl饱和溶液中溶质的质量分数约为35%
C. 分别将35℃的CaCl2和Ca(ClO3)2两种饱和溶液升温至40℃,CaCl2溶液中溶质的质量分数较大
D. 除去CaCl2中混有的少量Ca(ClO3)2,可在较高温度配成饱和溶液,再降温结晶、过滤
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列图象能正确反映对应操作的是( )
A. 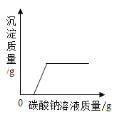 向一定质量的氯化钙溶液中加入碳酸钠溶液
向一定质量的氯化钙溶液中加入碳酸钠溶液
B. 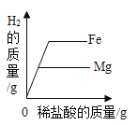 分别向足量的稀盐酸中加等质量的铁和镁
分别向足量的稀盐酸中加等质量的铁和镁
C. 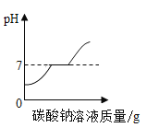 向氯化钙和盐酸的混合溶液中加入过量的碳酸钠溶液
向氯化钙和盐酸的混合溶液中加入过量的碳酸钠溶液
D. 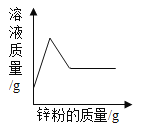 向硝酸银和硝酸铜混合溶液中加入过量的锌粉
向硝酸银和硝酸铜混合溶液中加入过量的锌粉
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】海洋是人类宝贵的自然资源,海水“制盐”体现了人类利用化学科学征服和改造自然的智慧。通过晾晒海水,可以得到粗盐,担盐中含有不溶性杂质(如泥沙等)和可溶性杂质(如MgCl2、CaC12等),工业上以粗盐为原料制取精盐,其生产流程如图所示
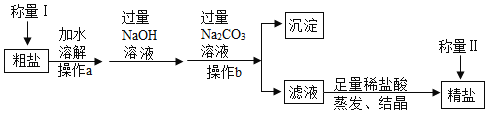
请回答下列问题:
(1)操作b中玻璃棒的作用是_____。
(2)加入Na2CO3溶液除去的离子是_____(填离子符号),加入NaOH溶液发生反应的化学方程式为_____;
(3)滤液中溶质的主要成分是_____(填化学式),加入足量稀盐酸的目的是_____。
(4)如果称量Ⅰ中称得粗盐的质量为3g,称量Ⅱ中称得精盐的质量为3.1g,则下列分析正确的是_____(填字母)
A 精盐的产率为103.3%
B 蒸发操作中可能有水分没有蒸干
C 除杂过程中有NaCl生成
D 溶解操作中粗盐没有完全溶解
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】中国是把香椿当做蔬菜的唯一国家,它不仅营养丰富,而且具有极高的药用价值,如香椿中含有的皂甙,具有抗菌、防癌的作用,皂甙的化学式为C27H42O3,请你计算:
(1)皂甙属于_______________(填“有机物”或“无机物”);
(2)皂甙中各元素的质量之比是____________________(最简整数比);
(3)含氢元素8.4 g的皂甙的质盆为________________克(写出计算过程)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲和乙两种物质的溶解度曲线如图所示。下列叙述正确的是( )
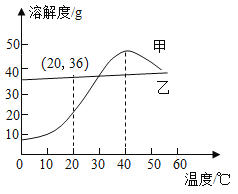
①甲的溶解度随温度的升高而增大
②40℃时,使甲的饱和溶液析出晶体可用加热升温、冷却降温和蒸发溶剂三种方法
③20℃时,向125g溶质质量分数为20%的乙溶液中加入15g乙固体并振荡,有固体不溶解
④将相同质量的甲和乙的饱和溶液分别从40℃降温至10℃,甲析出晶体的质量大
A. ①②B. ③④C. ①③④D. ②③④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com