
科目: 来源: 题型:
【题目】80g质量分数为40%的氢氧化钠溶液与一定质量的氯化镁溶液混合,恰好完全反应,经过滤,得到滤液的质量为216.8g。请计算:
(1)原氯化镁溶液中溶质的质量分数;
(2)所得滤液中溶质的质量分数(计算结果精确至0.1%)。
查看答案和解析>>
科目: 来源: 题型:
【题目】维生素C(C6H8O6)主要存在于蔬菜,水果中,它能促进人体生长发育,增强人体对疾病的抵抗力.计算:
(1)维生素C的相对分子质量 .
(2)维生素C中碳、氢两种元素的质量比 (写最简比).
(3)维生素C中 元素的质量分数最大.
查看答案和解析>>
科目: 来源: 题型:
【题目】甲、乙、丙三种固体物质的溶解度曲线如图所示,回答下列问题:
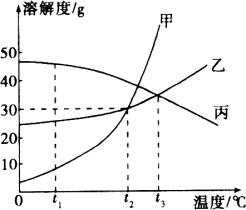
(1)t1℃时,甲、乙、丙三种物质的溶解度由大到小的顺序是________;
(2)t2℃时,甲和乙的溶解度________(填“相等”或“不相等”);
(3)t2℃时,甲物质的饱和溶液中溶质与溶剂的质量比为________(写最简比);
(4)t3℃时,将乙和丙两种物质的饱和溶液降低到t1℃,所得溶液中溶质的质量分数大小关系为:乙________丙(填“>”“<”或“=”).
查看答案和解析>>
科目: 来源: 题型:
【题目】某同学在实验室用氯酸钾和二氧化锰的混合物制取氧气,并对反应后固体剩余物进行回收、利用,实验操作流程及数据记录如下:

请回答下列问题:
(1)滤液可作化肥使用,你认为它属于_______肥。
(2)该同学制得氧气的质量_______g。
(3)计算滤液中溶质质量分数。
查看答案和解析>>
科目: 来源: 题型:
【题目】早在春秋战国时期,我国就开始生产和使用铁器。从1世纪起,铁成了一种最主要的金属材料,工业上可利用一氧化碳还原赤铁矿制得金属铁。
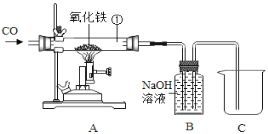
(1)如下图回答问题:
①加热一段时间后玻璃管内的现象是_____,反应的化学方程式为_____
②你认为B装置的优点是_____
(2)工业上可利用“铝热反应”焊接钢轨、冶炼难熔金属等,其原理是在高温下用铝将某些金属从其氧化物中置换出来,在高温下铝与四氧化三铁反应的化学方程式为_____。
(3)向硝酸银、硝酸铜和硝酸锌的混合溶液中,加入一定量的铁粉,充分反应后过滤,向过滤出的固体中滴加稀硫酸,有气体生成,则过滤出的固体中一定有_____.
(4)现有一包黑色固体粉,可能含有炭粉、CuO、Fe3O4中的两种或者三种,某化学兴趣小组通过实验探究其成分。
I提出问题:该黑色固体粉末成分是什么?
II作出猜想:猜想一:混合固体是炭粉、CuO
猜想二:混合固体是炭粉、Fe3O4
猜想三:混合固体是_____(两种物质写不全不给分)
猜想四:混合固体是炭粉、CuO、Fe3O4
III查阅资料:Fe3O4为黑色粉末,能与盐酸反应,含有Fe3+的盐溶液遇到KSCN(硫氰化钾)溶液时变成红色,Fe(OH)2是一种白色沉淀。
IV实验探究:取一定量的固体于试管中,加足量的盐酸,充分反应后有部分固体溶解,过滤,得到滤液A,并对滤液A的成分进行如下探究:
实验操作 | 实验现象 | 实验结论 |
步骤一:取一定量滤液A于试管中,加入足量的铁粉 | 无红色固体析出 | 该固体物质一定没有_____ |
步骤二:又取一定量的滤液A于试管中,加入少量的KSCN(硫氰化钾)溶液 | 溶液变成红色 | 滤液A中还一定含有的物质是_____ |
步骤三:再取一定量的滤液A于试管中,加入足量的NaOH溶液 | 有红褐色沉淀生成,同时还有少量的白色沉淀生成,白色沉淀迅速变成灰绿色,最后面变成红褐色 | 滤液A中还一定含有的物质是_____ |
V讨论交流:
①通过以上实验,猜想_____成立。
②写出Fe3O4与盐酸反应的化学方程式_____。
③Fe3O4与盐酸反应时元素的化合价没有改变,请大家推断Fe3O4中铁元素的化合价为_____(写两种价态才得分)。
VI拓展:请写出同种元素显不同化合价的一种盐_____(其它合理答案也得分)
查看答案和解析>>
科目: 来源: 题型:
【题目】“化学究竟是什么,化学就是你,化学究竟是什么,化学就是我,化学究竟为什么,化学为了你…”.一首神曲唱出了化学对人类的贡献.在日常生活中化学无处不在.
(1)在人类食物所供给的总能量中,有60%~70%来自_____。
(2)人体血液中的血红蛋白在吸入氧气和呼出二氧化碳的过程中起着载体的作用与含有的亚铁离子密切相关,写出亚铁离子的符号_____;
(3)亚硝酸盐是一类无机化合物的总称,主要指亚硝酸钠,它是白色或淡黄色粉末,有咸味,易溶于水,水溶液呈碱性,亚硝酸钠由钠、氮、氧三种元素组成,其中氮的化合价为+3价,亚硝酸钠的化学式为_____;鉴别食盐和亚硝酸钠可用_____溶液。
(4)食品包装袋中经常用生石灰作干燥剂,写出生石灰干燥原理的化学方程式:_____。
(5)“神舟十号”飞船的发射让航天员再次访问“天宫一号”资源舱舱段使用了铝锂合金材料代替传统材料,铝锂合金属于_____材料(“金属”或“合成”或“复合”)。
(6)我国南海神狐海域首次成功试采可燃冰,可燃冰的主要成分是甲烷水合物,请写出甲烷燃烧的化学方程式______
(7)实验室中装有氢氧化钠溶液的试剂瓶不能用玻璃塞,原因是在常温下,NaOH与玻璃塞中的SiO2缓慢地发生反应生成Na2SiO3和H2O.Na2SiO3使瓶口与瓶塞粘合在一起而无法使用.该反应的化学方程式为_____.
查看答案和解析>>
科目: 来源: 题型:
【题目】保险粉(化学式为Na2S2O4)在工农业生产中有广泛的用途,Na2S2O4在碱性溶液中稳定,在中性和酸性溶液中极不稳定,在NaCl存在下,Na2S2O4在水中溶解度显著下降.制备流程如图:
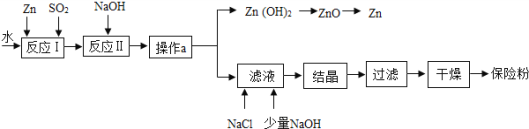
(1)反应Ⅰ的原理为:Zn+2SO2═ZnS2O4,该反应中将锌研磨成粉末的目的:_____;该反应的基本反应类型为_____.
(2)反应Ⅱ为复分解反应,该反应的化学方程式为_____.
(3)操作a得到的滤液有些浑浊,可能的原因_____.
(4)滤液中含有Na2S2O4,为使Na2S2O4结晶析出还需要加入少量NaOH的原因是_____,加入NaCl的原因是_____.
(5)氢氧化锌在加热的条件下分解成两种氧化物,写出氢氧化锌分解的化学方程式:_____
(6)198gZn(OH)2理论上能得到Zn的质量为_____g.
查看答案和解析>>
科目: 来源: 题型:
【题目】从微观的角度了解物质及其变化,有助于更好的认识物质组成和变化的本质。

(1)已知A的相对原子质量为19,粒子A核内中子数为_____,
(2)A与E形成化合物的化学式为_____。
(3)D、E化学性质不同的原因是_____。
(4)如图为两种化合物在一定条件下发生反应的微观示意图:

①该反应的化学方程式为_____。
②上述反应中,作为还原剂的物质是_____(填物质化学式);化合价升高的元素是_____(填元素符号)。
查看答案和解析>>
科目: 来源: 题型:
【题目】如图为某化工企业生产流程示意图,有关说法正确的是( )
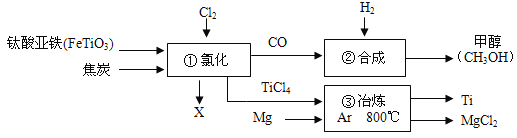
A. ②中为使原料全部转化为甲醇,理论上CO和H2投料的质量比为7:1
B. 钛酸亚铁(FeTiO3)中钛元素为+3价
C. ③的反应属于复分解反应
D. ①中反应为:2FeTiO3 +6C+6Cl2 ![]() 2X+2TiCl4 +6CO,则X为FeCl3
2X+2TiCl4 +6CO,则X为FeCl3
查看答案和解析>>
科目: 来源: 题型:
【题目】下列实验装置进行的相应实验,达不到实验目的是( )
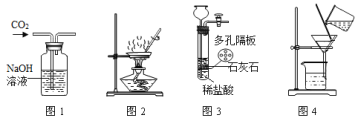
A. 用图1所示装置除去CO2中含有的少量HCl气体
B. 用图2所示的装置加热蒸发NaCl饱和溶液制备NaCl晶体
C. 用图3所示装置可以控制反应的发生和停止
D. 在实验室中,用图4所示装置除去少量河水中的泥沙
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com