
科目: 来源: 题型:
【题目】溶液与人们的生产生活密切相关。
(1)将少量下列物质分别放入水中,充分搅拌,可以得到无色溶液的是_____(填字母)。
A.高锰酸钾 B.汽油 C.面粉 D.白糖
(2)在盛有水的烧杯中加入以下某种物质,形成溶液过程中,温度没有明显变化的 是_____ (填字母)。
A.烧碱 B.硝酸铵 C.氯化钠 D.浓硫酸
(3)下图 1 为甲、乙两种固体物质的溶解度曲线。
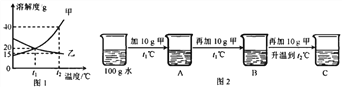
①溶解度随温度升高而增大的物质是_____(填 “甲”或“乙”)。
②某同学按图 2 所示进行实验,得到相应温度下的 A、B、C 溶液,在 A、B、C 三种 溶液中属于饱和溶液的是________(填字母)。向溶液 C 中再加入 25g 甲,充分搅拌, 恢复到 t2℃时,所得溶液中溶质的质量分数为_______________(结果精确到 0.1%)。
③将 t2℃时的甲、乙两种物质的饱和溶液降温至 t1℃,所得溶液中溶质的质量分数 甲_____乙(填“<”、“=”或“>”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列化学实验中能达到预期实验结果的是( )
A.借助托盘天平和其他手段测定铜锌合金中锌的质量分数为36.25%
B.用pH试纸测定某未知溶液的pH为5.5
C.20℃时,配制2%的氢氧化钙溶液
D.将100g 10%的稀盐酸加热蒸发掉50g水,使得稀盐酸溶质质量分数变成20%
查看答案和解析>>
科目: 来源: 题型:
【题目】向AgNO3、Cu(NO3)2、Mg(NO3)2的混合溶液中,加入一定量的铁粉,充分反应后过滤,滤液呈蓝色。下列判断正确的是( )
A. 滤液中可能有Fe(NO3)2、Mg(NO3)2和Cu(NO3)2
B. 向滤渣中加入稀盐酸,可能有气泡产生
C. 与原溶液相比,滤液的质量可能增大
D. 向滤液中滴入稀盐酸,可能会有白色沉淀出现
查看答案和解析>>
科目: 来源: 题型:
【题目】把等质量的X、Y、Z、M四种金属分别加入到等质量、等质量分数的足量稀盐酸中(反应关系如图甲),把金属M加入到足量的Y(NO3)2溶液中(反应关系如图乙)。据此判断四种金属的活动性顺序为
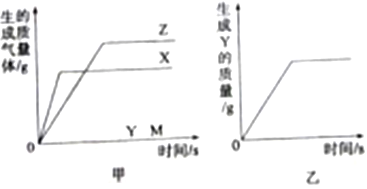
A. X>Z>M>Y B. Y>M>Z>X C. X>Z>Y >M D. Z>X>M>Y
查看答案和解析>>
科目: 来源: 题型:
【题目】等质量的M、N两种金属,分别与相同质量分数的足量稀盐酸反应(已知M、N在生成物中均为+2价),生成氢气质量和反应时间的关系如右图所示,下列叙述正确的是
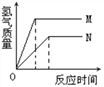
A. M、N两种金属中较活泼的是N
B. 生成H2的质量M<N
C. 相对原子质量较大的是N
D. 产生H2的速率N>M
查看答案和解析>>
科目: 来源: 题型:
【题目】小峰同学在体育课上腿部擦伤,医务室的大夫在他伤口上涂了医用过氧化氢溶液,小峰看到伤口处产生了小气泡,很好奇。为什么瓶中的过氧化氢溶液涂到伤口上,分解就加快了呢?
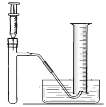
I.小峰准备用如图所示装置测定过氧化氢分解的快慢,实验前在注射器中吸入过氧化氢溶液,量筒内装满水。实验开始时,向试管中注入过氧化氢溶液,并用排水法收集氧气。记录2分钟收集的气体体积。
(1)请写出过氧化氢分解的化学方程式________。
(2)若要检验生成的气体是否为氧气,可将导气管从水中取出,取带火星的木条放在导气管口处,观察到________,说明生成的气体是氧气。
II.小峰查阅了相关资料,并进行了探究实验
(查阅资料)
①过氧化氢是人体代谢废物之一,它能够对机体造成损害,人体存在过氧化氢酶,可以催化过氧化氢分解。
②温度对化学反应的快慢有影响,人体正常体温是37℃。
(提出猜想)
猜想1:过氧化氢分解加快是因为体温比瓶中的温度高。
猜想2:过氧化氢分解加快是因为伤口中有过氧化氢酶。
(进行实验)
序号 | 实验步骤 | 实验现象 | 实验结论 |
① | 分两次进行实验,均注入5mL过氧化氢溶液 第一次在常温下进行 第二次将试管浸在37℃的温水中 | 量筒中2分钟收集到的气体体积均为5ml | |
② | 分两次进行实验 第一次 第二次将装有一小粒过氧化氢酶的试管浸在37℃的温水中,注入5ml过氧化氢溶液 | 第一次,量筒中2分钟收集到的气体体积为5ml 第二次,量筒中2分钟收集到的气体体积为 ml | 过氧化氢分解加快是因为过氧化氢酶的作用 |
(3)实验①得出的结论是_____________。
(4)实验②中“第一次”应进行的操作是_________。
(5)实验②中第二次收集到的氧气体积为________ml。
(实验反思)
小峰反思了实验过程,认为人体中过氧化氢酶是在体温条件下发挥作用的,实验得出的结论可能存在不足。因此又补充进行了几组实验,数据记录如下表所示。
加入过氧化氢酶 | 不加过氧化氢酶 | |||||
反应温度/℃ | 25 | 37 | 42 | 25 | 37 | 42 |
收集到气体体积/mL | 39 | 56 | 34 | 5 | 5 | 5 |
(6)通过这些数据,你能得出的新结论是_______
查看答案和解析>>
科目: 来源: 题型:
【题目】“打好蓝天保卫战、治理大气污染”是提升人民生活质量的重要工作。二氧化硫(SO2)是一种大气污染物。工业上可以利用海水对二氧化硫进行吸收利用,变害为宝。其工艺流程见图:
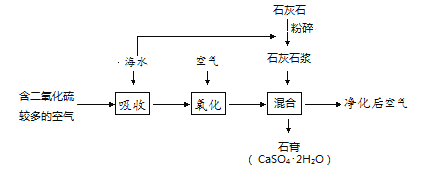
(1)流程中将石灰石加水制成石灰石浆的目的是_______。
(2)其中硫元素的化合价在反应前后的变化为________。.
(3)为了提升脱硫率(脱硫率是指已除去的二氧化硫的量占总二氧化硫量的百分比)与温度、烟气中SO2浓度的关系,技术人员进行了探究实验。实验结果如下:
实验序号 | 温度/℃ | 烟气中SO2浓度/10-2gL-1 | 脱硫率 |
Ⅰ | 23 | 2.5% | 99.5 |
Ⅱ | 23 | 3.2% | 97.1 |
Ⅲ | 40 | 2.5% | 94.3 |
由表中实验数据可得出的结论是_______。
查看答案和解析>>
科目: 来源: 题型:
【题目】高纯氧化铁[Fe2O3]又称“引火铁”,在现代工业上有广泛应用前景。以下是用赤铁矿(含少量不溶于水的SiO2等)为原料,制备高纯氧化铁的生产流程示意图。
小贴士:氨水呈碱性(主要成分NH3H2O是一种碱);(NH4)2CO3溶液呈碱性,40℃以上易分解。
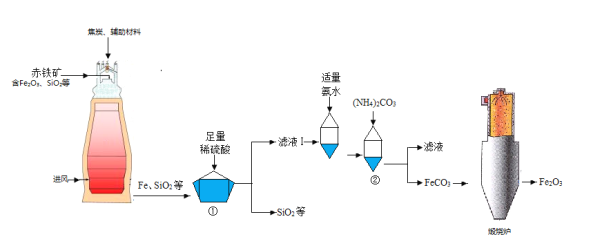
(1)①处发生反应的化学方程式为____________。
(2)加入(NH4)2CO3后,该反应必须控制的条件是________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某小组同学利用如图所示装置探究铁生锈的条件。
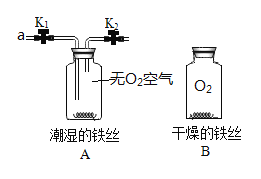
(1)要证明铁生锈与氧气有关,需要进行的实验操作为__________。
(2)实验中能说明铁生锈与水有关的实验现象是________。
(3)充分反应后,将装置A、B中分别注入少量稀盐酸,两个广口瓶中现象的不同点是:_______,由此也可以证明铁丝生锈情况。A中反应的化学方程式是______。
查看答案和解析>>
科目: 来源: 题型:
【题目】如图,化学小组同学制作了一个微型实验装置用来验证二氧化碳的性质。异型玻璃管A内充满了二氧化碳气体(已检查装置气密性),注射器B内吸取了一定量的浓氢氧化钠溶液,广口瓶C中盛有一定量稀盐酸。实验开始前止水夹K处于关闭状态。
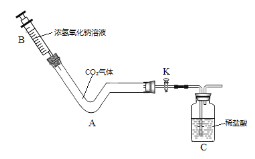
(1)将注射器中氢氧化钠溶液全部推入A中之前要进行的操作是_____。
(2)当C中部分液体流入A中后迅速关闭止水夹K,片刻后可看到的现象是____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com