
科目: 来源: 题型:
【题目】下列图象能正确反应对应变化关系的是( )
A.  将铁钉加入硫酸铜溶液中
将铁钉加入硫酸铜溶液中
B.  向一定量的二氧化锰中加入过氧化氢溶液
向一定量的二氧化锰中加入过氧化氢溶液
C.  向一定量的大理石(杂质不参加反应) 中加入足量的稀盐酸
向一定量的大理石(杂质不参加反应) 中加入足量的稀盐酸
D. 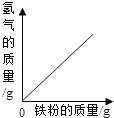 向一定质量的稀盐酸中加入足量铁粉
向一定质量的稀盐酸中加入足量铁粉
查看答案和解析>>
科目: 来源: 题型:
【题目】请利用如图给定的仪器组装成一套测定镁的相对原子质量的实验装置(每种仪器只允许使用一次),用排水法测量化学反应产生氢气的体积,根据化学方程式计算出镁的相对原子质量,回答问题:
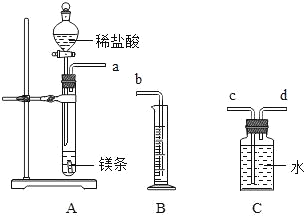
(1)假设气流方向由左向右,则各导管连接的先后顺序为_____(填字母);书写装置A中发生反应的化学方程式_____.
(2)连接好仪器后,要进行的操作有以下几步:①待仪器A中的物质恢复至室温时,测量量筒B中水的体积.②擦掉镁条表面的氧化膜,将其置于天平上称量后,立即将其投入试管A中.③检查装置的气密性.④旋开仪器A上分液漏斗的活塞,当镁条完全溶解时再关闭活塞.上述几步操作中的先后顺序是_____.
(3)分析下列其中一实验步骤出现的状况(其他操作均正确),将会使所测镁的相对原子质量数据偏低的是_____(填字母).
A 装置的气密性不够好
B 装置A的试管中剩余部分产生的氢气
C 若试管A尚未冷却至室温就测量量筒B中水的体积
D 若未擦净镁条表面氧化膜就进行实验
(4)假设在0℃、l01kPa条件下,氢气的密度为0.0899g/L的条件下进行实验,将质量为M克的镁与足量稀盐酸反应产生氢气,收集并测量产生氢气体积为V毫升,计算镁的相对原子质量为_____(填表达式).
查看答案和解析>>
科目: 来源: 题型:
【题目】食盐是一种重要的化工原料,请回答下列问题。
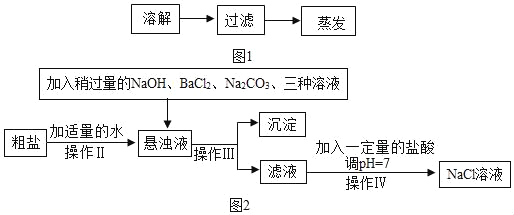
(1)如图1是实验室除去粗盐中泥沙等难溶性杂质的实验步骤。操作Ⅰ的名称是_____。
(2)由于粗盐中还含有少量的MgCl2、CaCl2、Na2SO4等可溶性杂质,不能满足化工生产的要求。因此必须将粗盐进行精制。其流程如图2所示:
①加入稍过量的Na2CO3溶液的目的是除去溶液中的_____ (填离子符号)。
②通过操作Ⅲ所得滤液中的溶质有三种,除了氧化钠外,还有两种,请分别写出它们的化学式_____、_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】A、B、C、D是初中化学常见的物质,其中A为无色气体单质,B、C为氧化物,且B为有毒气体,D是大理石的主要成分,它们之间的转化关系如下图所示(图中反应条件及部分反应物、生成物已省略)。
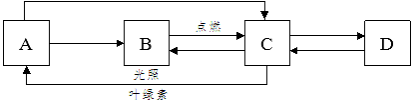
回答下列问题:
(1)写出下列物质的化学式:A ;B ;C 。
(2)实验室常用 鉴别B和C。
(3)写出由物质C转化为物质B的化学方程式 。
(4)写出物质C与过氧化钠(Na2O2)反应生成碳酸钠和物质A的化学方程式 。
查看答案和解析>>
科目: 来源: 题型:
【题目】现有盐酸和氯化镁的混合溶液,向其中逐滴滴入氢氧化钠溶液,生成沉淀质量与滴入氢氧化钠溶液质量的变化关系如图所示。下列说法错误的是

A. 滴加氢氧化钠溶液质量为a~cg时,溶液中发生的反应为:![]()
B. 滴加氢氧化钠溶液质量至ag时,溶液中溶质质量比原混合溶液中溶质质量大
C. 滴加氢氧化钠溶液质量至bg时,溶液中含三种溶质
D. 滴加氢氧化溶液质量至cg时,溶液呈中性
查看答案和解析>>
科目: 来源: 题型:
【题目】向盛有10g49%稀硫酸的烧杯中加入5.6克的铁粉,充分反应后有固体残留,t1时迅速倒入一定量的硫酸铜溶液。整个过程烧杯中溶液的质量随时间的变化如图所示。下列说法正确的是( )
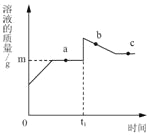
A. 取a点是溶液,加入锌粉,有气体放出
B. b点时,溶液中溶质只有一种
C. c点时,烧杯中固体一定是铜
D. m=12.7
查看答案和解析>>
科目: 来源: 题型:
【题目】下列叙述正确的是( )
A. 大气中二氧化碳含量不断上升,会导致酸雨的形成
B. 把干燥紫色石蕊小花放入盛满干燥的二氧化碳气体的集气瓶中,紫色小花会变红
C. KNO3饱和溶液一定比不饱和溶液溶质质量分数大
D. 焦炭可以通过下列反应还原出铁矿石中的铁:2Fe2O3+3C![]() 4Fe+3CO2↑
4Fe+3CO2↑
查看答案和解析>>
科目: 来源: 题型:
【题目】下列图象能正确反映对应变化关系的是( )
|
|
|
|
A.向一定量的二氧化锰中加入过氧化氢溶液 | B.将铁钉加入硫酸铜溶液中 | C.向一定量的大理石(杂质不参加反应)中加入足量的稀盐酸 | D.向一定质量的稀盐酸中加入足量铁粉 |
A. A B. B C. C D. D
查看答案和解析>>
科目: 来源: 题型:
【题目】某化学兴趣小组在做Fe和CuSO4溶液反应实验时,发现生成Cu的同时有气泡产生。为了进一步探究有气泡产生原因,做了如下实验:
①取8.5gFe粉放入一定量的CuSO4中,反应完成后,滤出固体,洗涤、干燥后称量,固体质量为9.2g。
②将该9.2g固体与一定质量分数的稀盐酸充分反应,消耗盐酸50.0g。根据实验绘制如图所示反应时间与反应产生氢气的质量关系图。
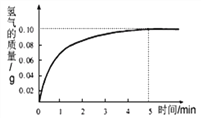
根据提供的有关数据进行下列计算和分析:
(1)根据图像可知,步骤②与稀盐酸反应的Fe的质量为_______。
(2)步骤①与CuSO4反应的Fe的质量为_______。
(3)步骤①与CuSO4反应的Fe的质量及步骤②与盐酸反应的Fe的质量之和______(选填“大于”、“小于”或“等于”)所取的Fe的质量8.5g。
(4)由上面实验的数据分析得出:Fe和CuSO4溶液反应,有气泡产生原因___________。
查看答案和解析>>
科目: 来源: 题型:
【题目】氧化锌(ZnO)可作为紫外线吸收剂应用于化妆品中,其一种生产工艺如下:
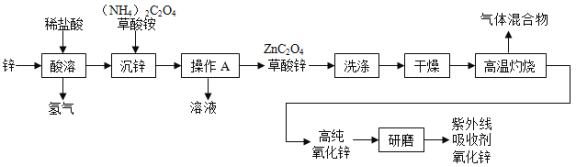
(1)推测草酸的化学式是____________;
(2)“沉锌”过程中发生复分解反应,反应的化学方程式是_______________________________
(3) “操作A”的名称是______________ 实验室常用的研磨仪器是_____________;
(4)“高温灼烧”时草酸锌分解,反应的化学方程式是______________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com