
科目: 来源: 题型:
【题目】现有两种稀溶液,标记为A的0.40%的氢氧化钠溶液和标记为B的3.65%的盐酸溶液.假设本题所涉及的各种稀溶液的密度均为1.00g/mL,且毎滴溶液的体积近似为0.05mL.在盛有40mLA溶液的锥形瓶中滴加2滴酚酞试液,再向瓶中缓缓倒入5mLB溶液,边倒边振荡,充分混合后溶液呈无色.若取该无色混合液5mL于一支试管内,再向试管内滴加40滴A溶液.求:此时试管内溶液呈现的颜色.
查看答案和解析>>
科目: 来源: 题型:
【题目】小华同学在探究金属与酸反应时,将铝片、锌片打磨后,分别投入盛有等体积、等浓度稀盐酸的试管中,观察到铝与稀盐酸反应较锌与稀盐酸反应快。
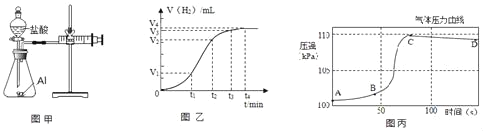
(提出问题)金属与盐酸反应快慢,除与金属的种类有关外,还受哪些因素的影响呢?
(猜想与假设)a.可能与盐酸的浓度有关;b.可能与反应时的温度有关;c.你的猜想是_____。
(设计并实验)小明利用如图甲所示装置,用不同质量分数的盐酸和相同形状的铝片进行如下实验。
实验编号 | 盐酸的浓度(均取20mL) | 温度/℃ | 记录的数据 |
① | 5% | 30 | |
② | 10% | 20 | |
③ | 5% | 20 | |
④ | 10% | 30 |
(交流讨论)(1)请写出铝与盐酸反应的化学方程式:_____。
(2)实验前小明先将分液漏斗的活塞关闭,再将注射器活塞往右拉,松手后,观察到注射器活塞回到原处。小明进行该操作的目的是_____。
(分析数据、得出结论)
(3)实验中记录的数据可能是:_____;
对比实验②③可知_____ 对金属与酸反应的速率的影响
(4)实验表明,四次实验时,反应的速率由快到慢依次为④、②、①、③.根据记录的数据分析,如果盐酸质量分数为10%,温度为25℃,则所记录数据应该介于_____两次实验所记录的数据之间。
(拓展延伸)
(5)小明进行铝与稀盐酸反应时,试管外壁发烫,并测得实验过程中生成氢气的体积随时间变化的曲线如图乙所示,根据曲线归纳铝与稀盐酸反应速率的变化规律:_____
(6)研究小组同学对铝和稀盐酸的反应进行再探究。将橡皮塞连接气体压力传感器,烧瓶中放入铝片和稀盐酸,塞紧瓶塞并打开仪器,一段时间后,得到如丙图所示的气体压强与时间的关系曲线图。
AB段气体压力变化不明显的原因是:_____。
CD段气体压力逐渐下降的原因是:_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】山西省是重要的煤化工基地,煤及其相关产品是转型发展的方向之一,以煤层气(主要成分是甲烷)、焦炭、水、空气为原料,可制得若干产品,部分生产过程如图:
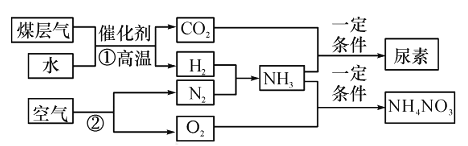
请回答下列问题:
(1)过程②是利用分离液态空气法进行分离的,该变化是_____(填“物理”或“化学”)变化.
(2)写出①所发生反应的化学方程式_____.
(3)下列说法正确的是_____.
a无机物可以转化成有机物
b氮气在工业上可用于制尿素、硝酸铵等氮肥
c生产过程使煤及其相关产品得到了综合利用
(4)尿素和NH4NO3都是氮肥,其中NH4NO3中氮元素与氧元素的质量比为_____,100gNH4NO3中氮元素的质量为_____g.
查看答案和解析>>
科目: 来源: 题型:
【题目】某固体可能由Na2SO4、NaCl、Na2CO3、KNO3中的一种或几种组成,现实验如下:
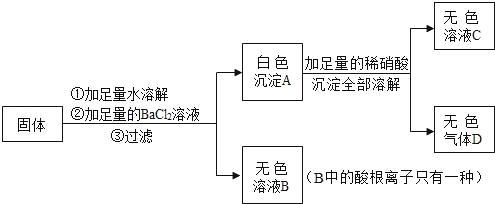
试回答:
(1)白色沉淀A的化学式为_____,无色气体D的化学式为_____
(2)原固体中一定含有_____,一定不含有_____,可能含有_____.
(3)为检验上述可能含有的物质是否一定存在,某同学又设计了如下实验方案:
①取少量固体溶于水,加入足量的Ba(NO3)2溶液,充分反应后,过滤;
②取滤液加入AgNO3溶液,观察有无白色沉淀生成,由此得出结论.在上述某同学的实验方案①中,加入足量的Ba(NO3)2溶液的目的是_____.
查看答案和解析>>
科目: 来源: 题型:
【题目】CO是一种无色、无味、有毒的可燃气体污染物,具有还原性,可用于冶金工业。某兴趣小组为探究其具有还原性,设计了如下实验装置。请回答以下有关问题:
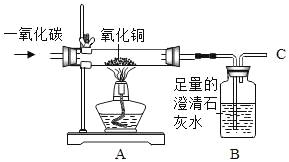
①CO气体能使人中毒,其原因是_____。
②实验开始时,先通入CO一段时间后,再加热,其原因是_____
③实验中图A处玻璃管中发生的现象是_____,其化学反应方程式为_____。
④实验中图B处发生的现象是_____其化学反应方程式为_____。
⑤该装置中有一个明显的缺陷_____,请指出改正方法_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】如图所示,甲、乙、丙、丁、戊五种物质分别是铁、盐酸、氢氧化钙、硫酸铜、碳酸钠中的一种。连线两端的物质间能发生化学反应,甲与戊反应产生的气体能使澄清石灰水变浑浊,丙溶液为蓝色。下列能替代图中丁物质的是( )
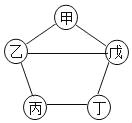
A. AgB. BaCl2C. CuOD. NaOH
查看答案和解析>>
科目: 来源: 题型:
【题目】现有25g石灰石样品,请按下面要求计算
(1)25g样品与足量的稀盐酸反应放出8.8gCO2(杂质不溶于酸,且不与酸反应),请计算该样品的纯度(CaCO3的质量分数)是多少?_____
(2)若将25g样品平均分成两份,分别加工成块状和粉末状,将两份样品分别放入锥形瓶中,同时加入相同体积,相同浓度的足量稀盐酸充分反应,请在图象上画出块状样品与稀盐酸反应放出CO2的曲线示意图。_____
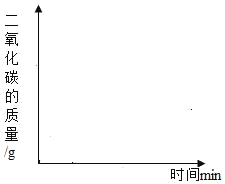
(3)若将一定质量的该石灰石样品高温煅烧,有关物质质量反应时间的变化如表所示:
时间/min | t1 | t2 | t3 | t4 | t5 |
CO2质量/g | 2.2 | 4.4 | 6.6 | 8.8 | 8.8 |
剩余固体质量/g | 22.8 | 20.6 | m | 16.2 | 16.2 |
则m=_____,t3时剩余固体中除杂质外含有的物质是_____(填化学式)
查看答案和解析>>
科目: 来源: 题型:
【题目】在科学拓展课中,甲同学向两个充满CO2气体的塑料瓶中分别加入NaOH溶液和Ca(OH)2溶液,迅速盖紧瓶盖后充分振荡,结果发现两个塑料瓶都变瘪。他认为据此实验现象,可以判定NaOH和Ca(OH)2均能与CO2发生反应。
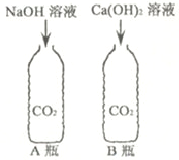
(1)乙同学认为上述判定方法还存在不严密之处,他的理由是______。
(2)丙同学根据B瓶中出现的浑浊现象,判定Ca(OH)2与CO2发生了反应,提出了可以从是否有新物质生成的角度去判断。那么,若要判定NaOH和CO2发生了反应,在排除了(1)中的干扰因素后,接下来的方法是____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】小君和小英同学发现:带火星的竹签在空气中不会复燃,若用装有60%水的集气瓶倒置在水槽中收集氧气,得到的气体能使带火星的竹签复燃,为了找到能使带火星竹签复燃的氧气含量最小值,他们进行了如下探究:
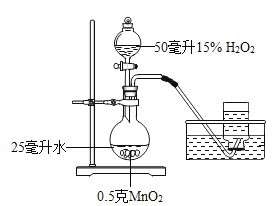
(设计实验)小君设计了如图的装置,该装置的圆底烧瓶中放入25毫升水的目的是____________。
(实验研究)第一组实验:取3只集气瓶,编号为①②③,分别装入15%30%和45%的水,盖上盖玻片倒置在水槽中。当气泡___________________放出后,导管口伸入集气瓶把其中的水全部排出,将相同的3支带火星竹签分别插入①~③号瓶中,记录实验现象。
获得第一组实验现象后,小君又做了第二组实验,并记录实验现象,两组实验数据和现象见下表:
实验分组 | 第一组 | 第二组 | ||||
实验序号 | ① | ② | ③ | ④ | ⑤ | ⑥ |
集气瓶装水的体积分数/% | 15 | 30 | 45 | 34 | 38 | 42 |
带火星竹签状况 | 亮 | 很亮 | 复燃 | 很亮 | 复燃 | 复燃 |
得出上述两组实验现象后,小英认为还不能确定能使带火星竹签复燃的氧气含量最小值,需继续进行实验。则实验序号⑦的集气瓶装水的体积分数应该是_________%。
(实验结论)再经过数次实验并计算后得出:能使带火星竹签复燃的氧气含量最小值为48.7%。
(继续探究)小君认为采用该方法收集的氧气中含有一定量的水蒸气,请你提出实验改进的措施______________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】为了测定某氧化铁样品中氧化铁的质量分数,某化学小组设计了如图所示装置进行实验。
已知:样品中的杂质不含铁元素,且不溶于水和酸;草酸(H2C2O4)在浓硫酸作用下受热分解生成CO2、CO和H2O,碱石灰主要成分为生石灰与氢氧化钠固体。请回答:

(问题讨论)
(1)进入E中的气体是纯净、干燥的CO,则B、C、D中依次是_____(填序号)。
①浓硫酸 ②氢氧化钠溶液 ③澄清石灰水
(2)B中发生反应的化学方程式为_____。
(3)C和G装置的作用分别是_____。
(数据处理)称取样品5.0g,用上述装置进行实验,充分反应后称量F装置,发现比反应前增重3.3g,则样品中氧化铁的质量分数为_____。
(实验反思)(1)该实验装置有一明显缺陷是_____。
(2)如果没有G装置,则测得的样品中氧化铁的质量分数_____(填“偏大”、“偏或“无影响”)。
(迁移应用)试计算,加热分解90t质量分数为20%的草酸溶液,能制得多少一氧化碳?_____
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com