
【题目】小华同学在探究金属与酸反应时,将铝片、锌片打磨后,分别投入盛有等体积、等浓度稀盐酸的试管中,观察到铝与稀盐酸反应较锌与稀盐酸反应快。
(提出问题)金属与盐酸反应快慢,除与金属的种类有关外,还受哪些因素的影响呢?
(猜想与假设)a.可能与盐酸的浓度有关;b.可能与反应时的温度有关;c.你的猜想是_____。
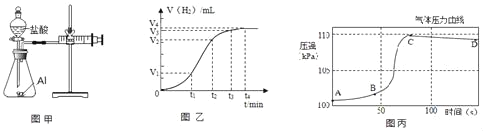
(设计并实验)小明利用如图甲所示装置,用不同质量分数的盐酸和相同形状的铝片进行如下实验。
实验编号 | 盐酸的浓度(均取20mL) | 温度/℃ | 记录的数据 |
① | 5% | 30 | |
② | 10% | 20 | |
③ | 5% | 20 | |
④ | 10% | 30 |
(交流讨论)(1)请写出铝与盐酸反应的化学方程式:_____。
(2)实验前小明先将分液漏斗的活塞关闭,再将注射器活塞往右拉,松手后,观察到注射器活塞回到原处。小明进行该操作的目的是_____。
(分析数据、得出结论)
(3)实验中记录的数据可能是:_____;
对比实验②③可知_____ 对金属与酸反应的速率的影响
(4)实验表明,四次实验时,反应的速率由快到慢依次为④、②、①、③.根据记录的数据分析,如果盐酸质量分数为10%,温度为25℃,则所记录数据应该介于_____两次实验所记录的数据之间。
(拓展延伸)
(5)小明进行铝与稀盐酸反应时,试管外壁发烫,并测得实验过程中生成氢气的体积随时间变化的曲线如图乙所示,根据曲线归纳铝与稀盐酸反应速率的变化规律:_____
(6)研究小组同学对铝和稀盐酸的反应进行再探究。将橡皮塞连接气体压力传感器,烧瓶中放入铝片和稀盐酸,塞紧瓶塞并打开仪器,一段时间后,得到如丙图所示的气体压强与时间的关系曲线图。
AB段气体压力变化不明显的原因是:_____。
CD段气体压力逐渐下降的原因是:_____。
【答案】与金属与酸的接触面积 2Al+6HCl═2AlCl3+3H2↑ 检查装置气密性 相同时间内注射器中收集到气体的体积(或注射器中收集相同体积气体所用的时间) 盐酸的浓度 实验②与实验④ 开始由慢变快,一段时间后,由快变慢 铝表面的氧化铝先与盐酸反应 到C点,反应完成,气体体积最大,并且该反应放热,所以反应结束后,随着温度降低,气体体积减小,压力逐渐下降
【解析】
[猜想与假设]金属的种类、盐酸的浓度、反应时的温度、金属与酸的接触面积对金属与盐酸反应快慢可能都会产生影响;故填:与金属与酸的接触面积(答案合理即可);
[交流讨论](1)铝与盐酸反应生成氯化铝和氢气;故填:2Al+6HCl═2AlCl3+3H2↑;
(2)实验前小明先将分液漏斗的活塞关闭,再将注射器活塞往右拉,松手后,观察到注射器活塞回到原处。小明进行该操作的目的是检查装置气密性;故填:检查装置气密性;
(3)该实验是比较化学反应速率,所以记录的数据是相同时间内注射器中收集到气体的体积或注射器中收集相同体积气体所用的时间;故填:相同时间内注射器中收集到气体的体积(或注射器中收集相同体积气体所用的时间);
实验②③反应温度相同、铝片的形状相同,只有酸的浓度不同,所以是探究盐酸的浓度对金属与酸反应的速率的影响;故填:盐酸的浓度;
(4)盐酸质量分数为10%,温度为25℃,则所记录数据应该介于实验②与实验④之间,故填:实验②与实验④;
(5)根据坐标中的曲线变化可以看出,反应开始由慢变快,一段时间后,由快变慢,这是因为锌与稀盐酸反应放出热量使温度升高,开始时温度升高对反应速率的影响较盐酸浓度变小对反应速率影响更大,一段时间后,盐酸浓度减小对反应速率的影响较温度升高对反应速率的影响更大,故填:开始由慢变快,一段时间后,由快变慢;
(6)铝在空气表面会生成致密的氧化铝薄膜,氧化铝会先与盐酸反应,随着时间的推移,盐酸的浓度会逐渐降低,所以AB段气体压力变化不明显的原因是:铝表面的氧化铝先与盐酸反应;CD段气体压力逐渐下降的原因是:到C点,反应完成,气体体积最大,并且该反应放热,所以反应结束后,随着温度降低,气体体积减小,压力逐渐下降;故填:铝表面的氧化铝先与盐酸反应;到C点,反应完成,气体体积最大,并且该反应放热,所以反应结束后,随着温度降低,气体体积减小,压力逐渐下降。


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:
【题目】小华将一张滤纸在某示剂中浸泡后晾干,用蘸有氢氧化钠溶液的玻璃棒在上面写“化学”两字,立刻显红色。再将其悬挂于铁架台上,并在滤纸的下方(如图)放置一个盛有某溶液的烧杯,过一会儿,发现红色的字消失,则滤纸上的指示剂和烧杯中的溶液分别是( )
A | B | C | D | |
滤纸上的指示剂 | 酚酞溶液 | 酚酞溶液 | 石蕊溶液 | 石蕊溶液 |
烧杯中的溶液 | 浓氨水 | 浓盐酸 | 浓氨水 | 浓盐酸 |
A. A
B. B
C. C
D. D
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在2018全国两会上,农业部部长韩长赋在人民大会堂“部长通道”回答记者提问时说,农药和化肥确实对粮食增产发挥了重要作用,“十三五”开始,我国大力开展农药减量,效果明显。2016年,全国农药使用量负增长。
谈到农药,人们可能想到农药对人体健康和环境的危害,其实农药在农业生产上起着重要的作用。目前市售蔬菜农药残留量虽然已达到国家标准,但通过科学的清洗方法仍可进一步降低农药残留。
实验人员分别选取含甲、乙农药的蔬菜,研究了不同的清洗方法对农药的去除率的影响。
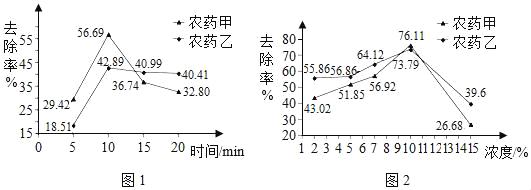
清水浸泡。图1呈现出两种农药的去除率随浸泡时间的变化。
洗洁精清洗。实验选择了6种洗洁精进行测试,结果表明多数洗洁精对农药的去除率可达到60%以上,最高可达到84%。
碱性溶液。浸泡食用碱溶液有利于农药分解,图2表示不同浓度的食用碱溶液对农药的去除率的影响。
希望同学们可以选择科学的清洗方法,更加安全的食用蔬菜。
依据文章内容,结合所学化学知识,回答下列问题。
(1)农药和化肥对粮食增产发挥了重要作用,请你写出一种氮肥:_____(合理即可)。
(2)依据图1分析去除农药残留的最佳浸泡时间是_____。
(3)食用碱主要是碳酸钠和碳酸氢钠,它们的溶液的pH_____7(填“>”或“<”)。测定溶液pH的正确方法是_____。
(4)用食用碱溶液浸泡含有农药甲的蔬菜时,要想超过清水浸泡的最大去除率,可以选取的浓度是_____(填序号,下同)。
A 2% B 5% C 10% D 15%
(5)下列说法正确的是_____。
A 采用清水浸泡去除农药的时间不宜过长
B 多数洗洁精对农药的清洗效果比清水浸泡的好
C 食用碱的去除效果较好,是因为在浸泡过程中农药发生了化学变化
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列实验操作能达到预期目的是( )
①用20mL水和20mL酒精配制成40mL酒精溶液;
②用量筒量取5.62mL的水;
③用托盘天平称量5.6gNaCl固体;
④用托盘天平、烧杯、量筒、玻璃捧配制一定温度下30%的NaCl的溶液.
A. ③B. ③④C. ②③D. ①④
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】现有25g石灰石样品,请按下面要求计算
(1)25g样品与足量的稀盐酸反应放出8.8gCO2(杂质不溶于酸,且不与酸反应),请计算该样品的纯度(CaCO3的质量分数)是多少?_____
(2)若将25g样品平均分成两份,分别加工成块状和粉末状,将两份样品分别放入锥形瓶中,同时加入相同体积,相同浓度的足量稀盐酸充分反应,请在图象上画出块状样品与稀盐酸反应放出CO2的曲线示意图。_____
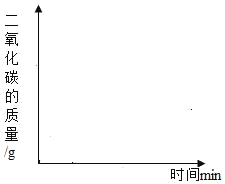
(3)若将一定质量的该石灰石样品高温煅烧,有关物质质量反应时间的变化如表所示:
时间/min | t1 | t2 | t3 | t4 | t5 |
CO2质量/g | 2.2 | 4.4 | 6.6 | 8.8 | 8.8 |
剩余固体质量/g | 22.8 | 20.6 | m | 16.2 | 16.2 |
则m=_____,t3时剩余固体中除杂质外含有的物质是_____(填化学式)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(1)用适当的数字和符号填空:①氧化镁中镁元素显+2价___________;②1个亚铁离子___________; ③氦气_________; ④形成化合物种类最多的元素________;
(2)现有六种物质,选择相应物质的字母填空:A金刚石 B汽油 C小苏打 D熟石灰 E蛋白质 F锰钢
①____可用于治疗胃酸过多症 ②____可用于制造钢轨
③____是构成细胞的基本物质 ④____可用来切割大理石
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在已平衡的天平两边分别放一个等质量的烧杯,烧杯中装有等质量、等质量分数的足量稀盐酸,在左边烧杯中加入5.6g金属铁,在右边烧杯中加入5.5g镁和铜的混合物,充分反应后天平仍然保持平衡,则右边烧杯中加入的混合物中镁和铜的质量比为( )
A. 36:19 B. 12:43 C. 24:31 D. 13:42
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学小组利用如图所示装置(图中固定装置已略去)测定铜锌合金中锌的质量分数,探究过程如下:
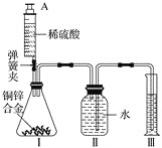
①连接实验装置并检查装置气密性。
②向装置Ⅰ中的锥形瓶加入2.0g的铜锌合金样品粉末,由注射器缓缓注入稀硫酸,待到锥形瓶中不再产生气体时,准确读取注射器内读数,减少10.5mL稀硫酸,同时立即夹紧弹簧夹,移出装置Ⅲ中的导管,准确读取量筒内水的体积为214.0mL(注:样品中的杂质不参加反应
③装置Ⅰ中剩余固体物质经过适当处理后,准确称量其质量为1.4g
④该小组的三位同学利用实验过程测得不同数据,计算铜锌合金样品中锌的质量分数
甲同学利用装置Ⅰ中反应前后固体的质量进行计算;
乙同学利用装置Ⅰ中加入稀硫酸的量进行计算;
丙同学利用装置Ⅲ中量取水的体积进行计算,并查得:在标准状况下,氢气的密度为0.09gL-1。
回答下列问题:
(1)装置Ⅰ中反应的化学方程式为___,实验过程中须加入稀硫酸至不再产生气体,目的是___。
(2)步骤③中称量剩余固体之前的正确操作是_______、洗涤、干燥。
(3)根据实验测定的数据,上述三位同学中________(填“甲”、“乙”或“丙”)同学无法进行计算样品中锌的质量分数。
(4)化学小组同学发现:按照丙同学的方案进行计算,致使实验结果出现较大偏差。以下因素可能造成偏差的有________(填标号)。
A 移出装置Ⅲ时,导管内留存了一部分水
B 实验测量前,没有排除装置Ⅰ中的空气
C 数据处理时,未排除加入稀硫酸所占的体积
【答案】(1)![]() ;使样品中的锌完全反应;(2)过滤;(3)乙;(4)AC;
;使样品中的锌完全反应;(2)过滤;(3)乙;(4)AC;
【解析】
试题(1)由于铜排在了氢的后面,所以与酸不反应,反应物是锌和硫酸,生成物是硫酸锌和氢气,氢气后面标上上升符号;实验过程中须加入稀硫酸至不再产生气体,目的是使样品中的锌完全反应;(2)从铜和硫酸锌溶液的混合物中得到铜,先进行过滤,得到带有硫酸锌溶液的铜,再进行洗涤除去表面的硫酸锌,再进行干燥除去水即可;(3)根据加入稀硫酸的量进行计算需要知道稀硫酸的溶质质量分数,而题中没有告知;(4)由于锌与硫酸反应生成硫酸锌和氢气时,放出热量,如果没等冷却到室温,根据热涨冷缩的原理可知进入量筒中水偏多,所以误认为得到的氢气多,再就是数据处理时,未排除加入稀硫酸所占的体积,计算的结果就偏大;
考点:金属的化学性质;化学方程式;实验误差分析;
点评:熟记金属活动性顺序表,知道排在氢之前的金属和稀盐酸或者硫酸反应生成氢气,而排中氢之后的金属和稀盐酸或者稀硫酸不生成氢气;化学反应中物质的质量比都是纯净物之间的质量比,而溶液中溶质的质量=溶液质量×溶质质量分数;本题容易出错的地方是对实验结果的评价,要知道锌与硫酸反应放出热量,会造成相应的误差,必须冷却到室温才能进行观察和计算。
【题型】实验题
【结束】
30
【题目】用1000t含氧化铁80%的赤铁矿石,理论上可以炼出含铁96%的生铁的质量是多少?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com