
科目: 来源: 题型:
【题目】下列图像不能正确反映其对应关系的是

A.加热一定质量的高锰酸钾
B.向含有HCl和CaCl2的混合溶液中加入Na2CO3溶液
C.向等质量等质量分数的稀盐酸中分别加入过量的锌和铁
D.将一瓶浓硫酸敞口放置在空气中
查看答案和解析>>
科目: 来源: 题型:
【题目】以硫铁矿烧渣(主要成分为Fe2O3、FeO、SiO2)为原料,制备高纯氧化铁(Fe2O3)的生产流程示意图如下,回答下列问题:
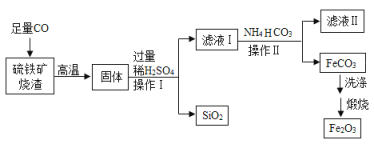
(1)操作Ⅰ、操作Ⅱ的名称是_____。
(2)写出高温时CO与硫铁矿烧渣反应生成Fe的其中一个化学方程式_____。
(3)滤液I的溶质是_____。
(4)高温煅烧时,FeCO3与空气中的氧气反应生成两种氧化物,写出该反应的化学方程式:_____,5.8tFeCO3在空气中煅烧,理论上可得到_____tFe2O3。
查看答案和解析>>
科目: 来源: 题型:
【题目】某活动小组探究某种塑料袋中碳元素的质量分数,装置如下图所示:
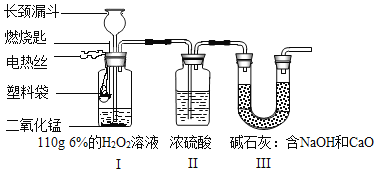
已知:①H2O2溶液分解放出的氧气在逸出时会带出少量水蒸气。
②碱石灰的作用是吸收CO2。
③忽略空气对本实验的影响。
实验步骤如下:
(1)检查装置气密性。
(2)称量塑料袋的质量是w克。
(3)用30%的H2O2溶液(密度为1.1g/mL)配制110g6%的H2O2溶液。
①需要30%的H2O2溶液_____g。
②配制时除了要使用200mL烧杯、100mL量筒和20mL量筒外,还需要的玻璃仪器有_____。
(4)进行实验和收集数据。
按图所示连接好实验装置,从装置I中的长颈漏斗中加入110g6%的H2O2溶液,通过电热丝点燃塑料袋。待塑料袋燃烧完,冷却后,装置Ⅲ实验后的质量比实验前增加了a克。则塑料中碳元素的质量分数是_____。(用含a和w的式子表示)
(5)实验分析。
①装置Ⅱ的作用是_____;
②实验中H2O2溶液需过量,其作用除了能防止装置Ⅱ中的液体倒吸外,还有_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】下图是实验室制取气体的装置,请回答下列问题。
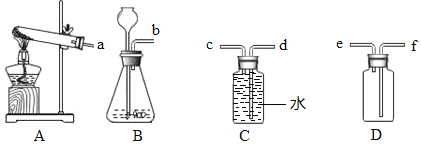
(1)根据实验室制备气体的方法,选择恰当的发生装置(填大写字母编号)并写出反应方程式。
制取的气体 | 选用药品 | 发生装置 | 反应方程式 |
O2 | 高锰酸钾 | _____ | _____ |
CO2 | 大理石和稀盐酸 | B | _____ |
H2 | 锌粒和稀硫酸 | _____ | Zn+H2SO4=ZnSO4+H2↑ |
(2)用过氧化氢溶液制备并收集一瓶较纯净的O2,装置的连接顺序是b→_____。(填小写字母编号)
(3)用D装置收集CO2时验满的方法是_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】如图是四种物质的溶解度曲线图,请回答下列问题。
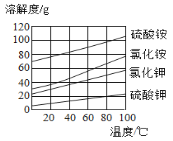
(1)在60℃时,四种物质中溶解度最大的是_____。
(2)80℃时,分别向都盛有100g水的四个烧杯中加入20g四种固体,充分溶解后能得到饱和溶液的是_____,a克该饱和溶液中溶质的质量是_____克(用含a的式子表示)。
(3)20℃将饱和硫酸铵溶液跟饱和氯化钾溶液混合,会析出硫酸钾晶体,写出该反应的化学方程式_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】含硫化合物在生产、生活中有着重要的用途。常见的含硫化合物有Na2S、H2S、SO2、SO3、H2SO4、Na2SO3、Na2SO4、NaHSO4等。
(1)Na2S读作_____。
(2)NaHSO4中S的化合价是_____。
(3)2H2S+SO2=3S↓+2X,则X的化学式是_____。
(4)①NaHSO4溶液、Na2SO4溶液都能与BaCl2溶液反应,是因为NaHSO4溶液和Na2SO4溶液中都含有_____。(填离子符号)

②往NaHSO4溶液中滴加NaOH溶液至恰好完全反应。如图表示该反应前后溶液中存在的主要离子,写出下列图形代表的离子(填离子符号):
![]() _____
_____![]() _____。
_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】丙氨酸的化学式为C3H7O2N。下列说法正确的是
A. 丙氨酸的相对分子质量为89 g
B. 丙氨酸中C、H、O、N四种元素的质量比是3:7:2:1
C. 丙氨酸中C、H、O、N四种元素的原子个数比是36:7:32:14
D. 丙氨酸中氮元素的质量分数是![]() ×100%
×100%
查看答案和解析>>
科目: 来源: 题型:
【题目】充分燃烧1kg天然气和煤所产生CO2和SO2的质量如下图所示。下列说法不正确的是
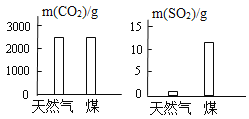
A. 燃烧煤比燃烧天然气更容易导致酸雨
B. 用天然气替代煤作燃料,有利于改善空气质量
C. 等质量的天然气和煤,充分燃烧产生CO2的质量接近
D. 天然气、煤都是重要的化石燃料,属于可再生能源
查看答案和解析>>
科目: 来源: 题型:
【题目】某化学兴趣小组的同学学习“灭火器原理”后,设计了如图所示实验,并对反应后瓶中残留废液进行探究。
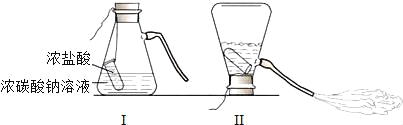
(提出间题)废液中所含溶质是什么?
(查阅资料)1.碳酸钠溶液呈碱性;
2.反应原理:Na2CO3+2HCl=2NaCl+H2O+CO2↑
(猜想与假设)
猜想1:废液中的溶质是NaC1、Na2CO3和HCl
猜想2:废液中的溶质只有NaC1
猜想3:废液中的溶质是NaCl、HCl
猜想4:废液中的溶质是NaC1、Na2CO3
(讨论与交流)
小明同学认为其中有一个猜想无需验证就知道是错误的,这个猜想是_____。
(实验与结论)
(1)小亮同学为验证猜想3,取少量反应后的废液装入试管中,然后滴入酚酞溶液,发现溶液不变色,于是小亮得出猜想3是正确的结论。你认为他的结论_____(填“正确”或“错误”),理由是_____。
(2)验证猜想4,可选择的试剂有_____。
A 酚酞溶液 B 氢氧化钾溶液 C 稀硫酸 D 氯化钡溶液
(拓屐与应用)若废液中的溶质是NaCl和HCl,根据盐酸的性质,无需另加试剂,只要对废液进行_____操作,即可从废液中得到NaCl固体。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com