
科目: 来源: 题型:
【题目】根据实验装置图,回答下列问题:

(1)用过氧化氢溶液和二氧化锰混合制取氧气应选用的发生装置是___;反应方程式为____
(2)实验室制取CO2和收集二氧化碳气体应选择的装置是___;
(3)如装置F所示,点燃两支短蜡烛,然后沿烧杯内壁倾倒二氧化碳时,看到F中的实验现象是__________;
(4)某同学选用G装置进行实验,看到与上一步实验F的实验现象___(填“相同”或“不同”);
查看答案和解析>>
科目: 来源: 题型:
【题目】如图是甲、乙两种物质的溶解度曲线,请回答:
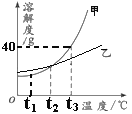
(1)t3℃时,两种物质溶解度的大小关系为甲__乙;(填“大于”、“小于”或“等于”)
(2)t3℃时,把30g固体甲放入50g水中,充分溶解后可得到甲的溶液_____g;
(3)在其他条件不变的情况下,若把t1℃时甲、乙的饱和溶液分别升温至t2℃,此时两种溶液中溶质的质量分数关系为甲__乙(选填:>、<或=)。
查看答案和解析>>
科目: 来源: 题型:
【题目】人们生产、生活中处处有化学。
(1)活性炭具有疏松多孔的结构,具有极强的_______性,可以用于除去有害气体。
(2)为了保证饮水安全,测定水样的pH略小于7,该水样显____性
(3)每到春节,都会看到有人燃放鞭炮,燃放烟花、鞭炮会产生SO2、CO、CO2气体、烟尘等,其中严重时会造成大气污染,能使大气PM2.5升高的物质是_______。
(4)能与血液中血红蛋白结合的有毒气体是___。
(5)叠氮化钠(NaN3)被广泛应用于汽车安全气囊,汽车经撞击后30毫秒内引发叠氮化钠迅速分解为两种单质,该反应的化学方程式是__。
查看答案和解析>>
科目: 来源: 题型:
【题目】将相同体积、相同溶质质量分数的稀盐酸,分别滴到等质量、颗粒大小相同的X、Y、Z三种较活泼金属中,生成H2的质量与反应时间的关系如右图所示。下列说法中正确的是
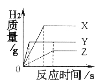
A.三种金属的活动性顺序为X>Z>Y
B.产生氢气的速率顺序为 X>Y>Z
C.反应完成时消耗稀盐酸的质量顺序为X>Y>Z
D.相对原子质量由大到小的顺序为 X>Y>Z
查看答案和解析>>
科目: 来源: 题型:
【题目】某氢氧化钙样品中含碳酸钙杂质,现称取研细的该样品12.4g放入锥形瓶中,加入32.6g的水,充分振荡形成悬浊液,再向锥形瓶中逐滴滴加盐酸使其充分反应至无气泡产生。测得加入盐酸的质量与锥形瓶中的物质的质量关系如下表示:
加入盐酸的质量g | 0 | 25 | 37.5 |
锥形瓶中物质的质量g | 45 | 70 | 80.3 |
请你完成以下问题:
(1)加入盐酸的质量在0—25g时,______与盐酸发生反应;
(2)求样品中氢氧化钙的质量分数(写出计算过程,精确到0.1%)。______。
查看答案和解析>>
科目: 来源: 题型:
【题目】碲(Te)被誉为“现代工业、国防与尖端技术的维生素,创造人间奇迹的桥梁”。实验室模拟提取碲的一个实验是:取某含碲溶液于烧瓶中,加入适量NaCl,加热到一定温度,持续通入SO2,待反应一段时间,过滤得到粗碲。
(1)反应的总化学方程式为: ![]() ,则X为______(填化学式);
,则X为______(填化学式);
(2)为探究获得较高粗碲沉淀率的反应条件,某研究小组在控制NaCl浓度和SO2流量不变的条件下,进行下述对比试验,数据如下:
实验 | 温度/℃ | 反应时间/h | 粗碲沉淀率/% |
a | 65 | 3.0 | 65.0 |
b | 80 | 3.0 | 98.9 |
c | 80 | 2.0 | 98.9 |
d | 90 | 2.0 | 97.0 |
①该小组研究的反应条件是______和______;
②实验a和b 的目的是______;
③为了提升设备利用效率和节约能源,可进一步优化反应条件测定粗碲沉淀率。若再设计对比实验,选择的反应条件还可以是______(填序号)。
A 80℃,1.5h B 80℃,2.5h C 70℃,2.0h D 95℃, 2.0h
查看答案和解析>>
科目: 来源: 题型:
【题目】金属钛密度小、硬度大、抗腐蚀性能好,被誉为“未来的金属”,某工厂用钛酸亚铁(FeTiO3)、焦炭为原料制取金属钛,请据图回答下列问题:
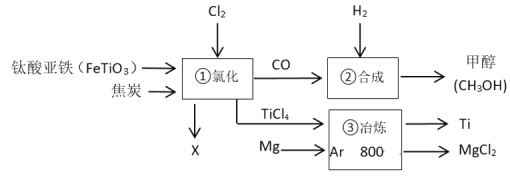
(1)反应前将钛酸亚铁和焦炭磨成粉末状的目的是_____,钛酸亚铁(FeTiO3)中钛元素为____价;
(2)步骤②中为使原料全部转化为甲醇,理论上CO和H2投料的最简质量比为____;
(3)写出步骤③中,在高温时生成金属钛的化学反应方程式_____,该反应的基本类型为___;
(4)工业上用电解熔融的TiO2来制取金属Ti,从能量的角度分析,工业利用该方法制备金属Ti的缺点是__________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】实验是研究化学的重要方法,请根据下图装置图回答问题。
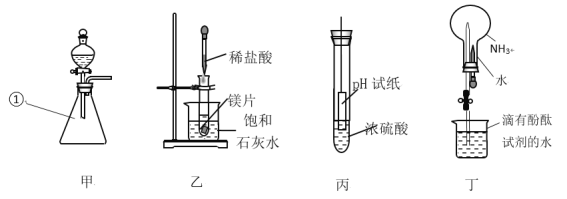
(1)标号仪器①的名称是______;写出用甲装置制氧气的反应方程式______;
(2)将乙装置中的稀盐酸滴入试管后较长一段时间内,看到的实验现象是______;根据实验现象你能获得哪些知识______;
(3)将丙装置中的PH试纸浸入浓硫酸中,试纸变黑,说明浓硫酸有______性;
(4)将丁装置中胶头滴管内的水挤入烧瓶中,并打开玻璃管上的弹簧夹,看到的实验现象是______。
查看答案和解析>>
科目: 来源: 题型:
【题目】食品与健康、能源与环境是我们共同关注的社会问题。
(1)紫薯营养丰富,具有特殊的保健功能。紫薯中富含淀粉、维生素C、维生素B、铁、钙、硒等。
①这里的“铁”“钙”是指 ______;
②人体缺“铁”,会导致______病症;
③紫薯中能给人体提供能量的物质是______;
④硒元素被誉为“抗癌大王”。硒元素的部分信息如下图。下列说法正确的是______(填序号)。
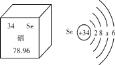
A 硒属于金属元素 B 一个硒原子中有34个质子
C 硒的原子结构示意图中x=18 D 硒元素的相对原子质量为78.96g
(2)①合理使用化肥是农业增产的重要手段,下列属于复合肥的是(填序号)______;
A 尿素[CO(NH2)2] B 硫酸钾[K2SO4]
C 磷酸二氢铵[NH4H2PO4] D 硝酸钾[KNO3]
②配制农药波尔多液时不宜用铁制容器,用化学方程式表示原因_______。
查看答案和解析>>
科目: 来源: 题型:
【题目】阅读下列科普材料,回答相关问题。
说起二氧化硫(SO2),你可能首先想到它是空气质量播报中提及的大气污染物。其实你真的了解SO2吗?难道它只是有害物质吗?
SO2与食品工业
SO2作为防腐剂、漂白剂和抗氧化剂广泛用于食品行业。葡萄酒酿制中适量添加SO2,可防止葡萄酒在陈酿和贮藏过程中被氧化,抑制葡萄汁中微生物的活动。食糖加工过程中可使用SO2进行脱色。按照我国《食品添加剂使用标准(GB2760-2014)》,合理使用SO2不会对人体健康造成危害。
标准中部分食品的SO2最大残留量
食品 | 蜜饯 | 葡萄酒 | 食糖 | 水果干 | 巧克力 | 果蔬汁 |
最大残留量 | 0.35 g/kg | 0.25 g/L | 0.1 g/kg | 0.1 g/kg | 0.1 g/kg | 0.05 g/kg |
SO2与硫酸工业
硫酸是重要的化工原料,工业制硫酸的关键步骤是SO2的获取和转化。工业利用硫制硫酸的主要过程示意如下:
![]()
硫酸工业尾气中含有少量的SO2,若直接排放会污染空气,并导致硫酸型酸雨。工业上可先用氨水吸收,再用硫酸处理,将重新生成的SO2循环利用。
SO2与化石燃料
化石燃料中的煤通常含有硫元素,直接燃烧会产生SO2。为了减少煤燃烧产生的SO2污染空气,可以采取“提高燃煤质量、改进燃烧技术”的措施,例如,对燃煤进行脱硫、固硫处理;还可以采取“优化能源结构、减少燃煤使用”的措施,例如,北京大力推广的“煤改气、煤改电”工程,有效改善了空气质量。
现在,你对SO2一定有了新的认识,在今后的化学学习中你对SO2还会有更全面的认识!
依据文章内容回答下列问题。
(1)按照国家标准,食糖中的SO2最大残留量为______ g/kg;
(2)用硫制硫酸的主要过程中,涉及到的含硫物质有S、______和H2SO4;
(3)硫酸工业生产中,吸收尾气中SO2的物质是______;
(4)下列措施能减少SO2排放的是______(填序号);
A 将煤块粉碎 B 对燃煤进行脱硫
C 推广煤改气、煤改电 D 循环利用工业尾气中的SO2
(5)在煤燃烧前需对煤进行脱硫处理。煤的某种脱硫技术的原理如下所示:![]() ,这种脱硫技术称为微生物脱硫技术。写出该技术中的第二步化学反应方程式:______。
,这种脱硫技术称为微生物脱硫技术。写出该技术中的第二步化学反应方程式:______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com