
科目: 来源: 题型:
【题目】下列有关酸和碱的说法不正确的是( )
A.用酚酞溶液检验溶液是否显酸性
B.浓氢氧化钠溶液不慎沾到皮肤上,立即用大量的水冲洗,然后再涂上硼酸溶液
C.![]() 溶液和澄清石灰水都能使酚酞溶液变红,其原因是二者的溶液中均含有
溶液和澄清石灰水都能使酚酞溶液变红,其原因是二者的溶液中均含有![]()
D.向久置空气中的澄清石灰水中滴入足量稀盐酸,产生气泡
查看答案和解析>>
科目: 来源: 题型:
【题目】(5分)在用稀盐酸和氢氧化钠溶液进行中和反应实验时,反应过程中溶液的酸碱度变化如图所示。
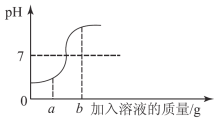
(1)该反应的化学方程式为 。
(2)该实验操作是将 滴加到另一种溶液中。
(3)当加入溶液的质量为a g时,所得溶液中的溶质为 (写化学式)。
(4)当加入溶液的质量为b g时,向所得溶液中滴加酚酞溶液,溶液呈 色。
查看答案和解析>>
科目: 来源: 题型:
【题目】推理是化学学习中常用的思维方法,下列推理正确的是( )
A.酸性溶液的pH小于7,食醋是酸性溶液,所以食醋的pH小于7
B.溶液中有晶体析出时,溶质质量减小,所以溶质的质量分数一定减小
C.酸能使紫色石蕊溶液变红,通入![]() 后的紫色石蕊溶液变红,所以
后的紫色石蕊溶液变红,所以![]() 是酸
是酸
D.酸碱中和反应生成盐和水,所以生成盐和水反应一定是中和反应
查看答案和解析>>
科目: 来源: 题型:
【题目】甲、乙两种物质的溶解度曲线如图所示,下列说法正确的是( )
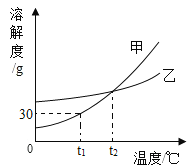
A.甲的溶解度比乙的大
B.t2℃时,甲、乙两种物质的溶解度相等
C.t1℃时,将50g水与20g甲混合,可以得到70g溶液
D.将t2℃时甲物质的饱和溶液降温到t1℃,溶液中溶质的质量分数没有变化
查看答案和解析>>
科目: 来源: 题型:
【题目】一些食物的近似pH如下:
食物 | 葡萄汁 | 苹果汁 | 牛奶 | 鸡蛋清 |
pH | 3.5~4.5 | 2.9~3.3 | 6.3-6.6 | 7.6~8.0 |
下列说法正确的是
A. 鸡蛋清和牛奶显碱性 B. 要补充维生索可以多吃鸡蛋清
C. 苹果汁的酸性比葡萄汁弱 D. 胃酸过多的人应少饮葡萄汁和苹果汁
查看答案和解析>>
科目: 来源: 题型:
【题目】某校化学小组对热水壶底部水垢的主要成分进行了如下探究,请完成以下活动并回答相关问题。
(查阅资料)天然水中含有Ca2+、Mg2+、HCO3-等离子,在加热条件下,这些离子趋于生成溶解度更小的物质—水垢(主要成分为碳酸盐和碱。有关物质的溶解性见下表:
阴离子 阳离子 | OH- | CO32- | HCO3- |
Ca2+ | 微溶 | 不溶 | 可溶 |
Mg2+ | 不溶 | 微溶 | 可溶 |
(提出猜想)水垢的主要成分一定有CaCO3和_____(填化学式),可能含有Ca(OH)2和______。
(提出问题)水垢的主要成分中是否含有Ca(OH)2和MgCO3呢?
(设计方案1)确定水垢中是否含Ca(OH)2
实验步骤 | 实验现象 | 结论 |
在少量研碎的水垢中,加入适量的蒸馏水充分搅拌,过滤,在滤液里加入Na2CO3溶液。 | ______________ | 一定不含Ca(OH)2 |
(实验方案2)确定水垢中是否含MgCO3
利用下列实验装置,完成实验2探究。其主要实验步骤如下:

其主要实验步骤如下:称量D、E装置总质量为200.0g,按上图组装后,将2.5g水垢试样放入锥形瓶中,加入足量稀盐酸溶液,待锥形瓶中不再产生气泡时,打开止水夹K,从导管a处缓缓鼓入空气,一段时间后称量装置D、E的总质量为201.25g(碱石灰主要成分为CaO和NaOH,不考虑稀盐酸的挥发性以及装置内空气、外界空气对实验的影响)。
(实验讨论)
(1)反应结束后打开止水夹K,缓缓鼓入空气的目的是_____A、B装置之间_____设置干燥装置。(填“要”或“不要”)其理由是______
(2)装置B盛放稀盐酸的仪器作用是:______
(3)装置 B中生成气体的反应的化学方程式为______
(4)装置B中生成气体的质量为______g通过计算说明该水垢中____(填序号)含MgCO3。
A 一定 B 一定不 C 可能 D 无法确定
已知CaCO3相对分子质量为100.Mg CO3相对分子质量为84):
(实验方案3)确定水垢中是否含有Mg(OH)2
(5)另取质量为1.2g的水垢试样,加入3.65%稀盐酸与之恰好完全反应,测得消耗稀盐酸mg。合上述实验,判断当m的值满足_____条件时,水垢中一定含有Mg(OH)2
查看答案和解析>>
科目: 来源: 题型:
【题目】精还原铁粉是一种重要的化工原料,某兴趣小组对其进行下列研究:
(物质制备)利用绿矾制备精还原铁粉的工艺流程如下:

粗还原铁粉中还含有少量铁的氧化物和Fe3C杂质,可用氢气在高温下进一步还原,其反应方程式:
FexOy+yH2![]() xFe+yH2O,Fe3C+2H2
xFe+yH2O,Fe3C+2H2![]() 3Fe+CH4
3Fe+CH4
(1)写出焙烧中氧化铁与CO反应的化学方程式____________.
(2)焙烧中加入焦炭的作用:______、_________。
(含量测定)为得到精还原铁粉并测定粗还原铁粉中氧和碳元素的质量分数,按如下装置进行实验。已知 3CH4+4Fe2O3![]() 3CO2+6H2O+8Fe (假设每步反应都完全且不考虑装置内原来有空气对测定结果的影响).
3CO2+6H2O+8Fe (假设每步反应都完全且不考虑装置内原来有空气对测定结果的影响).
(3)主要实验步骤如下:

①按顺序组装仪器,检查装置的气密性,称量样品和必要装置的质量;②点燃A处酒精灯;③缓缓通入纯净干燥的H2;④点燃C处酒精灯;⑤分别熄灯A、C处酒精灯;⑥再缓缓通入少量H2;⑦再次称量必要装置的质量.
操作的先后顺序是①→ _____ →______ →______→_______ → _______ →⑦(填字母);
步骤②和③能否交换?_____(填“能”或“不能”)原因是______
(4)步骤⑤和⑥能否交换?_______(填“能”或“不能”)原因是_______
(5)装置F的作用是____________,若缺少装置F,则所测氧元素质量分数将______ (选填“偏大”、“偏小”或“不变”下同),碳元素的质量分数将 _______
(6)粗还原铁粉样品的质量为5.0g,装置B,E分别增重0.54g和0.44g.则样品中氧元素质量分数为____和碳元素的质量分数为________(要求计算过程).
查看答案和解析>>
科目: 来源: 题型:
【题目】化工厂用废硫酸制备K2SO4的流程如下:
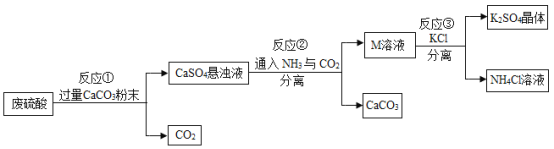
(1)生产上将CaCO3研成粉末的目的是_______欲达此目的,还可采用的方法是__________ (任写一条)
(2)上述流程中,还可循环使用的物质是___(填写化学式).
(3)写出反应①中主要的化学方程式_______
(4)反应③中相关物质的溶解度如下表所示,反应③在常温下可实现的原因是______
物质 | KCl | K2SO4 | NH4Cl | (NH4)2SO4 |
溶解度/g(20℃) | 34.2 | 11.1 | 37.2 | 75.4 |
(5)洗涤反应③所得晶体最适宜的试剂是___________ (填序号)
A H2O B 饱和K2SO4溶液 C 二者均可
(6)检验K2SO4晶体是否洗涤干净的方法是 ____________
查看答案和解析>>
科目: 来源: 题型:
【题目】某水溶液中含有以下离子中的若干种:K+、Cl-、Ca2+、H+、CO32-、SO42-,现取两份溶液中各100ml,分别进行如下实验:
(1)第一份加入AgNO3溶液有沉淀生成
(2)第二份加足量BaCl2溶液后,得沉淀物6.63g,经足量硝酸洗涤、干燥后,沉淀质量为4.66g;在所得滤液中加入AgNO3溶液有溶液生成。根据上述实验,回答下列问题。
(1)写出第(2)步中生成沉淀的反应方程式:__________。
(2)根据第(1)(2)步实验操作判断原溶液中_______(填“肯定有”或“肯定无”、“可能有”) CO32-和SO42-;
(3)原溶液中CO32-和SO42-的个数比为________
(4)原溶液中肯定没有的离子:__________。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知:![]() ,在密闭容器中,将11gCO2与一定量的
,在密闭容器中,将11gCO2与一定量的![]() 固体充分反应,气体变为5.4g,则下列说法正确的是( )
固体充分反应,气体变为5.4g,则下列说法正确的是( )
A.该5.4g气体全部是O2
B.该反应后的固体为![]() 和
和![]() 的混合物
的混合物
C.将该5.4g气体通入足量NaOH溶液中,气体质量减少2.2g
D.生成![]() 质量10.6g
质量10.6g
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com