
科目: 来源: 题型:
【题目】人类的日常生活和工农也生产都离不开水
(1)沾有较多油污的碗碟很难用水清洗干净,可向水中加入洗涤剂进行清洗,是因为洗涤剂具有_______作用;可供我们使用的淡水资源有限,我们必须要节约用水,爱护水资源。
(2)电解水的实验中,负极产生的气体是___________;配制一定溶质质量分数的氯化钠溶液,配制步骤为计算、称量、量取、___________、装瓶贴标签。
(3)自来水消毒过程中常会发生如下化学反应,其反应的微观过程可用下图表示:
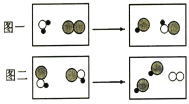
(○表示氧原子,●表示氢原子,![]() 表示氯原子)
表示氯原子)
①写出图一中反应的化学方程式___________。
②该反应中化合价升高的元素是________(填元素符号)
③在该反应中,________(填化学式)发生了还原反应。
查看答案和解析>>
科目: 来源: 题型:
【题目】人体摄入维生素C不足会引起坏血病,缺乏者可在医生指导下通过服用维生素C片来补充.已知维生素C的化学式为C6H8O6,请回答:
(1)维生素C中碳、氢、氧三种元素的质量比是 _________ ;
(2)维生素C的相对分子质量是 _________ ;
(3)维生素C中碳元素的质量分数是 _________ (精确到1%)
查看答案和解析>>
科目: 来源: 题型:
【题目】初中化学教材中的一些实验如图,请你回答下列问题:
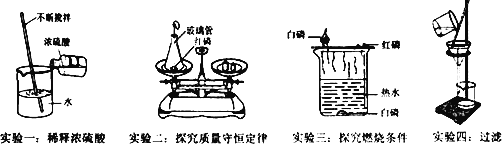
(1)实验一玻璃棒不断搅拌的目的是 _________ ;
(2)实验二锥形瓶内产生的主要现象是 _________ ;
(3)由实验三除了能得出可燃物燃烧的条件外,还可以比较出白磷、红磷化学性质上的不同点是 _________
(4)实验四得到的滤液仍然浑浊,原因是 _________ (答一点即可)
查看答案和解析>>
科目: 来源: 题型:
【题目】现有锌和另一种金属组成的合金6.5g,洋洋同学向此合金中加入100g一定溶质质量分数的稀盐酸,充分反应后发现金属完全消失,若产生氢气的质量为m.则下列判断正确的是( )
A.如果合金为锌和铁,m不可能是0.2g
B.反应后溶液中的溶质只有两种
C.如果合金为锌和镁,m可能是0.1g,则该合金中锌的质量分数为50%
D.如果合金为锌和铁,所加稀盐酸溶质质量分数一定大于7.3%.
查看答案和解析>>
科目: 来源: 题型:
【题目】下列四个图象,分别对应四种操作过程,其中正确的是
A. 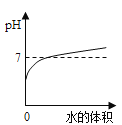 向盐酸中不断加水
向盐酸中不断加水
B. 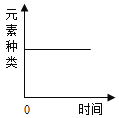 一定质量的镁在密闭的容器内燃烧
一定质量的镁在密闭的容器内燃烧
C. 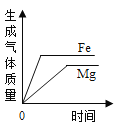 等质量的铁和镁同时分别放入两份溶质质量分数相同的足量稀盐酸中
等质量的铁和镁同时分别放入两份溶质质量分数相同的足量稀盐酸中
D. 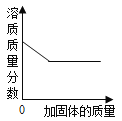 某温度下,向一定质量的饱和氯化钠溶液中加入氯化钠固体
某温度下,向一定质量的饱和氯化钠溶液中加入氯化钠固体
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室里有一瓶标签破损的硫酸,为测定其实际的溶质质量分数,小明同学在烧杯中加入50g稀硫酸,然后向烧杯内滴加溶质质量分数为10%的氢氧化钠溶液,边滴加边搅拌,随着氢氧化钠溶液的加入,溶液的pH变化情况如下表所示:
氢氧化钠溶液的质量/g | 溶液的pH | 溶液中的溶质 |
30 | pH<7 | a |
40 | pH=7 | b |
50 | pH>7 | c |
分析并计算:
(1)溶液中的溶质含有2种阴离子的是 ________(从abc中选)。
(2)计算硫酸溶液中溶质的质量分数________ (结果精确到0.1%)。
查看答案和解析>>
科目: 来源: 题型:
【题目】化学兴趣小组的同学们探究用Fe从含Fe2(SO4)3和CuSO4的溶液中获取金属Cu的原理,请你一起参与探究。小明将光亮的铁丝插入含Fe2(SO4)3和CuSO4的废液中,一段时间后取出,意外地发现铁丝表面没有变红。
(提出问题)Fe为什么没有从废液中置换出Cu呢?
(查阅资料)硫酸铁溶液为黄色,其中的三价铁离子具有较强的氧化性,所以能和很多金属反应,如能和铁或铜发生反应。
(进行猜想)小丽认为在铁丝表面可能有Cu析出,但被Fe2(SO4)3溶液溶解了。
(实验探究)小宇对小丽的猜想以及信息都有怀疑,于是,他们共同做了以下实验:
主要实验用品:洁净的铁丝和铜丝各两根,相同体积、相同浓度的Fe2(SO4)3溶液三份。
实验操作 | 实验现象和数据 | 结论 |
①准确称量洁净的铁丝和铜丝的质量 | 铁丝质量为ag, 铜丝质量为bg | |
②将铁丝插入Fe2(SO4)3溶液中,一段时间后取出、洗净、干燥、称量 | 铁丝质量为mg, m<a,溶液由黄色变为浅绿色 | 一定有__生成(填化学式) |
③将铜丝插入Fe2(SO4)3溶液中,一段时间后取出、洗净、干燥、称量 | 铜丝质量为ng n____b(填>或<) | 铜确实能与Fe2(SO4)3溶液反应 |
④另取相同质量、相同粗细的洁净铁丝和铜丝互相缠绕,插入Fe2(SO4)3溶液中,一段时间后取出、洗净、干燥、分别称量铁丝和铜丝的质量 | 铁丝质量减轻 铜丝质量不变 | Fe、Cu共存时____优先与Fe2(SO4)3溶液反应 |
(探究结论)小丽的假设______(选填“成立”或“不成立”),理由是____。
(拓展分析)①兴趣小组的同学们通过对上述实验的分析,找到了用Fe从含Fe2(SO4)3和CuSO4的溶液中提取金属Cu的关键,并且最终实验获得了成功,其实验成功的关键是:__________,并且反应充分。②已知Fe和Fe2(SO4)3发生化合反应,请按反应顺序写出用Fe从含Fe2(SO4)3和CuSO4的溶液中获取金属Cu的化学方程式:_______;_______。
查看答案和解析>>
科目: 来源: 题型:
【题目】化学兴趣小组的同学获得两包制作“跳跳糖”的添加剂,一包是柠檬酸晶体,另一包是标注为钠盐的白色粉末。同学们将少量柠檬酸和这种白色粉未溶于水,混合后产生了使澄清石灰水变浑浊的气体,于是他们对白色粉末的化学成分进行了以下探究:
(提出猜想)猜想1.碳酸钠;猜想2.碳酸氢钠;猜想3.___________。
(查阅资料)①碳酸钠溶液、碳酸氢钠溶液均呈碱性;② 碳酸氢钠受热分解生成碳酸钠、水和二氧化碳;碳酸钠受热不分解
(实验探究)兴趣小组设计不同实验方案进行探究。
甲组方案:将白色粉末溶于水后用pH试纸测定其酸碱度,pH>7猜想1正确
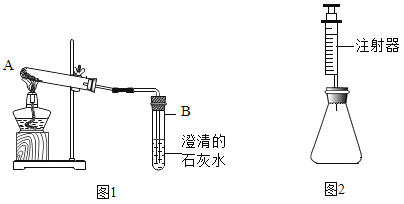
乙组方案:如图1,取适量白色粉末于试管中,将导管伸入澄清石灰水,加热,澄清石灰水变浑浊,猜想2正确,写出装置B中反应的化学方程式______________。
丙组方案:用如图2所示装置作为反应容器,准确测量生成气体的体积以判断白色粉末的成分。分别向盛有碳酸钠、碳酸氢钠和白色粉末的锥形瓶中,注入等体积、等浓度的足量的稀盐酸,记录如表:
实验编号 | 锥形瓶内物质[来源 | 最终得到 CO2 体积/mL | |
名称 | 质量/g | ||
① | 碳酸钠 | a | V1 |
② | 碳酸氢钠 | a | V2 |
③ | 白色粉末 | m | V3 |
实验①的化学反应方程式为____________; 表中 m=_______g; 根据上表中数据分析,猜想3正确,判断的依据是__________。
(交流反思)大家讨论后认为甲、乙组的结论都不准确:不准确的原因,甲是__________;乙是_____________。
(结论分析)探究后他们核查到添加剂的成分是柠檬酸和碳酸氢钠,分析后认为白色粉末中的碳酸钠是由碳酸氢钠分解产生的。
(拓展应用)下列物质常温下放置一段时间也会分解的是________(填序号)。
A 碳酸 B 氨水 C 碳酸氢铵 D 盐酸
查看答案和解析>>
科目: 来源: 题型:
【题目】请结合下列实验装置,回答有关问题.

(1)写出仪器a和b的名称:a______,b______.
(2)实验室用过氧化氢溶液制取并收集氧气,应选择的装置为______(填字母),发生反应的化学方程式为_________。实验室用石灰石与稀盐酸反应制取并收集二氧化碳,应选择的装置为________(填字母)。化学反应方程式为 ________。
(3)实验室用加热氯化铵和氢氧化钙固体混合物的方法制取氨气(NH3),同时得到氯化钙和水。该反应的化学方程式是_____,应选用的发生装置为________。
(4)如图是实验室常用的一个装置,相关说法错误的是(____)
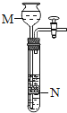
A M中盛放硫酸,N中隔板上放大理石,可以制二氧化碳
B 关闭弹簧夹,在M中不断加水,水面不断下降,证明该装置气密性良好
C 该装置可以控制反应的发生和停止,其原理与启普发生器相同
D N中储满气体后,通过M将水注入N,一定可以排出N中的气体
查看答案和解析>>
科目: 来源: 题型:
【题目】“水与我们的生活息息相关”。请回答下列与水有关的问题。
(1)水中鱼类可以呼吸因为水中溶有 ______________(写化学式)。
(2)一壶水烧开了,壶盖被顶开,这是因为_____________(填写序号)。
A 水分子变大了 B 水分子变多了 C 水分子不停地运动 D 水分子之间的间隔变大了
(3)电解一定量的水,当其中一个电极产生5 mL氧气时,另一电极产生的氢气体积______mL。
(4)自来水中的游离氯有少量可转变为氯离子,氯离子的符号是________。
(5)水瓶胆壁上的水垢的主要成分有CaCO3,可用家中厨房里有的_______________除去。
A 白酒 B 酱油 C 食醋 D 食盐
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com