
科目: 来源: 题型:
【题目】如图是KNO3和NaCl两物质的溶解度曲线,下列说法正确的是
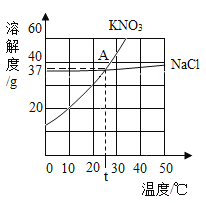
A.将30 ℃时KNO3的饱和溶液转化为不饱和溶液,可采取降温或加水的方法
B.KNO3的溶解度比 NaCl 大
C.t ℃时,两物质饱和溶液的溶质质量分数相等
D.KNO3中含有少量 NaCl,可采用蒸发结晶的方法除去 NaCl
查看答案和解析>>
科目: 来源: 题型:
【题目】下图为某反应的微观示意图(一种小球代表一种元素的原子,其中反应条件已略去),下列说法错误的是
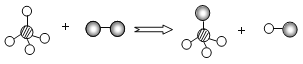
A.该反应前后分子的种类发生改变
B.该反应的本质是分子分解成原子,原子又重新结合成新的分子
C.该反应中反应物都是化合物
D.该反应的微观示意图可以表示 ![]() 的反应
的反应
查看答案和解析>>
科目: 来源: 题型:
【题目】水是宝贵的自然资源。 下列说法错误的是

A.电解水实验(如图)可以说明水是由氢元素和氧元素组成的化合物
B.沉淀、过滤和吸附是工业中常用的净水方法
C.为了节约用水,洗菜、淘米后的水用来浇花
D.为了防止水体污染,农业上禁止使用化肥和农药
查看答案和解析>>
科目: 来源: 题型:
【题目】某兴趣小组在实验室中探究金属钠与二氧化碳的反应。
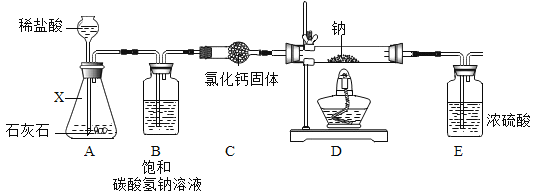
请回答下列问题:
(1)仪器X 的名称是_________;装置C 的作用是__________。
(2)装置B 的作用是除去 CO2 气体中混有的少量HCl 气体,反应的化学方程式为_________。
(3)实验开始时,应先通一段时间的CO2气体再点燃D 装置处的酒精灯,主要目的是_________。
(4)实验过程中D 装置可观察到的现象是:金属钠剧烈燃烧,产生大量白烟,玻璃管内壁上有黑色和白色两种固体产物生成。为了检验黑、白两种固体产物的成分,兴趣小组同学进行如下实验:
步骤 1:将玻璃管内壁的固体物质加入适量蒸馏水中,充分振荡后静置,过滤,滤纸上留下黑色固体,滤液为无色溶液。
步骤 2:取步骤1的无色滤液适量于 2 支试管中,向一支试管中滴加盐酸溶液,有无色气体产生;向第二支试管中滴加澄清石灰水,有白色沉淀生成。
步骤 3:将步骤 1 中的黑色固体与氧化铜固体混合,用酒精喷灯加热混合物,将生成的气体通入澄清的石灰水,溶液变浑浊。
①步骤 1 中过滤操作所需的玻璃仪器有:玻璃棒、烧杯、_________。
②本实验中金属钠与二氧化碳反应的化学方程式为__________。
查看答案和解析>>
科目: 来源: 题型:
【题目】以天然气(含少量 H2S 气体)为原料可获得工业合成氨所需的 N2 和 H2,其转化步骤如下:
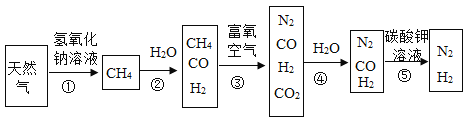
(1)天然气属于____燃料。合成氨的反应方程式为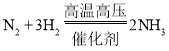 ,该反应属于_________(填基本反应类型)。氨气(NH3)常用于制备__________(填“氮”、“磷”或“钾”)肥。
,该反应属于_________(填基本反应类型)。氨气(NH3)常用于制备__________(填“氮”、“磷”或“钾”)肥。
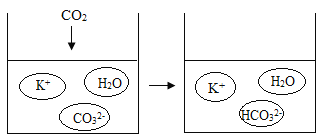
(2)步骤⑤中所涉化学反应前后主要微粒种类变化如图所示。试写出该反应的化学方程式:_______。
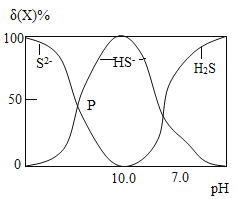
(3)步骤①中所用NaOH 溶液可吸收天然气中的H2S 气体并与之发生反应。常温下随着 H2S不断被吸收,NaOH 溶液的pH逐渐减小,溶液中含硫粒子(S2-、HS-、H2S)的分布δ(X)如图所示。
注:已知H2S气体溶于水后可解离出H+、HS-和 S2-。
δ(X)=![]()
①溶液的 pH=7 时,溶液呈________(填“酸性”、“碱性”或“中性”)。P 点对应的溶液中溶质主要为NaHS 和________,溶液中 S2-的个数_________(填“大于”、“等于”或“小于”)HS-的个数。
②当溶液的 pH=10 时,NaOH 与H2S 反应的化学方程式为____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】过一硫酸氢钠复合盐(Na2SO4·NaHSO4·2NaHSO5)是一种新型酸性过氧化物消毒剂。以过氧化氢溶液、浓硫酸、碳酸钠为原料制备过一硫酸氢钠复合盐的一种工艺流程如下:
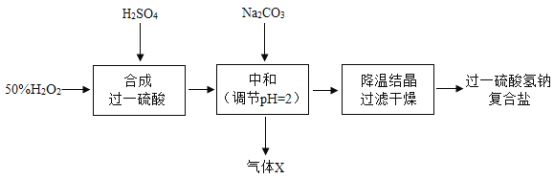
注:过一硫酸(H2SO5)在常温下为无色晶体,熔点 45℃,易溶于硫酸溶液中,可与水缓慢反应生成硫酸与过氧化氢,受热易分解。
(1)碳酸钠的俗名为________。过一硫酸氢钠复合盐中共含有_________种元素。
(2)中和过程中有如下反应发生:Na2CO3 + H2SO4 = Na2SO4 + X↑+ H2O。气体 X的化学式为_________。
(3)在合成过一硫酸时,反应温度应控制在-4℃左右的主要原因是_____。
(4)固定H2O2的用量,以H2O2与H2SO4的质量比、中和温度及所加 Na2CO3 的质量为变量,可探究上述三种因素对复合盐产量的影响(见下表)。
实验序号 | H2O2 与 H2SO4 质量比 | 中和温度/℃ | Na2CO3 用量/g |
① | 47.6 : 29.8 | 7 | 23.0 |
② | 47.6 : 33.6 | 10 | 25.0 |
③ | 47.6 : 25.3 | 4 | 21.5 |
④ | 47.6 : 29.8 | 10 | 23.0 |
⑤ | 47.6 : 25.3 | 7 | 21.5 |
上述实验中,可用来探究中和温度对复合盐产量影响的是__________(填字母)。
a 实验①、④ b 实验②、③ c 实验③、④ d 实验③、⑤
(5)在双氧水定量的基础上,所用硫酸溶液中溶质的质量分数与复合盐中活性氧含量的关系见下图。
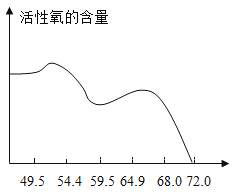
①验过程中选用质量分数为55%左右的硫酸溶液,主要原因是_______。
②配制 98g 质量分数为55.2%的硫酸溶液所需质量分数为 98%的硫酸溶液(密度约为1.84g/cm3)的体积为_______mL。
查看答案和解析>>
科目: 来源: 题型:
【题目】化学在人类的生产、生活中发挥着巨大作用。
(1)合理应用化学知识可提高人们的生活质量。
①下列食物中,富含蛋白质的是 ___(填字母)。
a  牛肉 b
牛肉 b  马铃薯 c
马铃薯 c  花生油 d
花生油 d  葡萄
葡萄
②菠菜中富含铁元素,经常食用可预防____。
(2)铁线莲是一种适宜在碱性土壤中生长的植物。

①欲在酸性土壤中种植铁线莲,可将适量的___(填化学式)加入土壤,以中和其酸性。
②铁线莲过冬期间常覆盖聚乙烯膜以御寒保温。聚乙烯属于 ___(填字母)。
a 金属材料 b 合成材料 c 复合材料
(3)2019 年政府工作报告中首次提出要加强加氢(H2)设施建设。人类可以通过电解水的方式获取氢能源。试写出电解水时反应的化学方程式: ____________。
(4)“鹊桥号”中继星的伞状通信天线是由表面镀金的钼丝编织而成。钼元素在元素周期表中的相关信息及原子结构示意图如下图所示。根据图示信息回答下列问题:
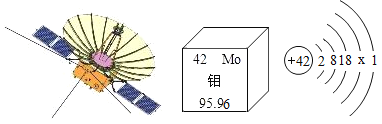
①x=______。
②二硫化钼是制备金属钼的主要原料。试写出二硫化钼的化学式:_________。
查看答案和解析>>
科目: 来源: 题型:
【题目】甲、乙、丙、丁和戊五种物质分别属于酸、碱、盐、单质、氧化物中的一种。它们之间的关系如图所示(“→”表示物质间的转化关系,“—”表示两端的物质能发生反应,部分反应物、生成物及反应条件已略去)。甲是由地壳中含量最高的金属元素组成的单质,丁的相对分子量为 135,其水溶液呈蓝色。下列说法中正确的是
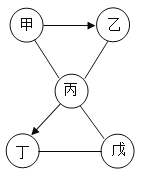
A.甲可能是 Fe,乙可能为 Fe3O4
B.丙→丁的转化可通过中和反应实现
C.甲浸入丁的水溶液中后,表面有银白色固体析出
D.丙与戊的反应可能为 2KOH+ H2SO4 = K2SO4 + 2H2O
查看答案和解析>>
科目: 来源: 题型:
【题目】下图是甲、乙两种物质的溶解度曲线,下列说法正确的是

A.甲、乙两种物质中,乙的溶解度受温度影响比甲的大
B.40℃时甲和乙的饱和溶液,降温至 20℃时仍是饱和溶液
C.40℃时甲和乙各 40g 分别加入 100g 水中,均形成饱和溶液
D.40℃时,将 30g 甲物质加入 50g 水中,充分搅拌后,所得溶液质量为 80g
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com