
【题目】过一硫酸氢钠复合盐(Na2SO4·NaHSO4·2NaHSO5)是一种新型酸性过氧化物消毒剂。以过氧化氢溶液、浓硫酸、碳酸钠为原料制备过一硫酸氢钠复合盐的一种工艺流程如下:
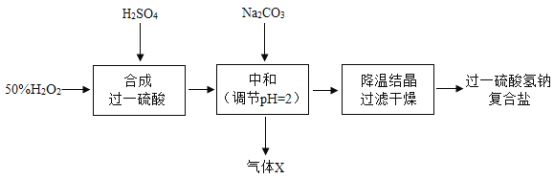
注:过一硫酸(H2SO5)在常温下为无色晶体,熔点 45℃,易溶于硫酸溶液中,可与水缓慢反应生成硫酸与过氧化氢,受热易分解。
(1)碳酸钠的俗名为________。过一硫酸氢钠复合盐中共含有_________种元素。
(2)中和过程中有如下反应发生:Na2CO3 + H2SO4 = Na2SO4 + X↑+ H2O。气体 X的化学式为_________。
(3)在合成过一硫酸时,反应温度应控制在-4℃左右的主要原因是_____。
(4)固定H2O2的用量,以H2O2与H2SO4的质量比、中和温度及所加 Na2CO3 的质量为变量,可探究上述三种因素对复合盐产量的影响(见下表)。
实验序号 | H2O2 与 H2SO4 质量比 | 中和温度/℃ | Na2CO3 用量/g |
① | 47.6 : 29.8 | 7 | 23.0 |
② | 47.6 : 33.6 | 10 | 25.0 |
③ | 47.6 : 25.3 | 4 | 21.5 |
④ | 47.6 : 29.8 | 10 | 23.0 |
⑤ | 47.6 : 25.3 | 7 | 21.5 |
上述实验中,可用来探究中和温度对复合盐产量影响的是__________(填字母)。
a 实验①、④ b 实验②、③ c 实验③、④ d 实验③、⑤
(5)在双氧水定量的基础上,所用硫酸溶液中溶质的质量分数与复合盐中活性氧含量的关系见下图。
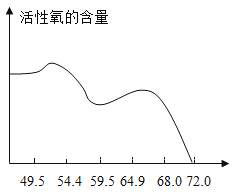
①验过程中选用质量分数为55%左右的硫酸溶液,主要原因是_______。
②配制 98g 质量分数为55.2%的硫酸溶液所需质量分数为 98%的硫酸溶液(密度约为1.84g/cm3)的体积为_______mL。
【答案】纯碱或苏打 四 CO2 防止过一硫酸受热分解 a、d 在此时活性氧含量最高 30
【解析】
(1)碳酸钠俗称纯碱或苏打;过一硫酸氢钠复合盐中一共含有Na、S、O、H四种元素;故填:纯碱或苏打;四。
(2)根据质量守恒定律可知化学反应前后原子种类、数目不变,反应前有钠原子2个,碳原子1个,氧原子7个,氢原子2个,硫原子1个,反应后钠原子2个,氧原子5个,氢原子2个,硫原子1个,缺了1个碳原子和2个氧原子,故X是CO2。故填:CO2。
(3)因为过一硫酸(H2SO5)熔点低且受热易分解,而浓硫酸入水会放出大量热,反应过程中也有热量放出,所以反应温度应控制在-4℃左右。故填:防止过一硫酸受热分解。
(4)要探究中和温度对复合盐产量影响,那么必须保证H2O2与H2SO4的质量比、所加 Na2CO3 的质量这俩是相同的,中和温度是不同的,根据表中数据可知实验①、④或实验③、⑤都满足,故填:a、d。
(5)①由图像可知在双氧水定量的基础上硫酸溶液在质量分数为55%左右时活性氧含量最高,所以才选用此时的质量分数。故填:在此时活性氧含量最高。
②设配制98g质量分数为55.2%的稀硫酸,需要质量分数为98%的浓硫酸的体积为x。根据溶液稀释前后溶质的质量不变得:98g×55.2%=1.84g/cm3×x×98%,得x=30ml。故填:30。


科目:初中化学 来源: 题型:
【题目】酸、碱、盐是几类重要的化合物。
(1)打开盛有浓盐酸和浓硫酸的试剂瓶盖,立即就能把它们区分开来的原因是_____。
(2)100 g质量分数为10%的稀硫酸和100 g质量分数为10%的氢氧化钠溶液充分反应后,溶液的pH_____7(填“大于”“小于”或“等于”)。
(3)在“创新实验装置”的竞赛中,某化学兴趣小组的同学设计了如图所示的装置。
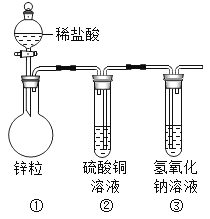
①写出装置甲中发生反应的化学方程式_____。
②丙装置中会出现什么现象_____。
(4)某同学为了除去NaCl溶液中CaCl2、MgCl2、Na2SO4杂质制取精盐,制作流程如图所示:[提示:Mg(OH)2、BaSO4、BaCO3难溶于水]
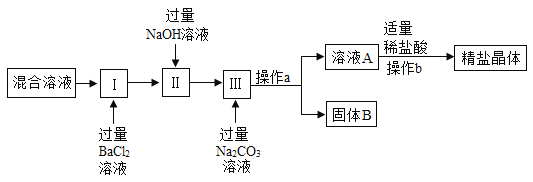
①写出第I步中加入过量BaCl2溶液所发生反应的化学方程式_____。
②操作a的名称为_____。
③通过操作a所得溶液A中除氯化钠外,还含有的溶质有哪些_____?
(5)向20 g含有氯化钠杂质的碳酸钠固体中加入100 g稀盐酸,恰好完全反应,得到115.6g不饱和溶液。求所用稀盐酸的溶质质量分数_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】对乙酰氨基苯酚(C8H9NO2)是速效感冒胶囊的有效成分之一。下列叙述正确的是( )
A. 对乙酰氨基苯酚的相对分子质量是141
B. 对乙酰氨基苯酚中含有2个氧原子
C. 对乙酰氨基苯酚中碳元素的质量分数最大
D. 对乙酰氨基苯酚中,碳、氢、氮、氧元素的质量比是8∶9∶1∶2
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】A、B、C三种固体物质的溶解度曲线如图所示,回答下列问题 。
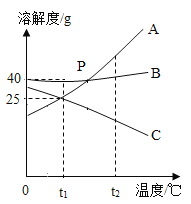
(1)t1℃时,A、B、C三种物质中溶解度最大的是_______ ;
(2)t1℃时,在盛有100克水的烧杯中,加入50克B物质,充分溶解后,得到溶液的质量为_______g;
(3)t1℃时,C的饱和溶液的溶质质量分数为_______ ;
(4)将t1℃的A、B、C三种饱和溶液分别升温至t2℃,所得溶液中溶质质量分数由大到小的顺序是_______________ 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图为某反应的微观示意图(一种小球代表一种元素的原子,其中反应条件已略去),下列说法错误的是
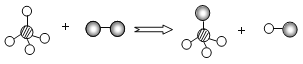
A.该反应前后分子的种类发生改变
B.该反应的本质是分子分解成原子,原子又重新结合成新的分子
C.该反应中反应物都是化合物
D.该反应的微观示意图可以表示 ![]() 的反应
的反应
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】已知 A、B、C、D 是初中化学中常见的四种不同类别的物质,A 是一种经过一系列复杂变化形成的红色固体,用“—”表示物质之间可以相互反应,用“→”表示一种物质可以转化生成另一种物质(部分反应物、生成物和反应条件已略去)。 请回答下列问题:
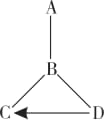
(1)A 的化学式:_______________。
(2)写出 A-B 反应的化学方程式:_____________,工业上该反应可应用于______________。
(3)写出 D→C 反应的化学方程式:_______________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】请回答下列与金属有关的问题。
(1)生铁片与纯铁片相互刻画时,在_____片表面会留下划痕。
(2)为了防止月饼变质,常在月饼的内包装袋中放入一小包防腐剂,它的主要成分是铁粉,铁粉的作用是_____。
(3)向AgNO3和Cu(NO3)2的混合溶液中加入一定量的Zn粉,充分反应后过滤,向滤渣中加盐酸有气泡,则滤渣中一定含有的金属是_____。
(4)为了达到收旧利废的目的,欲从含有金属镁、铁、铜的粉末中,分离和提取出重要化工原料MgSO4和有关金属,其主要实验过程如下,请回答:
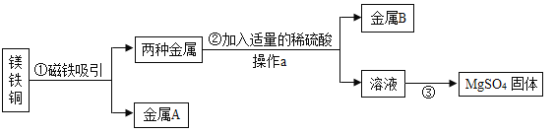
①步骤①中被磁铁吸引的金属A是_____。
②步骤③的操作是_____。
③步骤②所涉及的化学方程式为_____。
(5)将7.3g已部分氧化的锌粉,加入到98g10%的稀硫酸中,恰好完全反应。则所得溶液中溶质的质量为_____(填序号)。
A 14.5g B 5.5g C 16.1g D 18.1g
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】国家卫健委向民众发布防治指南中明确指出 75%的医用酒精可以杀灭新型冠状病毒,下列关于酒精(C2H5OH)的说法错误的是( )

A.酒精属于有机化合物
B.酒精由碳、氢、氧三种元素构成
C.酒精分子中碳、氢、氧原子的个数比2:6:1
D.酒精中碳元素的质量分数最大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com