
【题目】A、B、C三种固体物质的溶解度曲线如图所示,回答下列问题 。
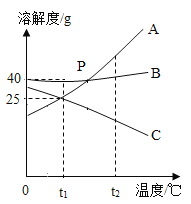
(1)t1℃时,A、B、C三种物质中溶解度最大的是_______ ;
(2)t1℃时,在盛有100克水的烧杯中,加入50克B物质,充分溶解后,得到溶液的质量为_______g;
(3)t1℃时,C的饱和溶液的溶质质量分数为_______ ;
(4)将t1℃的A、B、C三种饱和溶液分别升温至t2℃,所得溶液中溶质质量分数由大到小的顺序是_______________ 。
【答案】B 140 20% B>A>C
【解析】
(1)由溶解度曲线可知,t1℃时,A、B、C三种物质的溶解度大小关系是B>A=C。故A、B、C三种物质中溶解度最大的是B;
(2)由溶解度曲线可知,t1℃时,B的溶解度是40g,故在盛有100克水的烧杯中,加入50克B物质,充分溶解后,得到溶液的质量为140g;
(3)t1℃时,C的溶解度为25g。故C的饱和溶液的溶质质量分数为![]() ×100%=20%;
×100%=20%;
(4)由溶解度曲线可知,t1℃时,A、B、C三种物质的溶解度大小关系是B>A=C,A、B的溶解度随温度的升高而增大,C的溶解度随温度的升高而降低。故将t1℃的A、B、C三种饱和溶液分别升温至t2℃,A、B溶质质量分数不变,C溶质质量分数变小,因此所得溶液中溶质质量分数由大到小的顺序是B>A>C。


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:
【题目】化学是认识、改造和应用物质的科学。从海水中提取镁、制“碱”,都体现了人类改造物质的智慧。结合下列流程图(其中部分操作和条件已略去),请回答相关问题:
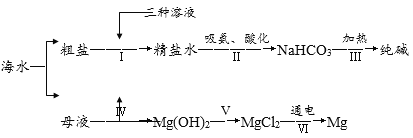
(1)提纯物质常用转化的方法,就是将杂质转化为沉淀或气体而除去。粗盐中含有氯化镁、硫酸钠、氯化钙等可溶性杂质,通过步骤Ⅰ,再利用过滤操作进行除杂。步骤Ⅰ加入下列三种溶液的先后顺序为_____(填字母序号);
a.稍过量的Na2CO3溶液 b.稍过量的BaCl2溶液 c.稍过量的NaOH溶液
(2)母液中有MgCl2,却经历了步骤Ⅳ、Ⅴ的转化过程,其目的是_____;
(3)步骤Ⅱ中先向饱和食盐水中通入氨气,有利于二氧化碳的吸收,这样做的目的是_____,写出该反应的化学方程式_____;
(4)化学变化是改造物质的重要途径。上述流程图中没有涉及的基本反应类型是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】氯化钠是日常生活的必需品,也是重要的化工原料,海水“晒盐”得到的是粗盐。粗盐除含NaCl 外,还含有少量 MgCl2、CaCl2、Na2SO4以及泥沙等杂质
(1)有关粗盐提纯的实验操作合理的是___(填序号)。
A 溶解前用玻璃棒研磨大颗粒粗盐
B 过滤时液体的液面要低于滤纸边缘
C 蒸发时要不断搅拌直至水分全部蒸干
D 实验结束用玻璃棒把固体转移到纸上,称量后,回收到指定容器中
(2)粗盐进行精制,流程如图。

温合液Ⅲ经过“过滤”操作,得到沉淀的成分有:泥沙、BaSO4、Mg(OH)2、___(填化学式)
(3)加入过量的NaOH溶液的目的为___(用化学方程式表示)。
(4)实验所得精盐的质量大于粗盐中NaCl的质量,原因是___。
查看答案和解析>>
科目:初中化学 来源: 题型:
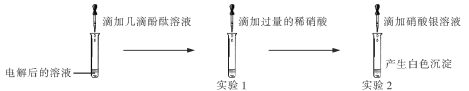
【题目】工业采用电解氯化钠溶液制备烧碱。某同学取电解后的溶液进行如下探究:
(提出问题)电解后的溶液中的溶质是什么?
(猜想假设)(1) NaOH、NaCl (2) NaOH
(实验探究)取电解后的溶液,进行如下实验:
(收集证据)实验1的反应现象为(1)____________,实验2发生反应的化学方程式为(2)_______。
(实验结论)电解后的溶液中的溶质是(3)____________________。
(表达交流)实验中滴加酚酞溶液的作用是(4)____________________。在滴加过量稀硝酸的过程中,下图中①表示的是(5)____________________(填符号),②表示的是(6)____________________(填符号)。
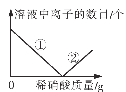
(总结规律)通过探究还可以认识到:上述实验1和实验2的反应都是两种化合物在溶液中以(7)____________________的形式,通过一种(8)____________________的方式而发生的复分解反应。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】过氧化钙(CaO2)是一种重要的化工产品,可用来改善地表水质、治理赤潮,过氧化钙产品中常含有氧化钙杂质,以下是某学习小组为测定过氧化钙产品纯度设计的实验,实验装置如图;已知:CaO2是一种白色粉末,微溶于水,易溶于稀盐酸,且发生反应: CaO2+2HCl=CaCl2+H2O2

实验步骤:实验前称取产品及二氧化锰共12克,先缓慢通入氮气,一段时间后,加热铜网至红热,再缓慢滴入过量稀盐酸,直至A中样品完全反应。继续缓慢通入氮气,一段时间后停止加热,待C中铜网冷却后,停止通入氮气,将锥形瓶中的剩余物过滤,洗涤,干燥,得到滤渣2.0克。回答下列问题,
(1)二氧化锰与稀盐酸不反应,A中二氧化锰的作用是______________
(2)样品完全反应后,继续缓慢通入氮气的目的是______________
(3)装置B的作用有,除去气体中的水蒸气、______________
(4)实验测得C装置中铜网增重1.8克,该产品中过氧化钙的质量分数为_____________
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(1)小雨为了验证质量守恒定律设计了如图1所示的实验A、B。其中实验前后天平不能保持平衡的是______(填序号),理由是_____________________。实验A中小气球的变化是_____________。
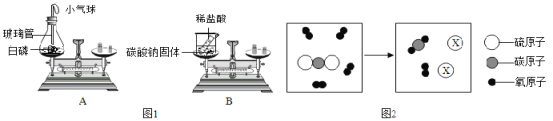
(2)某反应的微观示意图如图2所示。①X的化学式是_______ 。②根据上述微观示意图,可得出化学反应遵循质量守恒定律的本质原因是______________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某同学设计了测定空气中氧气含量的实验,实验装置如图。该同学的实验步骤如下:
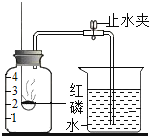
①将图中的集气瓶分为5等份,并作好标记。
②在带橡皮塞和导管的燃烧匙内装入足量的红磷,将
导管上的止水夹夹紧,在酒精灯上点燃红磷,并立即
伸入集气瓶内,塞紧橡皮塞。
③充分反应后,待集气瓶冷却至室温,打开止水夹。
请回答下列问题:
(1)该实验中红磷需稍过量,目的是_______。
(2)步骤③中打开止水夹后观察到的现象是_______,由此可得出空气中氧气的体积分数约为_____。
(3)该实验可推论出氮气__________(填“易”或“难”)溶于水和其化学性质________(填“活泼”或“不活泼”)的结论。
(4)若将红磷换成炭粉,该实验能否获得成功?_______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图表示氯酸钾和二氧化锰混合受热至完全反应的过程中某变量y随时间的变化趋势,纵坐标表示的是( )
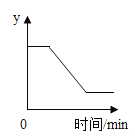
A. 剩余固体的质量B. 生成氧气的质量
C. 固体中二氧化锰的质量D. 氯酸钾的质量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com