
科目: 来源: 题型:
【题目】如图是元素周期表的一部分,及A、B、C、D是四种粒子的结构示意图.

(1)氟元素的原子序数为______,氧元素的相对原子质量为______。
(2)B所表示粒子的符号为_______,C表示的粒子在化学反应中易______电子(填“得到”或“失去”)。
(3)A、B、C、D四种粒子中属于同种元素的是______(填序号,下同);化学性质相似的是______。具有相对稳定结构的粒子是______。
查看答案和解析>>
科目: 来源: 题型:
【题目】如图是家用豆浆机,请根据图回答下列问题:

(1)属于有机合成材料的是______(填物质编号);
(2)豆浆中含有的最丰富的营养物质是______;
(3)传统的生豆浆是用石磨来打磨的,打磨的过程属于______变化;
(4)用操作将黄豆渣分离的方法类似于我们实验中的______操作;
(5)金属在生活生产中有重要的应用.某化学兴趣小组向硝酸银、硝酸铜、硝酸镁的混合溶液中加入一定质量的锌,充分反应后过滤,得到滤渣A和滤液B.请回答下列问题:
Ⅰ.若反应前后溶液质量不变,A中一定含有______.
Ⅱ.若反应后溶液质量减少,B中一定含有的金属离子是____,不能确定的金属离子是____.
查看答案和解析>>
科目: 来源: 题型:
【题目】将乙醇和氧气置于密闭容器中引燃,测得反应前后各物质的质量如表:
物质(纯净物) | 乙醇 | 氧气 | 二氧化碳 | 水 | X |
反应前质量/g | 2.3 | 4 | 0 | 0 | 0 |
反应后质量/g | 0 | 0 | 2.2 | 2.7 | 待测 |
下列说法正确的是( )
A.反应后X的质量为1.4g
B.X中一定含有碳元素和氢元素
C.X中一定含有碳元素和氧元素
D.X中两种元素的质量比为1:1
查看答案和解析>>
科目: 来源: 题型:
【题目】为测定由盐酸和硫酸组成的某混合酸中溶质的质量分数,取100g该混合酸,逐滴滴加某Ba(OH)2溶液,生成沉淀BaSO4的质量和pH的变化关系如图1所示.
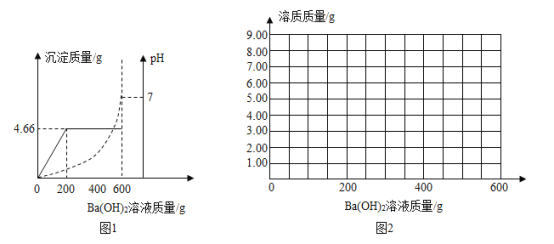
(1)当加入的氢氧化钡溶液为______g时,混合酸恰好被中和.
(2)求Ba(OH)2溶液中的溶质质量分数是多少?_____(写出计算过程,结果精确到0,01%)
(3)盐酸的溶质质量分数是______.(结果精确到0.01%)
(4)请在图2中画出向100g该混合酸中加入600g Ba(OH)2溶液的过程中,混合酸中,生成溶质的质量与所加的Ba(OH)2溶液的质量关系图._____
查看答案和解析>>
科目: 来源: 题型:
【题目】某实验需要100g 7.6%的硫酸亚铁(FeSO4)溶液.
(1)该溶液中含硫酸亚铁的质量为______g(精确到0.1);
(2)硫酸亚铁中硫、氧元素的质量比为______;
(3)实验室用硫酸亚铁晶体(化学式为FeSO47H2O)配制100g 7.6%的硫酸亚铁溶液,需称取硫酸亚铁晶体______g(精确到0.1).(已知相对分子质量:FeSO47H2O为278,FeSO4为152)
查看答案和解析>>
科目: 来源: 题型:
【题目】工业上制备的高锰酸钾是锰的重要化合物.以下是工业上用软锰矿(主要成分是MnO2)制备高锰酸钾的一种工艺流程.

(1)操作I的名称是______.
(2)操作II选用饱和高锰酸钾溶液洗涤的原因是______.
(3)写出反应③的化学方程式______;该反应属于的基本反应类型为______.
(4)上述流程中可以循环使用的物质有________(写化学式).
(5)在该生产过程中,用90kg软锰矿制得了158kg的高锰酸钾.如果不考虑过程中的损耗,可计算出软锰矿中MnO2的质量分数为______.(结果保留一位小数)
查看答案和解析>>
科目: 来源: 题型:
【题目】A﹣G是初中化学的常见物质.其中,A是农药“波尔多液”的成分之一,C是红色金属,E是蓝色沉淀.如图是这些物质的转化关系,部分反应物、生成物及反应条件已省略.
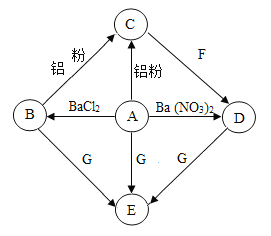
(1)请写出化学式:A______,E______.
(2)写出A→C的化学方程式:______.
(3)在B→C的反应过程中,溶液质量______(填“增加”、“不变”或“减少”).
(4)C与F的溶液反应后得到固体和溶液,取溶液于试管中加入盐酸,无白色沉淀生成,则得到的固体中一定有______(填化学式,下同),可能有______.
查看答案和解析>>
科目: 来源: 题型:
【题目】如图所示为实验室中常见的气体制备、干燥、收集、和性质实验的部分仪器.试根据题目要求,回答下列问题:

(1)写出①装置制取氧气的化学方程式______.
(2)实验室用二氧化锰粉末和过氧化氢溶液制取氧气的反应速率快,宜选择的发生装置为______(填序号),选择该装置的优点是______,用④装置收集氧气时,氧气从导管______(填“a”或“b”)入.
(3)测定某氧化铁样品中铁元素的质量分数(假设杂质不含铁元素,也不与氢气发生反应).某同学设计了用氢气还原氧化铁样品的一组实验:

该实验制取氢气的药品宜选择______(填名称);干燥管内生石灰的作用是______;若取用a克氧化铁样品,测得U型管内物质的质量增加b克,则样品中Fe元素的质量分数为______(用代数表示).
查看答案和解析>>
科目: 来源: 题型:
【题目】以下是初中化学做过的一些实验,回答有关问题.
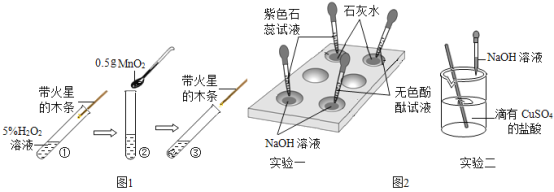
(1)图1是分解H2O2中MnO2作用的探究实验.
步骤①的现象说明常温下过氧化______(填“易分解”或“不易分解”);步骤③反应结束后向试管中加入5%H2O2溶液,伸入带火星的木条,木条______,说明二氧化锰的化学性质没有改变;接着还要完成的实验是______.
(2)在《酸、碱的化学性质》实验中,我们进行过下列一些实验(如图2),回答相关问题:
①实验一选在白色点滴板上进行的优点是______.
②实验二设计的目的是在不使用指示剂的情况下也能证明酸和碱之间能够发生______,当观察到______时,证明酸碱之间的反应已经完成.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com