
科目: 来源: 题型:
【题目】我国化学家侯德榜创立的侯氏制碱法,就是以海水“晒盐”得到的氯化钠为原料,制得纯碱(Na2CO3)。Na2CO3 和NaCl的溶解度曲线如下图1所示,试回答下列问题:
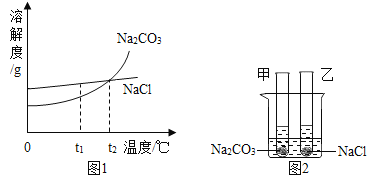
(1)t1°C时,Na2CO3的溶解度______NaCl的溶解度(填“大于”“等于”“小于”之一)。
(2)t2°C时,相同质量的Na2CO3和NaCl的饱和溶液中所含溶质的质量__________ (填“相等”或“不相等”)。
(3)如上图2所示,t2°C时, 甲、乙两试管中分别盛有Na2CO3和NaCl的饱和溶液,并都有少量固体存在.若向试管外盛有水的烧杯中加入某物质后,甲试管中固体明显减少,乙试管中的固体无明显减少,则烧杯中加入的物质可能是_____________ (写一种物质的化学式)。
查看答案和解析>>
科目: 来源: 题型:
【题目】如图中A、B、C、D是四种粒子的结构示意图,
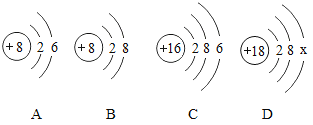
(1)A、B、C、D四种粒子结构示意图中,属于同种元素的粒子是_____,A、B、C三种粒子结构示意图中,属于阴离子的是_____(填序号)。
(2)A粒子的化学性质与B、C、D中哪一种粒子的化学性质相似?_____。(填序号)
(3)D中x=_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】化学兴趣小组活动中,甲、乙、丙三位同学对某化工厂的污水取样后进行了相关实验,请回答下列问题。
I.用pH试纸检测污水的酸碱性。三位同学分别进行如下实验:
甲同学:取pH试纸于表面皿上,用玻璃棒蘸取待测液滴在pH试纸上,测得pH<7.
乙同学:取pH试纸于表面皿上,先用蒸馏水湿润,再用玻璃棒蘸取待测液滴在pH试纸上,测得pH<7。
丙同学:取pH试纸直接浸入待测液中,测得pH <7.
(1)以上三位同学中操作规范的是___________同学。
Ⅱ.利用中和反应原理测定污水中污染物(设为盐酸)的质量分数。甲、乙两同学设计的方案分别如图甲、图乙所示:
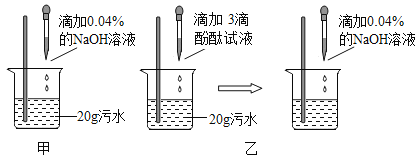
(2)甲同学取少量图甲所示反应后的溶液于试管中,滴加3滴紫色石蕊试液,溶液呈蓝色,于是得出了“两种物质已恰好中和”的结论,甲同学的结论是否正确?_____________ (选填“正确”或“不正确”),理由是______________。
(3)乙同学按图乙方案进行实验,实验过程中,NaOH溶液必须用胶头滴管逐滴加入,且用玻璃棒不断搅拌。当观察到____________现象时, 停止滴加NaOH溶液,此时可认为酸碱恰好完全反应。
(4)若要除去污水中的盐酸,从环保、原材料成本等角度考虑,最好选用________________。
A NaOH
B Ca(OH)2
C Fe2O3
D CaCO3
(5)若图乙方案实验中共消耗了NaOH溶液20g,请计算:
①20g NaOH溶液中溶质质量=______________g.
②污水中HCl的质量分数是多少? ____ (列式计算)
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室利用下图所示装置进行相关实验,请回答问题:
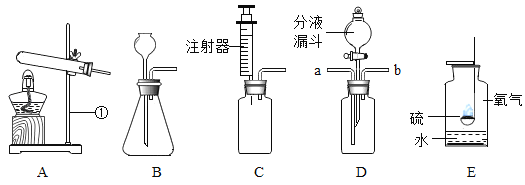
(1)写出有标号①的仪器名称: _____________________。
(2)老师提出用碳酸钠粉末和稀硫酸制取二氧化碳,其反应的化学方程式为____________,为了完成该实验,你认为最合适的发生装置是___________(从A-C 中选择),该装置的最大优点是__________。
(3)用图D验证二氧化碳与水的反应。为验证使石蕊变色的物质是碳酸而不是水或二氧化碳,应采取的实验操作顺序是_____________(填序号, 可重复使用)。
①从b端通氮气
②从分液漏斗中滴加适量水
③从a端通二氧化碳
④将用石蕊溶液染成紫色的干燥纸花放入瓶中
(4)用图E进行硫的燃烧实验时,集气瓶中水的作用为_______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某化学兴趣小组在实验室里完成了以下实验:称取5.0g粗盐(只含泥沙)进行提纯,并用提纯后获得的精盐(NaC1) 配制溶质质量分数为6%的NaCl溶液50g。实验的操作流程如下图所示,请你根据信息回答下述问题:

(1)步骤一中, 操作X的名称是__________;步骤二中, 实验步骤Y的名称为____________。
(2)粗盐加水溶解过程中用到了玻璃棒不断搅拌,它的作用是____________。
(3)某同学所得精盐比其他同学明显要少,原因可能是____________。
(4)配制50g质量分数为6%的NaCl溶液时,某同学量取水时仰视47mL刻度处,则他所配制的NaCl溶液质质量分数____________(填“大于 ”“小于”或“等于”)6%.
查看答案和解析>>
科目: 来源: 题型:
【题目】向Mg(NO3)2、Cu(NO3)2、AgNO3的混合溶液中加入一定量的铁粉并充分反应,得“滤渣”和“滤液”。
(1) Mg. Cu. Ag. Fe四种金属的活动性由强到弱的顺序是_________________。
(2)往“滤渣”中加入盐酸,若无明显规象,则可能发生的反应化学方程式为_______________。
(3)往“滤渣”中加入盐酸,若有气泡产生,则“滤液”中一定有的溶质是_______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】2019年12月16日,淮安正式迈入高铁时代!请结合所学化学知识,回答下列问题:
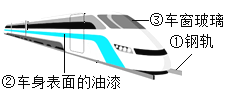
(1)图中标示的物质中为金属材料的是___________(填序号)。
(2)动车电路中的导线大多是用铜制的,这是利用了铜的延展性和__________性。
(3)动车表面喷漆主要是为了防止外壳生锈,其原理是___________.
(4)修建铁路所需的大量钢铁是以铁矿石为主要原料冶炼而得。写出一氧化碳和赤铁矿炼铁的化学反应方程式:____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】经过“碱的化学性质”的学习,小明同学用如图所示的示意图归纳总结了NaOH四条化学性质。
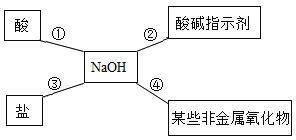
(1)反应①属于的基本反应类型是____________。
(2)为了验证反应②,小明同学向NaOH溶液中滴入无色酚酞试液,观察到无色酚酞试液变为红色,使无色酚酞试液变为红色的微粒是______________(填微粒符号)。
(3)为了验证反应③能够发生,应选用的试剂是______________.
A KNO3
B NaCl
C CuSO4
D Na2CO3
(4) NaOH溶液露置于空气中易变质,所以必须密封保存,请你写出NaOH溶液变质的化学方程式:____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】如图所示为a、b、c三种物质的溶解度曲线。
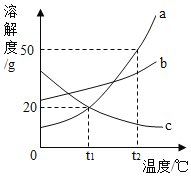
(1)t1℃时,将30ga物质加入到50g水中,而后升温到t2℃,此时该溶液的溶质和溶剂的质量比为__。
(2)t1℃时,24ga的饱和溶液稀释为10%,需要加入水__g。
(3)将t2℃时等质量的a、c的饱和溶液降温至t1℃此时两种溶液中溶质的质量分数大小关系为__。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com