
科目: 来源: 题型:
【题目】材料是生产不可缺少的原料,请完成下面小题。
【1】棉麻、塑料、橡胶等广泛应用于工业生产中,它们当中属于合成材料的是_____。
【2】金属在日常生活中应用广泛。
(1)下列金属制品中,利用金属的导热性的是_____。

(2)我国湿法冶金早在西汉时期就已开始,其中,“曾青得铁则化为铜”便是佐证,即将铁浸入硫酸铜溶液,该反应的化学方程式为_____。
(3)“暖宝宝”中的主要成分是铁粉、氯化钠、活性炭等,其发热原理应用的是铁粉缓慢氧化放热,检验“暖宝宝”是否有效的方法是_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】能源问题关系到可持续发展和环境保护 ,能源是国家和家庭中必不可少的。

(1)化石燃料仍然是当今的主要能源,它包括煤、天然气和____,家庭燃气主要是天然气(主要成分是CH4),甲烷燃烧的化学方程式是_____。
(2)新能源的开发和利用与时俱进,雁栖湖畔的日出东方酒店大量采用光伏发电,光伏发电是利用半导体界面的光生伏特效应而将光能直接转变为电能的一种技术。光伏发电传统的火力发电相比较优点是_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】健康和安全问题责任重大,请完成下面小题。
【1】我们要关注我们的营养问题。
(1)青少年成长需要充足的钙和维生素等,这里的“钙”是指_____(填“元素”或“分子”或“原子”)。下列富含维生素的是_____。
A 蛋 B 菜 C 饭 D
(2)我国科学家发现用亚硒酸钠(Na2SeO3)能消除加速人体衰老的活性氧,亚硒酸钠中硒(Se)元素的化合价为____。
(3)下列做法不利于身体健康的是____。
A 氮气作食品保护气 B 铁锅做炊具烹调食物
C 加碘食盐做调味品 D 甲醛溶液保鲜大白菜
【2】米酒味道变酸是因为米酒中产生的醋酸杆菌使乙醇(C2H5OH)和氧气发生反应生成了醋酸(CH3COOH)和另一种常见的液体。回答下列问题:
(1)食物变质是一种_______氧化反应(填“剧烈”、“缓慢”)。
(2)米酒味道变酸的化学反应方程式为______;可用_____检验米酒味道变酸确实生成了醋酸。
【3】日常生活中安全问题责任重大。
(1)炒菜时,油锅突然着火,用锅盖该灭原理是_____。
(2家用燃气灶使用时出现爆燃、黄火等现象时,发生了不完全燃烧,为使燃气完全燃烧需调节进风量,是为了____。
(3)下列日常生活中为确保人身安全,下列做法正确的是____。
A 气泄漏时,应及时关闭阀门,开窗通风
B 变的大豆、花生等食物因含大量黄曲霉素而不能食用
C 用电器失火,用水浇灭
查看答案和解析>>
科目: 来源: 题型:
【题目】如图表示一定质量的高锰酸钾受热过程中某变量y随时间的变化趋势,则y表示的是
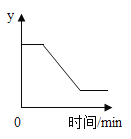
A. 高锰酸钾的质量
B. 固体中钾元素的质量
C. 固体中氧元素的质量
D. 固体中锰元素的质量分数
查看答案和解析>>
科目: 来源: 题型:
【题目】“侯氏制碱法”是我国近代著名科学家侯德榜发明的一种连续生产纯碱与氯化铵的联合制碱工艺。
①生产原理:NaCl(饱和溶液)+NH3+CO2+H2O=NaHCO3(固体)↓+NH4Cl
②主要生产流程如图所示:
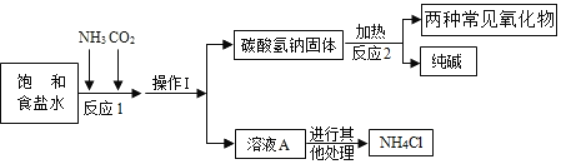
下列叙述不正确的是( )
A. 该过程操作1的名称是过滤
B. 该工艺流程可看出:该温度下碳酸氢钠的溶解度大于氯化铵的溶解度
C. 该过程涉及的物质中元素的化合价不发生改变
D. 图中反应2的化学方程式是2NaHCO3![]() Na2CO3+CO2↑+H2O
Na2CO3+CO2↑+H2O
查看答案和解析>>
科目: 来源: 题型:
【题目】甲、乙两种物质的溶解度曲线如图所示。下列叙述正确的是( )
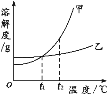
A. 依据溶解度曲线可判断,甲的溶解度比乙的大
B. 将甲、乙的饱和溶液从t2℃降到t1℃,析出甲的质量大
C. t1℃时,甲和乙的饱和溶液各100g,其溶质的质量一定相等
D. 将t2℃时甲的饱和溶液变为不饱和溶液,可采取降温或加水的方法
查看答案和解析>>
科目: 来源: 题型:
【题目】锌是人体重要的必需微量元素,被称作“生命之花”。在元素周期表中,锌元素的某些信息如图所示,下列说法不正确的是
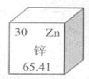
A.锌元素属于非金属元素
B.锌元素原子的核电荷数为30
C.锌元素原子的核外电子数为30
D.锌元素的相对原子质量为65.41
查看答案和解析>>
科目: 来源: 题型:
【题目】珍珠粉是由珍珠加工制成的白色粉末,主要成分是碳酸钙,是重要的化妆品原料,市场上出现的假珍珠粉外观上与真珍珠粉差不多,肉眼无法辨别它们。
(提出问题)假珍珠粉的主要成分是什么?真假珍珠粉的差别在哪里?
(作出猜想)①含有碳酸钙;②含有蛋白质;③含有碳酸钙和蛋白质
(实验一)为了确认珍珠粉的组成,同学们进行了下列实验:
操作方法 | 结论与化学反应方程式 |
| 通过a、b实验及其他手段,证明了二者都含有碳酸钙。b中化学反应方程式: _________________ |
判断真、假珍珠粉中是否含蛋白质的方法是: ______________________ | 真珍珠粉中含有蛋白质,假珍珠粉中不含蛋白质。 |
(拓展实验)将a中完全反应后的混合物过滤,测得滤液的![]() ,是什么物质使滤液的
,是什么物质使滤液的![]() ?小羽和小吴分析后认为只有两种可能性并作了猜想:猜想①:反应后生成的碳酸 猜想②:反应后剩余的盐酸
?小羽和小吴分析后认为只有两种可能性并作了猜想:猜想①:反应后生成的碳酸 猜想②:反应后剩余的盐酸
(实验二)小明和小吴用下列实验对猜想进行验证。
实验操作 | 实验现象 | 实验结论 |
向蒸馏水中通入________至饱和,测pH | pH约为5.6 | 猜想①错误 |
向滤液中滴入石蕊试液,然后加热至沸腾 | ________________ | 猜想②正确 |
写出猜想①发生的化学反应方程式__________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】化学实验室要从含少量铜粉的银、锰混合金属粉末中分离出贵金属,并获得一种盐晶体。将这三种金属随意编号为:A、B、C,并设计了如图1所示流程:

(1)A、B、C三种金属的活动性由强到弱顺序为____________(用元素符号表示)。活泼金属将不活泼金属从溶液中置换出来,实质上是电子在原子和离子间的转移,图2中用“o”表示电子在铁原子和铜离子间移动,则电子的移动方向是________(填序号,“①从铁原子到铜离子”或“②从铜离子到铁原子”)。
(2)写出上述实验中产生的无色气体的一种用途__________________。进行蒸发时,观察到蒸发皿内_______________,停止对蒸发皿进行加热。
(3)金属B与硝酸银反应的化学方程式为____________________。除了用活泼金属外,判断滤液中是否有硝酸银剩余的方法是____________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】碳酸钠广泛用于造纸、纺织、洗涤剂等工业。是一种重要的化工原料,工业制碱法的原理是:![]() ,然后加热分解
,然后加热分解![]() 固体得到
固体得到![]() ,兴趣小组采用下列装置模拟工业制碱法制备碳或氢钠,进而制得碳酸钠。
,兴趣小组采用下列装置模拟工业制碱法制备碳或氢钠,进而制得碳酸钠。
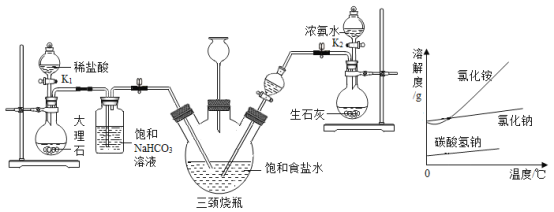
(查阅资料)氨气易溶于水,通常状况下1体积水约溶解700体积的氮气;二氧化碳能溶于水,通常状况下1体积水约溶解1体积的二氧化碳。
(实验过程)
(1)关闭![]() ,打开
,打开![]() 通入
通入![]() 并调节气流速率,然后打开
并调节气流速率,然后打开![]() 通入
通入![]() 。
。
(2)当三颈烧瓶内出现较多固体时,先后停止通入两种气体。
(3)将三颈烧瓶内反应后的混合物过滤、洗涤,并将所得固体加热充分加热。
(问题讨论)
(1)停止通气后三颈烧瓶内的溶液是否是![]() 的饱和溶液?________,洗气瓶中饱和
的饱和溶液?________,洗气瓶中饱和![]() 溶液的作用是__________________(用化学方程式表示)。
溶液的作用是__________________(用化学方程式表示)。
(2)实验中长颈漏斗的作用是____________________。有同学认为应在长颈漏斗内放置蘸有酸液的棉花,理由是_________________。
(3)依据“查阅资料”所得信息,实验结束时应先停止通![]() 还是
还是![]() ?________,已知氯化铵、氯化钠和碳酸氢钠的溶解度如右图所示,从反应后的滤液里得到氯化铵固体可采用的方法是________________。
?________,已知氯化铵、氯化钠和碳酸氢钠的溶解度如右图所示,从反应后的滤液里得到氯化铵固体可采用的方法是________________。
(4)实验过程中先通入![]() ,能充分吸收
,能充分吸收![]() 的原因是_______________。实验中用生石灰能更好地产生氨气,理由是__________________、____________________。
的原因是_______________。实验中用生石灰能更好地产生氨气,理由是__________________、____________________。
(5)加热分解![]() 固体得到
固体得到![]() ,判断得到的
,判断得到的![]() 固体中是否有
固体中是否有![]() 剩余的方法是_________________________。
剩余的方法是_________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com