
科目: 来源: 题型:
【题目】氢氧化镁是一种重要的化工原料,某矿石由MgO、Fe2O3、CuO和SiO2组成。用它制备氢氧化镁的流程示意图如下:

部分金属阳离子以氢氧化物形成沉淀时溶液的pH见下表:
沉淀物 | Fe(OH)3 | Cu(OH)2 | Mg(OH)2 |
开始沉淀 | 1.9 | 4.2 | 9.1 |
完全沉淀 | 3.2 | 6.7 | 11.1 |
(1)熟石灰主要成分的化学式是____________。
(2)溶液A中的阳离子是___________________(填离子符号)。
(3)沉淀C的成分是_____________________。
(4)溶液B与熟石灰反应的化学方程式是____________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】硫酸锂(Li2SO4)和硝酸钾在不同温度时的溶解度如下表:
温度/℃ | 0 | 10 | 20 | 30 | 40 | |
溶解 度/g | Li2SO4 | 36.1 | 35.4 | 34.8 | 34.3 | 33.9 |
KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | |
请回答下列问题:

(1)依据溶解度表,绘制溶解度曲线如图所示,其中能表示Li2SO4溶解度曲线的是_______(填“甲”或“乙”)。
(2)Li2SO4和KNO3在某一温度时具有相同的溶解度x,则x的范围是_________________。
(3)40℃时,有含少量Li2SO4的KNO3饱和溶液,欲从中提纯KNO3晶体,方法是________________。
(4)将10℃时两种物质的饱和溶液分别升温至30℃,所得Li2SO4溶液中溶质的质量分数__________(填“>”、“<”或“=”)KNO3溶液中溶质的质量分数。
(5)如图所示,20℃时,将盛有饱和Li2SO4溶液的试管放入盛水的烧杯中,向烧杯的水中加入某物质后,试管内有晶体析出。则加入的物质可以是______(填字母序号)。
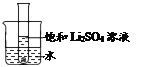
①浓硫酸 ②冰块 ③生石灰固体 ④硝酸铵固体 ⑤氢氧化钠固体
A.②④ B.①③⑤ C.③④ D.①②⑤
查看答案和解析>>
科目: 来源: 题型:
【题目】溴原子结构示意图如图所示。请回答下列问题:
![]()
(1)图中x的值为_________。
(2)溴元素的化学性质与下图中____(填字母标号)的化学性质相似。A、B、C、D属于____种元素。
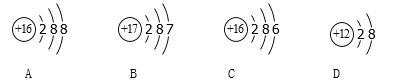
(3)第117号元素在元素周期表中的部分信息如图所示,它与溴元素属同族元素,化学性质与溴元素相似,则第117号元素原子最外层有________个电子,原子中有________个质子。

(4)依据Fe+CuSO4===FeSO4+Cu,推断出Fe的金属活动性比Cu强,非金属也有类似规律,据此推断,在2KI+Cl2===2KCl+I2反应中,Cl2的“非金属活动性”比I2的_____(填“强”或“弱”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】化学兴趣小组的同学在探究分子的特征时设计了如图所示的实验,请你参与他们的探究活动,回答有关问题:烧杯A中盛有10mL浓氨水;在烧杯B、C中分别盛有20mL蒸馏水,并分别滴加3滴酚酞试液于蒸馏水中,得到无色溶液。用只大烧杯把A、B两烧杯罩在一起,几分钟后,观察现象。
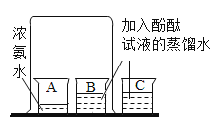
(1)实验中观察到的现象是_____。请你用分子的知识解释出现该现象的原因_____。
(2)由该实验可知氨水具有的性质是:_____。
(3)实验中烧杯C的作用是_____。
(4)该装置有一个明显的不足之处是_____,你的改进建议是_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】向AgNO3、Cu(NO3)2、Mg(NO3)2的混合溶液中,加入一定量的铁粉,充分反应后过滤,滤液呈蓝色。下列判断正确的是( )
A. 滤液中可能有Fe(NO3)2、Mg(NO3)2和Cu(NO3)2
B. 向滤渣中加入稀盐酸,可能有气泡产生
C. 与原溶液相比,滤液的质量可能增大
D. 向滤液中滴入稀盐酸,可能会有白色沉淀出现
查看答案和解析>>
科目: 来源: 题型:
【题目】α-丙氨酸是合成蛋白质的基础物质之一,其分子结构如右图所示。下列有关该物质的说法不正确的是
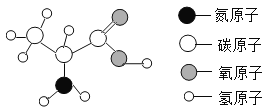
A. 从分类角度看:α-丙氨酸属于有机物
B. 从量的角度看:在α-丙氨酸中碳、氢、氧、氮各元素的原子个数比为3:7:2:1
C. 从变化角度看:α-丙氨酸全燃烧后的产物是二氧化碳和水
D. 从微观角度看:α-丙氨酸是由分子构成
查看答案和解析>>
科目: 来源: 题型:
【题目】活动小组为测定由氧化铜和铜组成的混合物中氧化铜的质量分数,现取3份该固体混合物各20g,分别缓慢加入到50 g、100 g、150 g某稀硫酸中,测得三组实验数据如下表:
组别 | 第1组 | 第2组 | 第3组 |
稀硫酸质量/g | 50 | 100 | 150 |
剩余固体的质量/g | 10.0 | 4.0 | 4.0 |
根据实验及有关数据进行分析与计算:
(1)第1组实验中_____________(填“氧化铜”“稀硫酸”或“氧化铜与稀硫酸”)完全反应。
(2)样品中氧化铜的质量分数是__________g。
(3)根据第1组实验数据计算所用的稀硫酸溶质的质量分数__________(写出计算过程)。
(4)若将第2组实验后的混合物过滤,在滤液中滴加10%的NaOH溶液,请画出在该混合溶液中加入10% NaOH溶液的质量与生成沉淀质量变化关系的曲线图__________。
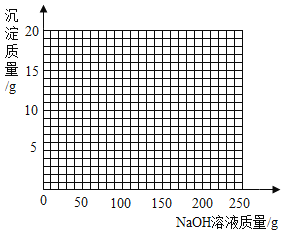
查看答案和解析>>
科目: 来源: 题型:
【题目】小新同学为补充维生素,服用2片21金维他片,该药品部分标签如图所示。请你计算:

(1)小新同学每天补充的维生素C为_______mg。
(2)维生素B2中氢、氧两元素的质量比为_______。
(3)维生素E的相对分子质量为________。
查看答案和解析>>
科目: 来源: 题型:
【题目】化学兴趣小组的同学发现有一瓶氢氧化钠溶液没有塞橡皮塞,在老师指导下,开展了以下探究:
(提出问题1)该氢氧化钠溶液是否变质了呢?
(实验探究1)
实验操作 | 实验现象 | 实验结论 |
取少量该溶液于试管中,向溶液中滴加稀盐酸,并不断振荡。 | 有气泡冒出。 | 氢氧化钠溶液一定变质了。 |
(提出问题2)该氢氧化钠溶液是全部变质还是部分变质呢?
(猜想与假设)猜想1:氢氧化钠溶液部分变质。猜想2:氢氧化钠溶液全部变质。
(查阅资料)(1)氯化钙溶液呈中性。
(2)氯化钙溶液能与碳酸钠溶液反应:CaCl2+Na2CO3=CaCO3↓+2NaCl
(实验探究2)
实验步骤 | 实验现象 | 实验结论 |
(1)取少量该溶液于试管中,向溶液中滴加过量的氯化钙溶液,并不断振荡。 | 有________生成。 | 说明原溶液中一定有碳酸钠。 |
(2)取步骤(1)试管中的少量上层清液,滴加酚酞溶液。 | 溶液变红色。 | 说明原溶液中一定有_________。 |
(实验结论)该氢氧化钠溶液___________(填“部分”或“全部”)变质。
(反思与评价)
(1)氢氧化钠溶液露置于空气中容易变质,发生反应的化学方程式是_______________。
(2)在上述(实验探究2)中,小明提出可用氢氧化钙溶液代替氯化钙溶液,你认为该方案____(填“可行”或“不可行”)。
(理解与应用)氢氧化钠溶液容易变质,必须密封保存。实验室必须密封保存的药品还有很多,试另举一例:_________________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】请根据如图所示装置,回答下列问题:
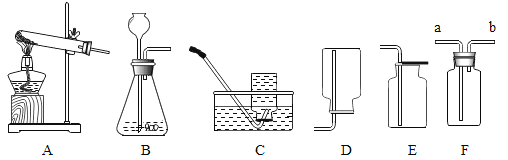
(1)实验室用大理石和稀盐酸反应制取并收集二氧化碳,应选用的装置是________,发生反应的化学方程式是_________________,若使用高锰酸钾制取氧气,还需要对A装置做出的改进是_________________,发生反应的化学方程式是_________________。
(2)下列反应可使用A装置进行实验的是_______。(填序号)
①过氧化氢溶液和二氧化锰制氧气;②一氧化碳还原氧化铁;③木炭还原氧化铜。
(3)装置F可用来收集气体,还具有其他用途,如在F瓶中装入___________,可用来干燥某些气体,若用F收集氧气并测量制得氧气的体积,需在瓶内先装满水,气体从_____________(填“a”或“b”)处导管通入,并需要补充的一种玻璃仪器是___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com