
科目: 来源: 题型:
【题目】物质的用途和使用方法等与其性质密切相关。
(1)铁粉常用于食品的保鲜剂,其原因是________________。
(2)生石灰常用作食品干燥剂,用化学方程式表示其原因是________________。
(3)浓硫酸是无色黏稠液体,有吸水性,在化学实验中常用它作干燥剂,但日常生活中却很少用它作除湿剂,原因是________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】化学与生活生产密切相关。
(1)食盐是常用的调味品和防腐剂,其主要成分的构成粒子是_________(填化学符号)。
(2)铁制品表面涂油、刷漆或镀铬都能防止铁生锈,其原理是_____________________。
(3)干粉灭火器中干粉的主要成分是碳酸氢钠,灭火时其受热分解生成碳酸钠、水和一种能灭火的气体,该反应的化学方程式是________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列四个图象中,能正确反映对应变化关系的是( )
A. 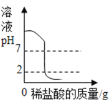 向一定量的氢氧化钠溶液中逐滴加入pH=2的稀盐酸至过量
向一定量的氢氧化钠溶液中逐滴加入pH=2的稀盐酸至过量
B. 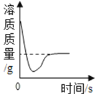 某温度时,向一定量的饱和石灰水中加入少量生石灰
某温度时,向一定量的饱和石灰水中加入少量生石灰
C. 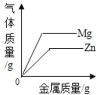 向两份完全相同的稀盐酸中分别加入足量锌粉、镁粉
向两份完全相同的稀盐酸中分别加入足量锌粉、镁粉
D. 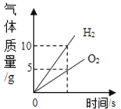 将水通电一段时间
将水通电一段时间
查看答案和解析>>
科目: 来源: 题型:
【题目】a、b、c三种物质的溶解度曲线如图所示。取t2°C的a、b、c三种物质的饱和溶液,分别蒸发等质量的水后恢复至t2°C,再降温到t1°C。下列说法不正确的是
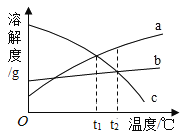
A.降温至t2°C时,三种溶液一定都是饱和溶液
B.原饱和溶液中,溶质的质量分数一定是a>b=c
C.恢复至t2°C时,析出溶质的质量一定是a>b=c
D.降温至t1°C,三种溶液中溶质的质量分数一定是a=c>b
查看答案和解析>>
科目: 来源: 题型:
【题目】在密闭容器中有甲、乙、丙、丁四种物质,在一定条件下反应,测得反应前后各物质的质量分数如图所示。下列说法正确的是( )
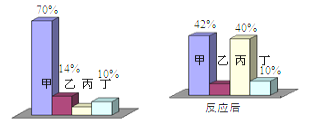
A.丙可能是单质
B.若消耗 3 g 的乙,则生成 17 g 的丙
C.丁一定是该反应的催化剂
D.甲、乙的质量之和一定等于生成丙的质量
查看答案和解析>>
科目: 来源: 题型:
【题目】化学家舍勒和普利斯特里早在![]() 世纪就先后独立地发现了氧气,但由于受“燃素理论”的影响,使他们放弃了自己的研究成果.根据“燃素理论”推知,燃烧后物质的质量应当减轻,但法国化学家拉瓦锡在研究磷以及一些金属燃烧时,做了大量实验,实验结果都与“燃素理论”相违背.他大胆知疑,尊重实验事实,进行深入研究,克服重重阻力,击破了“燃素理论”,真正发现了氧气.通过以上叙述你有何感想________?
世纪就先后独立地发现了氧气,但由于受“燃素理论”的影响,使他们放弃了自己的研究成果.根据“燃素理论”推知,燃烧后物质的质量应当减轻,但法国化学家拉瓦锡在研究磷以及一些金属燃烧时,做了大量实验,实验结果都与“燃素理论”相违背.他大胆知疑,尊重实验事实,进行深入研究,克服重重阻力,击破了“燃素理论”,真正发现了氧气.通过以上叙述你有何感想________?
查看答案和解析>>
科目: 来源: 题型:
【题目】2005年给我们留下了许多深刻的记忆.10月中旬,世界上海拔最高、线路最长,穿越冻土里程也最长的高原铁路–青藏铁路全线铺通;11月13日,中国石油吉化公司双苯厂苯胺装置发生爆炸,造成松花江水体严重污染;11月17日,神六载人航天“多人多天”飞行圆满成功.关于上述事实,下列说法不正确有是( )
A.在运送飞船的火箭推进器中盛有液态肼![]() 和液态双氧水
和液态双氧水![]() ,当它们混合反应时,即产生大量的氮气、二氧化碳和水蒸气,并放出大量的热
,当它们混合反应时,即产生大量的氮气、二氧化碳和水蒸气,并放出大量的热
B.化学给人类带来灾难,应取缔所有的化工厂
C.用于制造钢轨的合金材料–高锰钢,具有很好的韧性和耐磨性
D.尽管青藏高原气候寒冷、空气稀薄,在选择钢轨时仍要注意钢材的防锈功能
查看答案和解析>>
科目: 来源: 题型:
【题目】纯碱是一种重要的工业原料,盐湖中的纯碱常常会含有少量的氯化钠(其它杂质忽略不计)。取6g纯碱样品放在烧杯中并不断滴入稀盐酸,当稀盐酸滴加至35g时,烧杯内溶液的总质量为38.8g(假设产生的气体全部逸出),产生气体的质量与滴入稀盐酸的质量关系如下图所示。请计算:
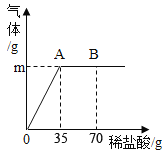
(1)A点产生气体的质量m是_________g。
(2)B点时,烧杯内溶液中的溶质是________(写化学式)。
(3)纯碱样品中碳酸钠的质量分数。(精确到0.1%)
查看答案和解析>>
科目: 来源: 题型:
【题目】研究金属的腐蚀对资源的利用和保护意义重大。
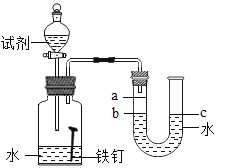
(1)为了探究铁锈蚀的条件,进行如图-12所示实验。经过一周后观察,试管A和C中的铁钉无明显变化,试管B中的铁钉明显锈蚀。
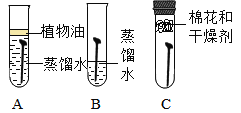
①通过实验发现:铁锈蚀是铁与_____________发生化学反应的过程。
② A中加入的蒸馏水要事先煮沸,其目的是______________________。
(2)家中的刀具若沾有食盐水锈蚀更快。为了进一步探究影响铁锈蚀速率的因素,做了如下的实验。
(提出问题)铁锈蚀速率与哪些因素有关。
(查阅资料)①物质溶解在水中得到的混合物称为水溶液,如氯化钠溶解在水中得到氯化钠溶液,乙醇溶解在水中得到乙醇溶液。
②氯化钠溶液能导电;乙醇溶液不能导电。
(猜想)铁的锈蚀速率与下列因素有关:
①反应时的温度;②氧气的含量;③水溶液的导电性。
(实验)每次取两套如图-13所示的装置,编号为I、II。向两套装置中分别装入质量、大小相同的铁钉和等体积的蒸馏水,进行如下三组对比实验(实验开始时,各瓶内气体压强保持一致)。
影响因素 | 实验设计 | 实验现象 | 实验结论及解释 |
①温度 | 装置I放入25℃恒温环境中,装置II放入40℃恒温环境中。 | 两套装置中铁钉均锈蚀,且U型管中液面均由b处上升至a处,则所需时间I>II。 | 锈蚀的速率I<II;铁的锈蚀速率与反应时的温度有关,_。 |
②氧气含量 |
|
| 铁的锈蚀速率与氧气的含量有关,氧气的含量越多,铁的锈蚀越快。 |
③水溶液的导电性 | 在相同温度下,装置I集气瓶中加入10mL氯化钠溶液;装置II集气瓶中加入10mL乙醇。 | 两套装置中铁钉均锈蚀; |
|
(3)若将两根铁钉分别放入两支试管中,在一支试管中加入稀硫酸,另一支试管中加入稀盐酸,观察到两支试管内均有大量气泡产生,铁钉逐渐溶解,在酸溶液中被快速腐蚀。
(反思与提高)
根据该探究实验以及你所学的知识,判断下列说法正确的是________(填序号)。
A金属的腐蚀是指金属单质与其它物质发生化学反应的过程[
B金属越活泼,就越容易被锈蚀
C金属腐蚀不一定要有氧气参加
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室以MnO2为原料制备少量高纯MnCO3的流程如下:
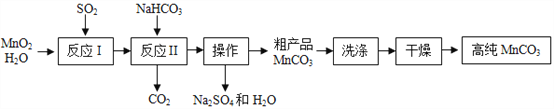
已知:①反应Ⅰ的化学方程式:MnO2+SO2═MnSO4;
②MnCO3、Mn(OH)2均难溶于水,MnCO3在100℃时开始分解.
(1)反应Ⅰ属于基本反应类型中的______________反应.
(2)流程中“操作”的名称为___________,所需要的主要玻璃仪器有__________.
(3)反应Ⅱ的化学方程式为_______________________.反应Ⅱ需控制溶液的酸碱性,若碱性过强,MnCO3粗产品中将混有______________(填化学式).
(4)验证MnCO3粗产品表面附着有Na2SO4杂质:取样品少许,向其中加入水,搅拌、过滤,向滤液中加入适量的______________(填化学式)溶液,有白色沉淀产生.
(5)为获得高纯MnCO3,需选择“低温”干燥的原因是_______________________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com