
科目: 来源: 题型:
【题目】某同学欲测定某石灰石样品中碳酸钙的质量分数。取12.5g石灰石样品于烧杯中,再向其中加入100g稀盐酸,恰好完全反应后,测得烧杯内物质的总质量变为108.1g(假设石灰石中的杂质既不溶于水,也不与其他物质反应,生成的二氧化碳全部逸出)。试计算:

(1)生成的二氧化碳质量为_______g;
(2)该样品中碳酸钙的质量_______;
(3)所用稀盐酸的溶质质量分数_______。
查看答案和解析>>
科目: 来源: 题型:
【题目】为了证明氢氧化钠和稀盐酸反应有新物质生成,兴趣小组的同学进行了下列实验:
(实验目的)证明氢氧化钠溶液与稀盐酸发生了反应且生成了新物质。
(实验原理)___________ (用化学方程式表示)。
(药品仪器)
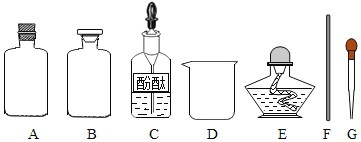
(实验步骤)
①取______(选填“A”或“B”)中试剂加入至D中,滴加2滴酚酞试液,溶液呈红色。
②用G_______(填仪器名称)向①所得的溶液中滴加稀盐酸,直至红色刚好消失。
③向②所得溶液中继续滴加稍过量稀盐酸,溶液保持无色。
④用F蘸取③所得溶液,在酒精灯上灼烧,有白色固体产生。
(思考拓展)
(1)步骤③的目的是:__________。
(2)进一步确认步骤④所得的白色固体不是氢氧化钠,不能选用的试剂有:_________。
ACuSO4溶液 BNa2CO3溶液 C无色酚酞试液 D(NH4)2SO4溶液
(3)已知酚酞试液在不同pH时的变色情况如下表。
pH | <8.2 | 8.2~10.0 | >10.0 |
颜色 | 无色 | 红色 | 无色 |
小文同学发现向某氢氧化钠溶液中滴加酚酞试液, 发现溶液瞬间变红但立即又变成无色,他接着逐滴加入稀盐酸,某一时刻溶液变红了,没有褪色,继续滴加稀盐酸,后褪至无色。小文认为该氢氧化钠溶液刚开始时滴加酚酞试液出现异常现象的原因,可能是氢氧化钠溶液浓度过大导致的,请你设计实验方案帮助他证明猜想:_________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某研究小组对自动充气气球(如下图1所示)进行下列探究。
(查阅资料)该气球充气原理是通过挤破气球内液体包使液体与白色粉末接触产生二氧化碳气体,实现气球自动充气。
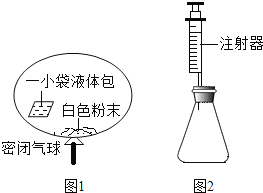
(1)为检验气体是二氧化碳,可选用________(填试剂名称)。
探究一:液体包内溶液酸碱性的探究
(2)室温时,用pH试纸测得溶液pH=3,则该溶液呈酸性。
探究二:白色粉末成分的探究
(猜想与假设)甲同学认为是碳酸钙;乙同学认为是碳酸钠;丙同学认为是碳酸氢钠
(设计并进行实验)
(3)将少量白色粉末放入水中搅拌,固体全部溶解,说明甲同学的猜想_______(填“正确”或“不正确”))。
(4)室温时,分别向盛有碳酸氢钠、碳酸钠和白色粉末样品的锥形瓶中注入等体积、足量的10%的盐酸(装置如上图2所示),记录如下表。
实验编号 | 锥形瓶内物质 | 最终得到CO2的体积/mL | |
物质 | 质量/g | ||
① | 碳酸氢钠 | 0.10 | V1 |
② | 碳酸钠 | 0.10 | V2 |
③ | 白色粉末 | X | V1 |
实验②的化学方程式为___________;表中X =______g;V1________(填“>”“<”或“=”) V2
(5)分析上表实验数据得出的结论及判断依据是_________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下图是实验室常见的制取气体的装置:
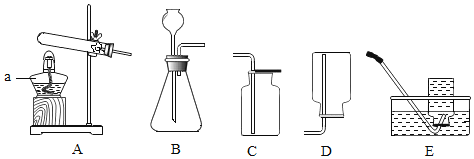
(1)写出上图中带标号a仪器的名称:________;
(2)请写出实验室用B装置制取氧气的化学方程式________,二氧化锰在此实验中的作用是______,可选用C装置收集氧气的原因是_______。
查看答案和解析>>
科目: 来源: 题型:
【题目】向装有等量水的A、B、C三个烧杯中分别加入10g、25g、25 g NaNO3固体,在不同温度下充分溶解后,现象如图1所示。
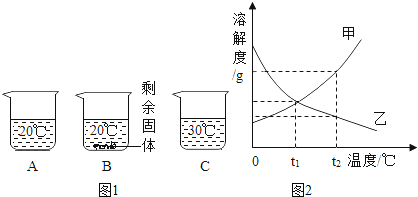
(1)烧杯中的溶液一定属于饱和溶液的是__________(选填“A”、“B”或“C”序号)。
(2)图2中能表示NaNO3溶解度曲线的是____________(填“甲”或“乙”)。
(3)要使B烧杯中剩余的固体继续溶解,可采用的方法是__________。
(4)由上图2分析,若分别将100g甲、乙两物质的饱和溶液从t2℃降温到t1℃,对所得溶液的分析正确的是__________(填序号)。
A甲、乙都是饱和溶液 B所含溶剂质量:甲<乙
C溶液质量:甲>乙 D溶质质量分数:甲>乙
查看答案和解析>>
科目: 来源: 题型:
【题目】生石灰是白色块状固体,生石灰被大量用做建筑材料,也是许多工业的重要原料,在日常生活的应用非常广泛,人类很早就会通过烧制石灰石来获得生石灰,请回答关于生石灰的相关问题:
(1)工业用烧制石灰石的方法获得生石灰,化学反应方程式是_______
(2)日常生活中常用的一种干燥剂,其成分是生石灰,生石灰做干燥剂不可以干燥的气体有__________。
A H2 B O2 C CO2 D HCl E NH3
(3)养鱼的池塘里也会定期洒少量的生石灰粉末,用以减少鱼类疾病的发生,撒入生石灰,池塘水的pH________7。(填“>”“<”或“=”)
查看答案和解析>>
科目: 来源: 题型:
【题目】为确定某固体洗涤助剂成分,兴趣小组进行如下探究:
(查阅资料)
(1)双氧水常用于漂白、消毒、杀菌,但不易保存。洗涤助剂具有相同作用,且易于保存。
(2)制取方法为:将一定量的质量分数为 30%的 H2O2 溶液和 Na2SO4 混合溶解,加入 NaCl,有白色固体析出,过滤得助剂。
(资料分析)由资料(1)可知助剂中一定含______。
(提出猜想)
(1)助剂中含 Na2SO4 和H2O2;(2)助剂中含NaCl 和H2O2;(3)助剂中含_____。
(实验探究)
步骤 1:将少量助剂溶解,向溶液中加入某种黑色粉末,有气泡产生。
步骤 2:另取少量助剂溶解,加热至不再产生气泡;向溶液中加入足量 BaCl2溶液,产生白色沉淀;过滤。
步骤 3:向步骤 2 所得滤液中加入足量AgNO3 溶液,有白色沉淀生成。
(1)步骤 1 反应的化学方程式为______。可用______检验产生的气体。
(2)步骤 2 中将助剂溶液充分加热的目的是______;由该实验可知助剂中存在______。
(3)步骤 3 中白色沉淀为______。
(4)甲同学由步骤 3 得出结论:助剂中含有NaCl;乙同学认为不能得出此结论,理由是_________。
(5)丙同学提出可通过如下方案确定助剂中是否含有 NaCl:将少量助剂溶解,加热至不再有气泡产生。向溶液中加入足量的试剂 X,产生沉淀。过滤,向所得滤液中滴加 AgNO3 溶液。若有白色沉淀,则含有 NaCl。其中试剂X 为______(填对应选项的字母)。
A CaCl2 B Na2CO3 C Ba(NO3)2
(实验结论)猜想 3 正确。
查看答案和解析>>
科目: 来源: 题型:
【题目】南通地铁的正式开建,标志着南通进入“地铁时代”。

(1)地铁列车车体大量使用的镁铝合金属于____________(填“金属材料” 或“合成材料”),镁铝合金的优点是_____________。
(2)地铁建造过程中需要使用大量的钢铁。工业炼铁可利用一氧化碳与氧化铁反应,写出该反应的化学方程___________________。
(3)地铁信息传输系统中使用的光导纤维和电子芯片的关键材料分别为二氧化硅(SiO2)和晶体硅(Si)。将二氧化硅转化为硅的过程属于________________(填“物理变化”或“化学变化”)。
(4)地铁施工过程中产生的废水、废浆以及机械漏油等,都会对水体产生污染。使用活性炭可对污水进行处理,这是利用了活性炭的 __________________性。
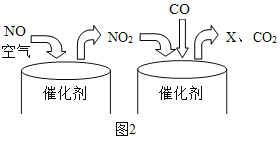
(5)地铁施工工程车的尾气中含 NO、CO。尾气经过如图所示催化转化后,可实现达标排放。写出该反应的化学方程式:____________________,其中发生还原反应的物质为 _______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】我国海水晒盐的历史悠久。粗盐中含有不溶性泥沙、可溶性 CaCl2、MgCl2 等杂质。学习小组设计了如下方案提纯粗盐:
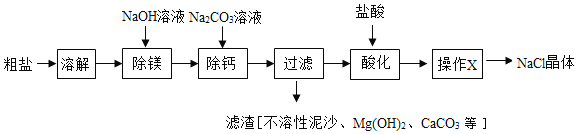
(1)用化学方程式表示 Na2CO3 溶液的作用:______。
(2)“过滤”中玻璃棒的作用为______;“操作 X”的名称为______。
(3)“酸化”过程中有气体生成的反应的化学方程式:______。
(4)酸化时加入过量的盐酸,对氯化钠晶体的纯度无影响,理由是______。
(5)若不考虑实验过程中的损耗,最终所得氯化钠晶体质量______(选填“大于”“等于”、“小于”)粗盐中氯化钠质量。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com