
科目: 来源: 题型:
【题目】通过电解水实验可以研究水的组成。电解水的实验如图所示:
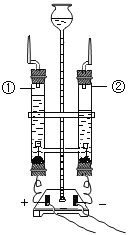
(1)该反应的化学方程式是_______________________。
(2)请从元素守恒角度解释“水是由氢、氧元素组成的”这一实验结论得出的原因:______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】阅读下面科普短文。
2017年,我国在南海北部神狐海域进行的可燃冰试采获得成功。你对可燃冰有多少了解呢?
什么是可燃冰?
可燃冰外观像冰,主要含甲烷水合物(由甲烷分子和水分子组成),还含少量二氧化碳等气体。甲烷水合物的分子结构就像一个一个由若干水分子组成的笼子,每个笼子里“关”一个甲烷分子。
可燃冰是怎样形成的?
可燃冰的形成要满足三个条件:(1)温度不能太高。(2)压力要足够大。(3)要有甲烷气源。在上述三个条件都具备的情况下,天然气可与水生成甲烷水合物,分散在海底岩层的空隙中。
甲烷水合物能稳定存在的压强和温度范围如图所示:
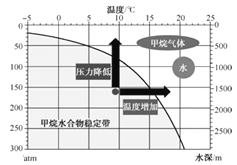
为什么开采困难?
可燃冰开采的最大难点是保证甲烷气体不泄露、不引发温室效应,甲烷引发的温室效应比二氧化碳厉害10至20倍,可燃冰一离开海床便迅速分解,容易发生喷井意外,还可能会破坏地壳稳定平衡,引发海底塌方,导致大规模海啸。
可燃冰有哪些用途?
一体积可燃冰可储载约164倍体积的甲烷气体,具有能量高、燃烧值大等优点,而且储量丰富,因而被各国视为未来石油天然气的替代能源。甲烷还是重要的化工原料,可制造碳黑、乙炔、氰化氢等。
依据文章内容,回答下列问题:
(1)可燃冰形成的适宜条件是_________。
A 高温高压 B 低温高压 C 低温低压
(2)可燃冰作为能源的优点是_________________。
(3)甲烷燃烧的化学方程式为_________________。
(4)有关可燃冰的说法正确的是___________。
A 可燃冰不是冰
B 可燃冰开采时若出现差错,可能引发严重的环境灾害
C 在1atm和25℃时,可燃冰能稳定存在
查看答案和解析>>
科目: 来源: 题型:
【题目】2019年政府工作报告明确今年继续执行新能源汽车购置优惠政策,同时培育新能源汽车产业集群,推动新能源汽车产业发展,是一项非常迫切的任务。太阳能燃料电池是一种零排放、无污染的新能源。

①如图所示,汽车外壳大多使用钢或者铝合金,汽车轮胎使用的是合成橡胶,其中属于金属材料的是___________
A 钢 B 铝合金 C 合成橡胶
②在铜的催化作用下由F2和足量的NH3反应可得到三氟化氮(NF3)和NH4F,三氟化氮在太阳能电池制造中有广泛应用。请写出此反应的化学方程式__________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】工业上利用某废渣(含FeSO4、Fe2(SO4)3及少量CaO和MgO)制备高档颜料铁红(主要成分为Fe2O3)和回收(NH4)2SO4.具体生产流程如下:

(背景信息)
a 氧化还原反应中,会有元素化合价发生变化。
b 3Fe2(SO4)3+12NH3H2O=(NH4)2Fe6(SO4)4(OH)12↓(铵黄铁矾晶体)+5(NH4)2SO4
(1)步骤③中操作Y的名称是_______________。
(2)加入物质X溶解废渣,X应选用______________(填序号)。
A 盐酸 B 硫酸 C 氨水 D 氢氧化钠
步骤①酸浸时,生成盐的化学方程式为___________________________(任写一个)。
(3)步骤②通入氧气氧化的目的是_________________;工业上对该操作控制在4小时左右为宜,根据如图有关数据分析,影响Fe2+氧化率的变化规律:________
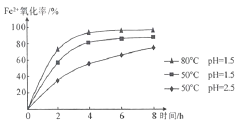
查看答案和解析>>
科目: 来源: 题型:
【题目】某化学兴趣小组在学习金属知识后,对金属钙及其化合物的化学性质非常感兴趣,并进行了以下实验探究。
(1)对金属钙的化学性质进行探究
(提出问题)金属钙能否与水反应?
(实验探究)取一粒金属钙投入盛有50mL水的烧杯中,钙粒与水剧烈反应,四处游动,产生气泡,溶液出现浑浊,用手触摸烧杯外壁,感觉发热。反应结束放置一段时间后,溶液变澄清,往烧杯中滴入无色酚酞试液,溶液变红色。
(实验结论)金属钙能与水反应。经进一步检验,产生的气体能燃烧。请写出钙与水反应的化学方程式___。
(交流与反思)反应结束放置一段时间后,溶液变澄清的原因是___。
(2)对久置于空气中的“生石灰”干燥剂的组成成分及含量进行探究
(查阅资料)Ca(OH)2加热到一定温度时会发生分解反应,生成两种氧化物。
(实验探究)该小组称取10.0g干燥剂样品于控温电加热器中,按如图所示装置进行实验(装置气密性良好,装置A、B、C中药品足量,实验操作正确)
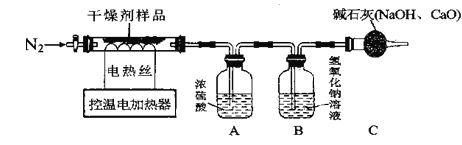
(实验数据记录)充分反应后,产物被完全吸收,A装置增重0.9g,B装置增重2.2g
(分析与结论)该包干燥剂的成分有____(填化学式),其中Ca(OH)2的质量为___g。
(反思与拓展)
①停止加热后,需要通入N2一段时间的目的是___。
②若没有C装置,会导致含量测定结果偏小的成分是___。
查看答案和解析>>
科目: 来源: 题型:
【题目】葡萄的果肉和果皮中都含有丰富的营养物质。
(1)用硫酸铜配制的农药波尔多液,可以防治葡萄生长中的病害。溶解硫酸铜时不宜用铁制容器,用化学方程式表示其原因: _____________________。
(2)食用葡萄前要清洗干净,如图是一种清洗的方法。
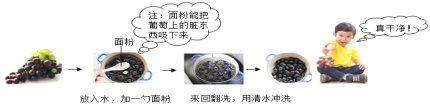
下列说法正确的是______________(填序号)。
A 面粉有利于去除葡萄皮上的脏东西
B 清洗干净后,建议吃葡萄不吐葡萄皮
C 葡萄富含糖类物质,糖尿病人不宜多食
查看答案和解析>>
科目: 来源: 题型:
【题目】鲜度保持卡(如图)以纸片为载体,以食用酒精(C2H5OH)和柠檬酸为原料制成。经常用于蛋糕、面包、月饼等食品包装内,能在被保鲜食品的周围形成一定浓度的气相保护层,从而达到保鲜的目的。

(1)酒精属于__________(填字母序号)。
A 单质 B 氧化物 C 化合物 D 有机物 E 纯净物
(2)酒精挥发形成气体保护层的过程其微观原因是:_____________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】为探究影响铁和盐酸反应速率的因素,兴趣小组利用传感器测定氢气浓度随时间的变化,如下表所示。每一个实验在其他条件不变时,下列说法不正确的是
图象 |
|
|
|
实验 | 等质量的铁丝、铁粉分别与相同浓度的盐酸反应 | 等质量的铁粉分别与不同浓度的盐酸(3%和15%)反应 | 不同温度下,等质量的铁粉与相同浓度的足量稀盐酸反应 |
A.由图1可知:盐酸不能与铁丝反应
B.由图1可得结论:铁粉反应更快
C.由图2可知3%的盐酸与铁粉反应更快
D.由图3所示实验可知温度不影响生成氢气的总质量
查看答案和解析>>
科目: 来源: 题型:
【题目】如图是a、b两种固体物质的溶解度曲线,下列说法中不正确的是( )
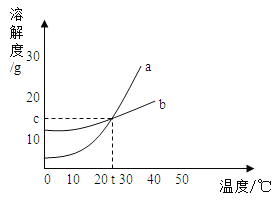
A.a的溶解度大于b的溶解度
B.在t℃时,a、b饱和溶液中溶质的质量分数相同
C.当a中含有少量b时,可以用降温结晶法提纯a
D.a,b都属于易溶物质
查看答案和解析>>
科目: 来源: 题型:
【题目】某化学兴趣小组为探究化学反应中的能量变化,进行以下实验:
(探究一)盐酸与氢氧化钠的反应
(1)写出氢氧化钠溶液与盐酸反应的化学方程式:_________________________________。
(2)甲同学设计实验:向一定量氢氧化钠固体中倒入20mL 4%盐酸,用温度计测量反应前后各溶液的温度。乙同学认为该实验方案不合理,其理由是_________________________。
(3)丙同学设计了如下三组实验,请你帮助他完成实验方案:
实验编号 | 实验方案 |
实验1 | 向20mL 4%盐酸中倒入20mL水,测定稀释前后溶液的温度。 |
实验2 | 向20mL 5%氢氧化钠溶液中________________,测定稀释前后溶液的温度。 |
实验3 | _______________________________________________________________。 |
(4)丙同学观察到的实验现象是:实验3溶液升高的温度远大于实验1与实验2溶液升高的温度之和,由此你能得出的实验结论是①____________;②____________。
(探究二)盐酸与碳酸氢钠溶液的反应。
下图是丁同学在20℃、基本隔热条件下利用温度传感器,分别测定向20mL水和20mL饱和碳酸氢钠溶液中各倒入20mL 13.7%盐酸的温度与时间变化曲线。
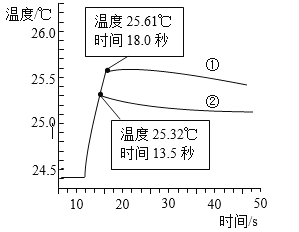
曲线①为水+13.7%盐酸温度变化曲线
曲线②为饱和碳酸氢钠溶液+13.7%盐酸温度变化曲线
实验测得饱和碳酸氢钠溶液稀释时温度变化不大,可忽略不计,据此回答下列问题:
(5)18.0秒后,曲线①逐渐下降的原因是____________________________________;
(6)比较曲线①和曲线②,你认为13.7%盐酸与饱和碳酸氢钠溶液的反应是________(填“放热”或“吸热”)反应,其理由是_________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com