
【题目】亚硝酸钠(NaNO2)在纤维纺织品的染色和漂白、照相、生产橡胶、制药等领域有广泛应用,也常用于鱼类、肉类等食品的染色和防腐。但因其有毒,所以在食品行业中的用量有严格限制。现用下图所示仪器(夹持装置已省略)及药品,探究亚硝酸钠与硫酸反应及气体产物的成分。
已知:① NO+NO2+2OH-===2NO![]() +H2O;
+H2O;
② 气体液化的温度:NO2为21 ℃,NO为-152 ℃。
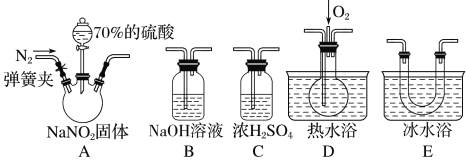
(1) 为了检验装置A中生成的气体产物,仪器的连接顺序(按左→右连接)为A、C、________、______、______。
(2)反应前应打开弹簧夹,先通入一段时间氮气,排除装置中的空气,目的是___________________。
(3) 在关闭弹簧夹、打开分液漏斗活塞、滴入70%硫酸后,A中产生红棕色气体。
① 确认A中产生的气体含有NO,依据的现象是___________________________。
② 装置E的作用是_____________________________。
(4) 如果向D中通入过量O2,则装置B中发生反应的化学方程式为______________________。
(5) 通过上述实验探究过程,可得出装置A中反应的化学方程式是______________。
【答案】(1)E D B
(2) 防止可能产生的NO被氧化成NO2,造成对A中反应产物检验的干扰
(3) ①装置D中通入氧气后出现红棕色气体 ②冷凝,使NO2完全液化
(4) 4NO2+O2+4NaOH===4NaNO3+2H2O
(5) 2NaNO2+H2SO4===Na2SO4+NO2↑+NO↑+H2O
【解析】(1)根据NO、NO2的液化温度和性质可知装置D用于检验NO,装置E用于检验并分离NO2,装置B为尾气处理装置,NO2会干扰NO的检验,所以为了检验装置A中的气体产物,仪器的连接顺序是A、C、E、D、B。(2)由于NO极易被空气中的氧气氧化为NO2,所以先通入一段时间氮气,排除装置中的空气,防止可能产生的NO被氧化成NO2,造成对A中反应产物检验的干扰。(3)①利用装置D检验NO。开始时装置D中无色,通入氧气后出现红棕色气体即可证明NO的存在。②装置E的作用是降温冷凝,使NO2完全液化,避免干扰NO的检验。(4)因为NO2、O2和水共同作用可以产生HNO3,所以装置B中发生反应的化学方程式为4NO2+O2+4NaOH===4NaNO3+2H2O。(5)装置A中发生反应的化学方程式是2NaNO2+H2SO4===Na2SO4+NO2↑+NO↑+H2O。


科目:高中地理 来源: 题型:
【题目】市场上有一种加酶洗衣粉,即在洗衣粉中加入少量的碱性蛋白酶,它的催化活性很强,衣服的汗渍、血液及人体排放的蛋白质油渍遇到它,皆能水解除去,下列衣料中不能用加酶洗衣粉洗涤的是( )
①棉织品 ②毛织品
③腈纶织品 ④蚕丝织品
⑤涤纶织品 ⑥锦纶织品
A.①②③④⑤⑥ B.②④
C.③④⑤ D.③⑤⑥
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】(2016·嘉兴一中期中)下图为“某区域某种工业企业、人口密度、人均GDP分布示意图”。读图,回答下列问题。
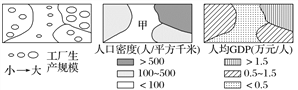
【1】该企业最可能是
A. 制糖厂 B. 啤酒厂
C. 钢铁厂 D. 电子装配厂
【2】图中甲区域第三产业所占比重超过70%,影响其发展的主导区位条件是
A. 交通便利 B. 边境贸易发达
C. 环境优美 D. 科技发达
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】阅读材料,完成下列问题。
材料一:2016年1月28日,首列“义乌—德黑兰”货运班列从浙江义乌发车,运载从义乌出口到伊朗的商品,跨过10399公里的距离抵达伊朗德黑兰,比传统海运节省了一半的时间。
材料二:左图为亚洲区域图和右图为伊朗首都德黑兰气候资料图。
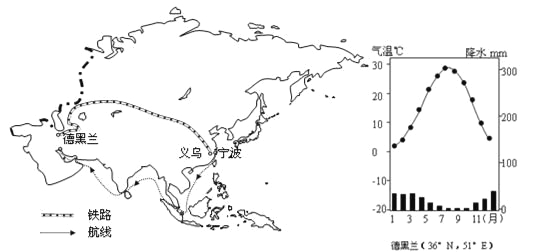
(1)义乌气候类型是 ,成因是 。
(2)据图写出德黑兰的降水特点 、 。
(3)货轮从宁波起航开往伊朗,航行至北印度洋时,正好是顺风顺流,此季节该地盛行 风,北印度洋洋流呈 (顺或逆)时针流动。
(4)中国与伊朗贸易互补性强,中国可以从伊朗进口的商品有 、 。
(5)简述义乌成为全球最大的小商品集散中心的区位条件。
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】阅读材料,回答问题。
2015年6月10日开始,江南、华南、西南地区东部等地先后出现大到暴雨,部分地区有大暴雨。强降雨导致福建、江西、湖南、广西、贵州等省份遭受洪涝风雹灾害,逾60万人受灾。据江西省民政厅报告,作物受灾面积20.5千公顷,其中绝收2千公顷,直接经济损失1.5亿元。

请分析6月初湘鄂黔等地区造成较大损失的洪涝灾害的成因。
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】某学习兴趣小组探究氨气的制取实验:
(1) 甲同学拟用下列实验方法制备氨气,其中合理的是________(填字母)。
A.将氯化铵固体加热分解收集产生的气体
B.将浓氨水滴入氢氧化钠固体中,收集产生的气体
C.将碳酸氢铵加热分解产生的气体用碱石灰干燥
D.将氯化铵稀溶液滴入氢氧化钠固体中,收集产生的气体
(2) 根据上述正确的原理,该同学欲用下列常见的实验室制气装置制取氨气,适宜的装置是________。
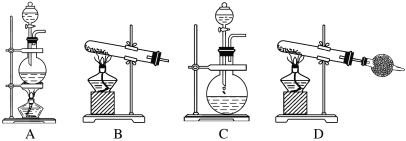
(3) 气体的性质是气体收集方法选择的主要依据。下列性质与收集方法无关的是____________(填序号)。
① 密度 ② 颜色 ③ 溶解性 ④ 热稳定性 ⑤ 与氧气反应
(4) 下图是甲同学设计收集氨气的几种装置,其中可行的是________,集气的原理是_____________________________________。
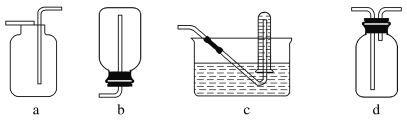
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】下列物质的分类正确的是
选项 | 碱 | 酸 | 盐 | 碱性氧化物 | 酸性氧化物 |
A | Na2CO3 | H2SO4 | NaOH | SO2 | CO2 |
B | NaOH | HCl | NaCl | Na2O | NO |
C | KOH | HNO3 | CaCO3 | CaO | Mn2O7 |
D | NaOH | HCl | CaF2 | Na2O2 | SO2 |
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】A~F六种元素中,除F外其他均为短周期元素,它们的原子结构或性质如下表所示。
元素 | 原子结构或性质 |
A | 其形成的一种同位素原子在考古中可推测化石的年代 |
B | 与A同周期,其最高价氧化物的水化物无论浓、稀溶液均有强氧化性 |
C | 地壳中含量最多的元素 |
D | D原子的内层电子数是最外层电子数的5倍 |
E | 其单质主要存在于火山口附近 |
F | 生活中常见的金属,它有两种常见的氯化物,且相对分子质量相差35.5 |
请回答下列问题:
(1)A在元素周期表中的位置是_______________;A与C形成的化合物AC2的电子式是__________。
(2) 下列事实能证明C和E的非金属性强弱的是 。(填序号)
①常温下,C的单质呈气态,E的单质呈固态
②C的气态氢化物的稳定性强于E的气态氢化物的稳定性
③C与E形成的化合物中,E呈正价
④E的氢化物的沸点高于C的氢化物的沸点
(3) 由A、B、C和氢元素四种元素所形成的阴、阳离子数目之比为1:1的离子化合物是 (填化学式),它与足量NaOH溶液在加热时反应的离子方程为: 。
(4) FC与足量B的最高价氧化物的水化物的稀溶液反应的离子方程式 。若有标准状况下5.6L的BC生成,则转移的电子数为 。
(5) A的氢化物有多种,1 mol A的某种氢化物分子中含有14 mol电子,已知在25℃、101kPa下,1g该氢化物在足量氧气中完全燃烧生成液态水时放出的热量为40 kJ,写出表示该氢化物燃烧热的热化学方程式: 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com