
【题目】下列说法正确的是
A.金属氧化物一定是碱性氧化物
B.碱性氧化物一定是金属氧化物
C.非金属氧化物一定是酸性氧化物
D.酸性氧化物一定是非金属氧化物
科目:高中地理 来源: 题型:
【题目】下图表示几种自然灾害的持续时间,读图完成下列各题。
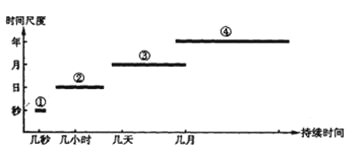
【1】①②③④四种灾害分别是
A.火山、地震、干旱、洪涝
B.地震、火山、洪涝、干旱
C.干旱、洪涝、地震、火山
D.火山、地震、洪涝、干旱
【2】蝗虫是危害严重的生物灾害。图中所示的自然灾害中,与其发生密切相关的是
A.①② B.②④ C.①②③ D.③④
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】洗车指数是根据过去12小时和未来48小时有无雨雪天气,路面是否有积雪和泥水,是否容易使汽车溅上泥水,是否有沙尘等天气条件,给爱车族提供是否适宜洗车的气象指数。洗车指数共分为4级,级数越高,就越不适宜洗车。读“2015年4月6日17时某区域地面天气图”,完成下列各题。
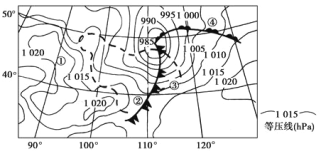
【1】图中①②③④四地,洗车指数数值最低的是( )
A.① B.② C.③ D.④
【2】如果图中等压线状况维持不变,某自驾游汽车从②地经③地到④地,天气变化可能是( )
A.气温:暖→冷→暖 B.气压:低→高→低
C.降雨:晴→雨→晴 D.风向:西北风→西南风→东南风
【3】关于图示虚线范围内可能出现的气象灾害的成因,叙述正确的是( )
A.冷气团过境,气温骤降 B.冷锋锋后,带来强降水
C.冷锋过境,风力强劲,扬起沙石 D.高压系统控制,降水偏少
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】某100 mL混合酸中,HNO3物质的量浓度为0.4 mol/L,H2SO4物质的量浓度为0.2 mol/L。向其中加入2.56 g Cu粉,待充分反应后(反应前后溶液体积变化忽略不计),溶液中Cu2+的物质的量浓度为( )
A.0.15 mol/L B.0.3 mol/L
C.0.225 mol/L D.无法计算
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】A、B、C、D、E、X是中学常见的无机物,存在如图转化关系(部分生成物和反应条件略去)。
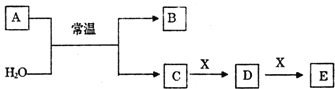
(1)若A为常见的金属单质,焰色反应呈黄色,X能使品红溶液褪色,写出C和E反应的离子方程式:__________________。
(2)若A为短周期元素组成的单质,该元素的最高价氧化物的水化物酸性最强,则:
①组成单质A的元素在周期表中的位置为______________.
②X可能为__________(填代号)。
a.NaHCO3 b.Na2CO3 c.Na2SO3 d.Al(OH)3
(3)若A为淡黄色粉末,回答下列问题:
①1molA与足量的H2O充分反应时转移的电子数目为__________。
②A中所含有的化学键类型为___________________。
③若X为一种造成温室效应的气体.则鉴别等浓度的D、E两种溶液,可选择的试剂为__________(填代号)。
a.盐酸 b.BaCl2溶液 c.NaOH溶液 d.Ca(OH)2溶液
(4)若A为氧化物,X是Fe,溶液D中加入KSCN溶液变红。则A与H2O反应的化学反应方程式为______________,E是________________(填化学式)。
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】读“城市化速度随时间的变化图”,回答下列问题。
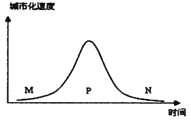
【1】关于图中各个时段城市化特点的叙述,正确的是
A.在M时段,城市化发展较快
B.在P时段,城市化水平较髙
C.在N时段,城市化水平较高
D.在N时段,人口向城市迅速集聚
【2】中国和英国分别处于图中的时段是
A.P、N B.N、P C.M、N D.P、M
【3】在P时段,一定不会出现的城市问题是
A.市区内平均行车速度明显下降 B.雾霾发生频率明显增加
C.大量人口从市区迁移到郊区 D.城市内涝严重
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】已知液态氯化氢和氯化钠固体均不能导电。下列物质中含有自由移动的Cl-的是
A.KClO3溶液 B.KCl溶液 C.液态HCl D.NaCl固体
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】研究硫元素及其化合物的性质具有重要意义。
(1)①硫离子的结构示意图为 。
②加热时,硫元素的最高价氧化物对应水化物的浓溶液与木炭反应的化学方程式为 ____ 。
(2)25℃,在0.10mol·L-1H2S溶液中,通入HCl气体或加入NaOH固体以调节溶液pH,溶液pH与c(S2-) 关系如图(忽略溶液体积的变化、H2S的挥发)。
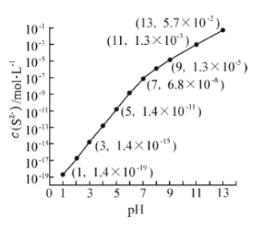
①pH=13时,溶液中的c(H2S)+c(HS-)= mol·L-1.
②某溶液含0.020 mol·L-1Mn2+、0.10 mol·L-1H2S,当溶液pH= 时,Mn2+开始沉淀。[已知:Ksp(MnS)=2.8×10-13]
(3) 25℃,两种酸的电离平衡常数如右表。
Ka1 | Ka2 | |
H2SO3 | 1.3×10-2 | 6.3×10-4 |
H2CO3 | 4.2×10-7 | 5.6×10-11 |
①HSO3-的电离平衡常数表达式K= 。
②0.10 mol·L-1Na2SO3溶液中离子浓度由大到小的顺序为 。
③H2SO3溶液和NaHCO3溶液反应的主要离子方程式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com