
【题目】A、B、C、D、E、X是中学常见的无机物,存在如图转化关系(部分生成物和反应条件略去)。
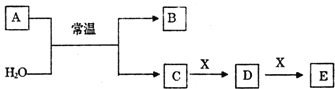
(1)若A为常见的金属单质,焰色反应呈黄色,X能使品红溶液褪色,写出C和E反应的离子方程式:__________________。
(2)若A为短周期元素组成的单质,该元素的最高价氧化物的水化物酸性最强,则:
①组成单质A的元素在周期表中的位置为______________.
②X可能为__________(填代号)。
a.NaHCO3 b.Na2CO3 c.Na2SO3 d.Al(OH)3
(3)若A为淡黄色粉末,回答下列问题:
①1molA与足量的H2O充分反应时转移的电子数目为__________。
②A中所含有的化学键类型为___________________。
③若X为一种造成温室效应的气体.则鉴别等浓度的D、E两种溶液,可选择的试剂为__________(填代号)。
a.盐酸 b.BaCl2溶液 c.NaOH溶液 d.Ca(OH)2溶液
(4)若A为氧化物,X是Fe,溶液D中加入KSCN溶液变红。则A与H2O反应的化学反应方程式为______________,E是________________(填化学式)。
【答案】(1)OH﹣+HSO3﹣=SO32﹣+H2O
(2)①第三周期第VIIA族 ②bc
(3)①NA ②离子键、共价键 ③ab
(4)3NO2+H2O=2HNO3+NO Fe(NO3)2
【解析】(1)若A为常见的金属单质,焰色反应呈黄色,应为Na,X能使品红溶液褪色,应为SO2,则B为H2,C为NaOH,D为Na2SO3,E为NaHSO3,C和E反应的离子方程式为OH﹣+HSO3﹣=SO32﹣+H2O;
(2)若A为短周期元素组成的单质,该元素的最高价氧化物的水化物酸性最强,应为Cl2,则B为HClO,C为HCl。①Cl原子核外有3个电子层,最外层电子数为7,位于周期表第三周期ⅦA族;
②C为盐酸,可与NaHCO3反应生成CO2,但CO2与NaHCO3不反应,a错误;与Na2CO3反应生成CO2,CO2与Na2CO3反应可生成NaHCO3,b正确;与Na2SO3反应生成SO2,SO2与Na2SO3反应可生成NaHSO3,c正确;盐酸与氢氧化铝反应生成氯化铝,氯化铝与氢氧化铝不反应,d错误,答案选bc;
(3)若A为淡黄色粉末,应为Na2O2。①1molA与足量的H2O充分反应时过氧化钠自身发生氧化还原反应,转移的电子数目为NA;
②A为Na2O2,所含有的化学键类型为离子键、共价键;
③若X为一种造成温室效应的气体,应为CO2,则C为NaOH,D为Na2CO3,E为NaHCO3,鉴别等浓度的D、E两种溶液,可用盐酸或氯化钡溶液,答案选ab;
(4)若A为氧化物,X是Fe,由转化关系可知C具有强氧化性,则A为NO2,B为NO,C为HNO3,NO2与水反应的方程式为3NO2+H2O=2HNO3+NO;C为HNO3,硝酸与铁反应生成硝酸铁,硝酸铁与铁反应生成硝酸亚铁,E为硝酸亚铁,化学式为Fe(NO3)2。


科目:高中地理 来源: 题型:
【题目】落户湖北省黄石市黄石港区江北工业园的中国-东盟北斗科技城(左图),计划建成面向全球、特别是以泰国、马来西亚等国家为主的东盟地区,集北斗应用和服务产业体系、北斗产业孵化体系、科技体验和休闲观光体系、国际高端学术交流和技术外包服务体系等为一体的科技城(右图)。据此完成下列各题。
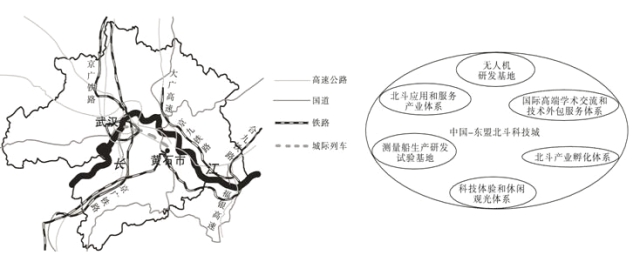
【1】测量船研发基地和无人机研发基地进入该科技城有利于
A.共同利用公共服务 B.及时把握研发动态
C.共同处理废弃物质 D.开拓产品销售市场
【2】中国-东盟北斗科技城的建设,有利于湖北省
A.提高城市化水平 B.开发能源矿产资源
C.缩小城乡间差异 D.促进产业结构升级
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】三支体积相等的试管分别充满相同状态下气体:①氨气;②体积比为4∶1的NO2和O2气体;③NO2气体;将他们分别倒立于盛有足量水的水槽中,液面恒定后(假设试管内液体不扩散),则下列结论正确的是( )
A.①和③试管内溶液的体积不等,溶质的物质的量浓度也不相等
B.因为它们都可溶于水,所以液面都上升到试管顶部
C.三支试管中,试管②中溶液中溶质的物质的量浓度最小
D.试管②和试管③中溶液的溶质的物质的量浓度一定相等
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】We thought of selling this old furniture,but we decided to___it.It might be valuable
A.hold on to
B.keep up with
C.turn to
D.look after
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】下列说法正确的是
A.金属氧化物一定是碱性氧化物
B.碱性氧化物一定是金属氧化物
C.非金属氧化物一定是酸性氧化物
D.酸性氧化物一定是非金属氧化物
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】A、B、C、D均为短周期元素。A、B可形成两种液态化合物甲和乙,其最简式分别为BA和B2A。A与D可形成气态化合物DA、DA2。B与D可形成一种极易溶于水的碱性气体X。B与C可形成极易溶于水的酸性气体Y。Y溶于水能完全电离。已知X分子与乙分子中的电子数相等,Y分子与甲分子中的电子数相等。请回答:
(1)甲的电子式为___________。
(2)常温下,aL pH为2的Y溶液与bL pH为12的氢氧化钠溶液混合后,所得溶液pH=3,则a:b=___________。
(3)X溶于水后发生电离,写出电离方程式____________,已知X在液态时和水一样,可发生微弱的电离,产生两种含相同电子数的粒子。请写出它的电离方程式:___________。
(4)X与甲在一定条件下可发生反应,生成无污染的产物,写出反应的化学方程式_________。
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】下图为某地等高线地形图,读图回答下列各题。
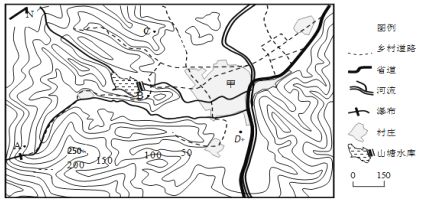
【1】甲村著名的古建筑旅游景点,某旅游者想拍摄一张该村的全景照,正确的拍摄地点和理由是( )
A.A点 海拔较高,适宜远眺 B.B点 距离较近,身临其境
C.C点 视线通透,俯视全村 D.D点 地形平坦,视野开阔
【2】图中地势相差最大可能是( )
A.449米 B.499米 C.549米 D.599米
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】阅读材料,回答下列问题。
材料一、2014年10月29日,国务院印发《关于调整城市规模划分标准的通知》。新的城市规模划分标准以城区常住人口为统计口径,将城市划分为五类七档。
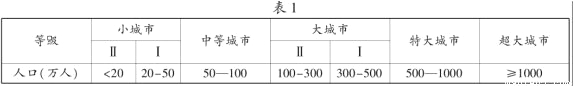
材料二、下图为某年江苏省城市地价及省辖市中心城市常住人口示意图。
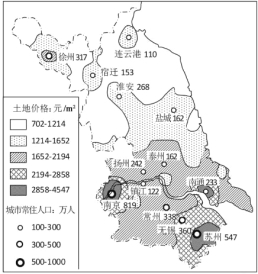
(1)按新的城市规模划分标准,江苏省13个省辖市可分为_____ 类_____档,其中特大城市有_____个。
(2)江苏省各城市地价空间分布的大致趋势是_______________________,影响其形成的最主要因素是_______________________。
(3)图中有三个地价高值区,从城市职能看,南京为__________,从接受大城市辐射看,苏州为__________,从交通区位看,南通濒江达海,所以地价较高。
(4)从地价因素考虑,江苏省内工业为降低生产成本,可能由_________向__________转移。
查看答案和解析>>
科目:高中地理 来源: 题型:
【题目】联氨(又称肼,N2H4,无色液体)是一种应用广泛的化工原料,可用作火箭燃料,回答下列问题:
(1)联氨分子的电子式为_____________,其中氮的化合价为____________。
(2)实验室可用次氯酸钠溶液与氨反应制备联氨,反应的化学方程式为___________。
(3)①2O2(g)+N2(g)=N2O4(l) ΔH1
②N2(g)+2H2(g)=N2H4(l) ΔH2
③O2(g)+2H2(g)=2H2O(g) ΔH3
④2 N2H4(l) + N2O4(l)= 3N2(g)+ 4H2O(g) ΔH 4=-1048.9kJ/mol
上述反应热效应之间的关系式为ΔH4=________________,联氨和N2O4可作为火箭推进剂的主要原因为_____________________________。
(4)联氨为二元弱碱,在水中的电离方程式与氨相似,联氨第一步电离反应的平衡常数值为___________________(已知:N2H4+H+![]() N2H5+的K=8.7×107;KW=1.0×10-14)。联氨与硫酸形成的酸式盐的化学式为 。
N2H5+的K=8.7×107;KW=1.0×10-14)。联氨与硫酸形成的酸式盐的化学式为 。
(5)联氨是一种常用的还原剂。向装有少量AgBr的试管中加入联氨溶液,观察到的现象___________。联氨可用于处理高压锅炉水中的氧,防止锅炉被腐蚀。理论上1kg的联氨可除去水中溶解的O2___________kg;与使用Na2SO3处理水中溶解的O2相比,联氨的优点是___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com