
| A. | H2O的结构式:H-O-H | B. | 乙烯的结构简式为CH2CH2 | ||
| C. | CO2的比例模型: | D. | 丙烯的电子式: |
分析 A.水中含有氢氧共价键;
B.碳碳双键为官能团,不能省略;
C.比例模型表示原子的相对大小及原子连接顺序、空间结构;
D.丙烯分子中含有6个氢原子,分别与3个碳形成6个C-H,三个碳中形成1个C-C,1个C=C.
解答 解:A.1个水分子中含有2个氢氧共价键,结构式为H-O-H,故A正确;
B.乙烯的结构简式为CH2=CH2,故B错误;
C.二氧化碳的分子式为CO2,由模型可知小球为碳原子,2个大球为氧原子,氧原子半径大,实际碳原子半径大于氧原子半径,故C错误;
D.图中丙烯分子中漏掉1个氢原子,故D错误;
故选:A.
点评 本题考查了常用化学用语,难度不大,加强基础知识的掌握理解,注意有机物中官能团不能省略.


科目:高中化学 来源: 题型:选择题
| A. | MnO 2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$ MnCl 2+Cl 2↑+2H 2O | |
| B. | K 2Cr 2O 7+6FeSO 4+7H 2SO 4═Cr 2(SO 4) 3+3Fe 2(SO 4) 3+K 2SO 4+7H 2O | |
| C. | 2Al+2NaOH+2H 2O═2NaAlO 2+3H 2↑ | |
| D. | 2KMnO 4+HCOOK+KOH═2K 2MnO 4+CO 2↑+H 2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 25 | B. | 20 | C. | 16 | D. | 9 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 铈、铬、钛、镍虽不是中学阶段常见的金属元素,但在工业生产中有着重要作用.
铈、铬、钛、镍虽不是中学阶段常见的金属元素,但在工业生产中有着重要作用.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| 选项 | X | Y | Z | W |  |
| A | Cu[ | CuSO4[来 | Cu(OH)2 | CuO | |
| B | Na | NaOH | NaCl | NaHCO3 | |
| C | 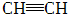 | CH2=CH2 | CH3CH3 | CH3CH2Cl | |
| D | Mg | MgO | MgSO4 | MgCl2 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳酸的电离:H2CO3?H++HCO3- | |
| B. | 将金属钠放入水中:Na+2H2O=Na++2OH-+H2↑ | |
| C. | 碳酸钠水解:CO32-+2H2O?H2CO3+2OH- | |
| D. | 向氯化铝溶液中加入过量的烧碱溶液:Al3++3OH-=Al(OH )3↓ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com