
【题目】按官能团的不同,可以对有机物进行分类,请指出下列有机物的种类,填在横线上。
(1)CH3CH2CH2COOH________,
(2)HCOOC2H5________,
(3)CH3CH2CH2CH2Cl________,
(4)CH3CHO________,
(5)![]() _________,
_________,
(6)![]() _________,
_________,
(7)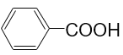 _________,
_________,
(8)CH3CH2CH=CHCH3_________。
【答案】羧酸 酯 卤代烃 醛 芳香烃 酚 羧酸 烯烃
【解析】
根据烃和烃的衍生物的官能团可确定有机物的种类,常见有机物有烷烃、烯烃、炔烃、卤代烃、醇、酚、醛、羧酸、酯、氨基酸等,结合有机物的结构简式判断有机物的种类。
(1)CH3CH2CH2COOH的官能团为羧基,属于羧酸,故答案为:羧酸;
(2)![]() 分子中含有酯基,属于酯,故答案为:酯;
分子中含有酯基,属于酯,故答案为:酯;
(3)CH3CH2CH2CH2-Cl的官能团为氯原子,属于卤代烃,故答案为:卤代烃;
(4)CH3CHO的官能团为醛基,属于醛,故答案为:醛;
(5)![]() 为乙苯,分子中不含官能团,含有苯环,属于芳香烃,故答案为:芳香烃;
为乙苯,分子中不含官能团,含有苯环,属于芳香烃,故答案为:芳香烃;
(6)![]() 的官能团为羟基,直接连接在苯环上,属于酚,故答案为:酚;
的官能团为羟基,直接连接在苯环上,属于酚,故答案为:酚;
(7)![]() 的官能团为羧基,属于羧酸,含有苯环,也属于芳香酸,故答案为:羧酸(或芳香酸);
的官能团为羧基,属于羧酸,含有苯环,也属于芳香酸,故答案为:羧酸(或芳香酸);
(8)CH3CH2CH=CHCH3的官能团为碳碳双键,为烃类,属于烯烃,故答案为:烯烃。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】元素![]() 、
、![]() 、
、![]() 在周期表中的相对位置如图所示。已知
在周期表中的相对位置如图所示。已知![]() 元素原子的外围电子排布式为
元素原子的外围电子排布式为![]() ,则下列说法不正确的是( )
,则下列说法不正确的是( )

A.![]() 元素原子的价电子排布式为
元素原子的价电子排布式为![]()
B.![]() 元素在元素周期表的第三周期第ⅥA族
元素在元素周期表的第三周期第ⅥA族
C.![]() 元素所在周期中所含非金属元素最多
元素所在周期中所含非金属元素最多
D.![]() 元素原子的核外电子排布式为
元素原子的核外电子排布式为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知CH4(g)+2O2(g)→CO2(g)+2H2O(g) ΔH== - Q1 ;
2H2(g)+O2(g) →2H2O(g) ΔH== - Q2;
H2O(g) →H2O(l) ΔH== - Q3
常温下,取体积比为4:1的甲烷和H2的混合气体112L(标准状况下),经完全燃烧后恢复到常温,则放出的热量为
A.4Q1+0.5Q2B.4Q1+Q2+10Q3C.4Q1+2Q2D.4Q1+0.5Q2+9Q3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汽车内燃机燃烧时,在高温引发氮气和氧气反应会产生 NOx 气体,NOx 的消除是科研人员研究的重要课题。
(1)通过资料查得 N2(g)+O2(g)2NO(g)△H反应温度不平衡常数的关系如下表:
反应温度/℃ | 1538 | 2404 |
平衡常数 |
|
|
则△H___________________0(填“<”“>”戒“=”)
(2)在 800℃时,测得 2NO(g)+O2(g) 2NO2(g)的反应速率不反应物浓度的关系如下表所示
初始浓度/ | 初始速率/ | |
C0(NO) | C0(O2) | |
0.01 | 0.01 |
|
0.01 | 0.02 |
|
0.03 | 0.02 |
|
已知反应速率公式为 V 正=K 正×c m(NO)cn(O2),则 m=___________________, K 正=___________________L2mol-2s-1
(3)在某温度下(恒温),向体积可变的容器中充人 NO2 气体,发生反应 2NO2(g) N2O4(g),气体分压随时间的变化关系如图
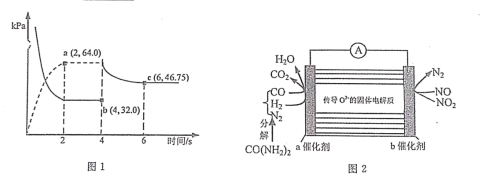
①该反应的压力平衡常数 KP=___________________。
②4s 时压缩活塞(活塞质量忽略不计)使容器体积变为原体积的 1/2,6s 时重新达到平衡,则P(N2O4)=___________________kPa。
(4)某学习小组利用图 2 装置探究向汽车尾气中喷入尿素溶液处理氮的氧化物。则该装置工作时,NO2 在 b 电极上的电极反应式为___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】写出下列物质的名称:
A.(CH3)3CCH(CH3)(CH2)2CH(C2H5)2 A的名称是________;
B.(CH3)3CC≡CCH2CH3 B的名称是____;
C.![]() C的名称是_____
C的名称是_____
D.CH2OHCH(C2H5) CH2OH D的名称是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质中互为同分异构体的有____,互为同素异形体的 有________,互为同位素的有________,是同一种物质的有________(填序号)。
(1)液氯 (2)氯气(3)白磷(4)红磷 (5)35Cl (6)37Cl
(7)![]() (8)
(8)![]() (9)CH2=CH-CH3 (10)
(9)CH2=CH-CH3 (10)![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氯化二硫(S2Cl2)是一种重要的化工原料,常用作橡胶硫化剂,改变生橡胶受热发粘、遇冷变硬的性质。查阅资料可知S2Cl2具有下列性质:
物理性质 | 毒性 | 色态 | 挥发性 | 熔点 | 沸点 |
剧毒 | 金黄色液体 | 易挥发 | -76℃ | 138℃ | |
化学性质 | ①300 ℃以上完全分解 ②S2Cl2+Cl2 ③遇高热或与明火接触,有引起燃烧的危险 ④受热或遇水分解放热,放出腐蚀性烟气 | ||||
(1)制取少量S2Cl2
实验室可利用硫与少量氯气在110~140℃反应制得S2Cl2粗品,氯气过量则会生成SCl2。
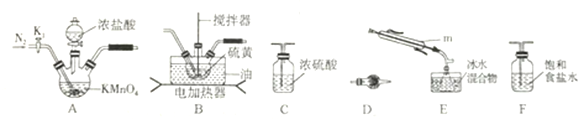
①仪器m 的名称为__________,装置F 中试剂的作用是_________。
②装置连接顺序: A![]() ______
______![]()
![]()
![]() E
E![]() D。
D。
③实验前打开K1,通入一段时间的氮气排尽装置内空气。实验结束停止加热后,再通入一段时间的氮气,其目的是_____________。
④为了提高S2Cl2的纯度,实验的关键是控制好温度和____________。
(2)少量S2Cl2泄漏时应喷水雾减慢其挥发(或扩散),并产生酸性悬浊液,但不要对泄漏物或泄漏点直接喷水,其原因是______________。
(3)S2Cl2遇水会生成SO2、HCl两种气体,某同学设计了如下实验方案来测定该混合气体中SO2的体积分数。
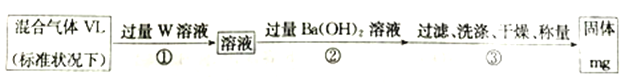
①W溶液可以是_____(填标号)。
a.H2O2溶液 b.KMnO4溶液(硫酸酸化) c.氯水
②该混合气体中二氧化硫的体积分数为_________(用含V、m 的式子表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝、铁、硅的单质及化合物在工业生产中具有广泛应用,工业上常用某矿石(主要成分有Al2O3、Fe2O3、FeO、SiO2等)来制备绿矾(FeSO4·7H2O)和氧化铝,其工艺流程如图:
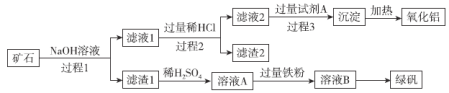
回答下列问题:
(1)滤渣1的成分是___,举例说明滤渣2的用途___。
(2)用离子方程式表示溶液A加入过量铁粉的目的是___。
(3)写出由滤液1生成滤液2的离子方程式___。
(4)过程1、2、3均涉及分离操作,所需玻璃仪器有___。
(5)由溶液B得到绿矾的具体操作为___、过滤、洗涤和干燥。
(6)过程3需要加入的试剂A是___,写出此过程的离子方程式___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于元素周期表、元素周期律及其相关应用叙述正确的是( )
A.原子的种类和元素的种类一样多
B.在现行元素周期表中,所含元素种数最多的是ⅢB族
C.可以在元素周期表金属与非金属分界处寻找催化剂
D.IA族的元素全部是金属元素
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com