
在某澄清、透明的浅黄色溶液中,可能含有下列八种离子:H+、NH4+、Fe3+、Ba2+、Al3+、SO42-、CO32-、I-,在检验方案设计时初步分析其溶液中最多可含离子(不包括OH-)有 ( )
| A.4种 | B.5种 | C.6种 | D.7种 |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:单选题
下列离子方程式正确的是 ( )
| A.NH4HCO3溶液与过量NaOH溶液反应:NH 4++ OH―=NH3↑+ H2O |
B.用惰性电极电解饱和氯化钠溶液:2Cl― + 2H +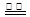 H2↑+ Cl2↑ H2↑+ Cl2↑ |
| C.向Fe(NO3)3溶液中加入过量的HI溶液:2Fe3++2I―= 2Fe2++I2 |
| D.Na2SO3溶液使酸性KMnO4溶液褪色:5SO32― + 6H+ + 2MnO4―=5SO42― + 2Mn2+ +3H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列离子在碱性溶液中能大量共存,并且溶液为无色透明的是
A.Al3+,K+,CO2-3,SO2-3 B.Na+,Ba2+,Cl-,NO-3
B.Na+,Cl-,Ca2+,MnO-4 D.K+,H+,SO2-4,Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
已知NH4+ + OH-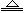 NH3↑ + H2O,NH3能使湿润的红色石蕊试纸变蓝。现某溶液中可能含有下列6种离子中的某几种:Na+、NH4+、K+、Cl-、SO42-、CO32-。为确认溶液组成进行如下实验:(1)取200 mL上述溶液,加入足量BaCl2溶液,反应后将沉淀过滤、洗涤、干燥,得沉淀4.30g,向沉淀中加入过量的盐酸,有2.33g沉淀不溶。(2)向(1)的滤液中加入足量的NaOH溶液,加热,产生能使湿润红色石蕊试纸变蓝的气体1.12L(已换算成标准状况,假定产生的气体全部逸出)。由此可以得出关于原溶液组成的正确结论是
NH3↑ + H2O,NH3能使湿润的红色石蕊试纸变蓝。现某溶液中可能含有下列6种离子中的某几种:Na+、NH4+、K+、Cl-、SO42-、CO32-。为确认溶液组成进行如下实验:(1)取200 mL上述溶液,加入足量BaCl2溶液,反应后将沉淀过滤、洗涤、干燥,得沉淀4.30g,向沉淀中加入过量的盐酸,有2.33g沉淀不溶。(2)向(1)的滤液中加入足量的NaOH溶液,加热,产生能使湿润红色石蕊试纸变蓝的气体1.12L(已换算成标准状况,假定产生的气体全部逸出)。由此可以得出关于原溶液组成的正确结论是
| A.一定存在SO42-、CO32-、NH4+,可能存在Na+、K+、Cl- |
| B.一定存在SO42-、CO32-、NH4+、Cl-,一定不存在Na+、K+ |
| C.c(CO32-)="0.01" mol/L,c(NH4+)>c(SO42-) |
| D.如果上述6种离子都存在,则c(Cl-)>c(SO42-) |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列离子方程式,正确的是
| A.氢氧化铁与盐酸反应:H++OH-=H2O |
| B.过量NaHSO4溶液与少量Ba(OH)2溶液反应:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O |
| C.铁与H2SO4反应:Fe+2H+=Fe3++H2↑ |
| D.CaCO3溶于稀盐酸中:CO32-+2H+=CO2↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列反应的离子方程式正确的是
| A.澄清石灰水跟盐酸反应:OH-+H+=H2O |
| B.金属钠跟水反应:Na+2H2O=Na++2OH-+H2↑ |
| C.碳酸钡与醋酸反应:BaCO3+2H+=CO2↑+Ba2++H2O |
| D.碳酸氢钠溶液和氢氧化钠溶液反应:HCO3-+OH-=CO2↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列电离方程式中,正确的是
| A.Na2CO3=Na++CO32- | B.Ba(OH)2=Ba2++OH2- |
| C.H2SO4=H2++SO42- | D.NaCl=Na++Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
某由离子化合物组成的混合物只可能含有以下离子中的若干种:K+、NH4+、Mg2+、Ba2+、Cl-、CO32-、SO42-。为确定其组成,准确称取14.82g混合物溶于水得300 mL澄清溶液,分成三等份分别进行如下实验:
(1)第一份加入AgNO3溶液有沉淀产生
(2)第二份加足量NaOH溶液并加热,经碱石灰干燥后收集到标况下气体1.12L
(3)第三份加足量BaCl2溶液,沉淀经洗涤、干燥后称重为6.27g,再向沉淀中加足量盐酸,经过滤、洗涤、干燥后称重为2.33 g
根据上述实验,以下推测不正确的是
| A.溶液中c(SO42-)为0.1mol/L、c(CO32-) 为0.2mol/L |
| B.该混合物中不含Ba2+、Mg2+ |
| C.一定存在NH4+、 K+,无法确定Cl-是否存在 |
| D.实验(3)沉淀中加盐酸后,若只过滤、不洗涤,会对除NH4+外的其他离子含量的测定造成影响 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com