
| ② | | | |
| | | ⑦ | ⑧ |


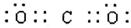 (1分)
(1分)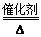 4NO+6H2O(2分)
4NO+6H2O(2分) 2Fe+Al2O3(2分)
2Fe+Al2O3(2分)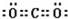 ;CCl4中碳原子与离子之间形成1对共用电子对,为共价键;非金属性C<S<Cl,最高价氧化物对应水化物的酸性强弱的顺序是HClO4>H2SO4>H2CO3;S2-、Cl-电子层结构相同,核电荷数越大离子半径越小,故离子半径S2->Cl-,答案为:第三周期第ⅥA族;;共价键;HClO4>H2SO4>H2CO3;S2->Cl-;
;CCl4中碳原子与离子之间形成1对共用电子对,为共价键;非金属性C<S<Cl,最高价氧化物对应水化物的酸性强弱的顺序是HClO4>H2SO4>H2CO3;S2-、Cl-电子层结构相同,核电荷数越大离子半径越小,故离子半径S2->Cl-,答案为:第三周期第ⅥA族;;共价键;HClO4>H2SO4>H2CO3;S2->Cl-;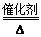 4NO+6H2O,故答案为:4NH3+5O2
4NO+6H2O,故答案为:4NH3+5O2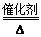 4NO+6H2O;
4NO+6H2O; 2Fe+Al2O3,故答案为:Fe2O3+2Al
2Fe+Al2O3,故答案为:Fe2O3+2Al 2Fe+Al2O3.
2Fe+Al2O3.

 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:不详 题型:单选题
| 2 | 3 | 4 | | | 2 | | | 3 | | | | 2 | | | ||||||||
| | 11 | | | 9 | 10 | | 10 | 11 | 12 | | | 10 | 11 | | ||||||||
| | 19 | 20 | | 17 | 18 | | | 19 | | | 17 | 18 | 19 | | ||||||||
| | A | | | | B | | | | C | | | | D | | ||||||||
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
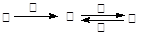 。下列有关物质的推断不正确的是( )
。下列有关物质的推断不正确的是( )| A.若甲为焦炭,则丁可能是O2 | B.若甲为SO2,则丁可能是氨水 |
| C.若甲为Fe,则丁可能是氯气 | D.若甲为NaOH 溶液,则丁可能是AlCl3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
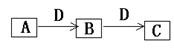
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
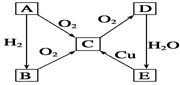
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 族 周期 | | | | |||||
| 1 | ① | | | | | | | |
| 2 | | | | | | ② | | |
| 3 | ③ | | | ④ | | ⑤ | ⑥ | |

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.X与Y形成化合物时,X显负价,Y显正价 |
| B.第一电离能可能Y小于X |
| C.最高价含氧酸的酸性:X对应酸的酸性弱于Y对应酸的酸性 |
| D.气态氢化物的稳定性:HmY小于HmX |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
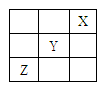
| A.Z的最高价氧化物的水化物是强酸 |
| B.Y的最高价氧化物的水化物是一种强酸 |
| C.Z离子半径比Y原子半径小 |
| D.Z的气态氢化物比Y的气态氢化物稳定 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com