

【题目】下列离子方程式中,正确的是
A.铜跟硝酸银溶液反应:Cu+Ag+= Cu2++Ag
B.小苏打溶液与稀硫酸混合:CO![]() +2H+= CO2↑+H2O
+2H+= CO2↑+H2O
C.大理石溶解于醋酸:CaCO3+2H+= Ca2++CO2↑+H2O
D.CuSO4溶液与Ba(OH)2溶液混合:Cu2++SO![]() +Ba2++2OH-=BaSO4↓+Cu(OH)2↓
+Ba2++2OH-=BaSO4↓+Cu(OH)2↓
 全能测控期末小状元系列答案
全能测控期末小状元系列答案科目:高中化学 来源: 题型:
【题目】亚硝酸钠(NaNO2)外观酷似食盐且有咸味,是一种常用的发色剂和防腐剂,使用过量会使人中毒。某兴趣小组进行下面实验探究,查阅资料知道:
①HNO2为弱酸,
②2NO+Na2O2=2NaNO2,
③2NO2+Na2O2=2NaNO3
④酸性KMnO4溶液可将NO和NO2-均氧化为NO3-,MnO4-还原成Mn2+。
NaNO2的制备方法可有如下2种方法(夹持装置和加热装置已略,气密性已检验):
制备装置1:
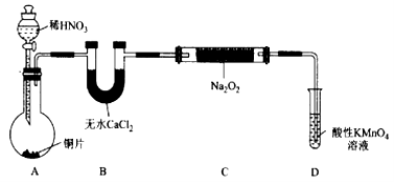
制备装置2:
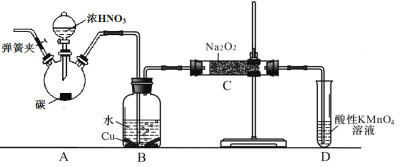
(1)在制备装置1中:
① 如果没有B装置,C中发生的副反应有 ;
② 甲同学检查完装置气密性良好后进行实验,发现制得的NaNO2中混有较多的NaNO3杂质;于是在A装置与B装置间增加了 装置,改进后提高了NaNO2的纯度;
③ D装置发生反应的离子方程式为 。
(2)在制备装置2中:
① B装置的作用是 ;
② 写出装置A烧瓶中发生反应的化学方程式并用单线桥标出电子的转移 ;
③ 为避免B中逸出的气体中混有的杂质气体与Na2O2反应,应在B、C装置间增加一个装置,则该装置中盛放的药品名称为 ;
④ 实验经改进后可制得较纯亚硝酸钠,下列关于亚硝酸钠的说法正确的是________。
a.亚硝酸钠有咸味,可代替食盐食用
b.常温下,0.1mol/L亚硝酸钠溶液pH>1
c.0.1mol/L亚硝酸钠溶液中存在:c(Na+)+c(H+)=c(NO2-)+c(OH-)
d.0.1mol/L亚硝酸钠溶液中存在:c(NO2-)>c(Na+)>c(OH-)>c(H+)
⑤ 试设计实验检验装置C中NaNO2的存在(写出操作、现象和结论) 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一小块钠投入盛20 mL饱和澄清石灰水的烧杯里,不可能观察到的现象应是
A. 钠熔成小球、四处游动 B. 钠浮在液面上
C. 溶液底部有银白色物质生成 D. 溶液变浑浊
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】相同物质的量的SO2和SO3相比较,下列叙述正确的是
①分子数之比为1:1 ②所含O原子数之比为2:3③原子总数之比为3:4 ④S原子数之比为1:1 ⑤质子数之比4:5
A. ①②③④⑤ B. ②③ C. ①⑤ D. ③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质发生反应后,固体质量一定减少的是
A. Na2O2敞放在空气中 B. 硫酸亚铁敞放在空气中
C. 铜片放入冷的浓硫酸中 D. 赤热的炭粒放入浓硝酸中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作中错误的是( )
A. 分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出
B. 蒸馏时,应使温度计水银球靠近蒸馏烧瓶支管口
C. 蒸发结晶时应将溶液蒸干
D. 称量时,称量物放在称量纸上置于托盘天平的左盘,砝码放在托盘天平的右盘中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组以木炭和浓硝酸为起始原料,探究一氧化氮与过氧化钠反应制备亚硝酸钠。设计装置如下(忽略装置中空气的影响),请回答下列问题:
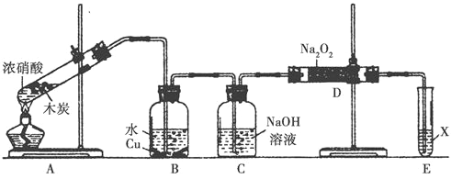
(1)组装好仪器后,必须进行的一项操作是_________________。
(2)装置A的试管中发生反应的化学方程式是_______________。
(3)推测B中可以观察到的主要现象是________;C装置的作用是________。
(4)装置D中除生成NaNO2外,还有另一种固态物质Y,Y的化学式是____________;为了不产生Y物质,可把C装置改为___________(填试剂和仪器名称)。
(5)在酸性溶液中,NO2-可将MnO4-还原为Mn2+。写出有关反应的离子方程式_______________。
(6)E装置中试剂X可以是________。
A.稀硫酸 B.酸性高锰酸钾溶液 C.稀硝酸 D.水
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com