
| A.因浓硫酸具有强氧化性,故不可用它来干燥氢气 |
| B.浓硫酸与浓氨水靠近时产生大量白烟 |
| C.浓硫酸有强氧化性,稀硫酸不具有氧化性 |
| D.浓硫酸具有腐蚀性,取用时要小心 |
科目:高中化学 来源:不详 题型:填空题
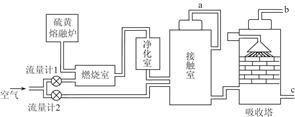
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.Fe在Cl2中的燃烧产物: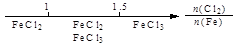 |
B.氨水与SO2反应后溶液中的铵盐: |
C.平衡常数与转化率关系: |
D.Cl2与CH4取代反应后的产物: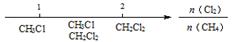 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 化合价 | -2 | -1 | 0 | +2 | +4 | +6 | +7 |
| 代表物的化学式 | | FeS2 | S | Na2S2O3 | | SO3或H2SO4或Na2SO4 | Na2S2O8 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 编号 | 实验操作 | 预期现象和结论 |
| 步骤① | 取少量待测液于试管A中,滴加2 mol·L-1HCl至溶液呈酸性,加入几滴________(填试剂),振荡 | ________,证明待测液中含SO32- |
| 步骤② | 另取少量待测液于试管B中,加入 ,再滴加适量 1 mol·L-1 BaCl2溶液 | |
| 步骤③ | 另取少量待测液于试管C中, ,振荡,静置后观察颜色 | 溶液分层,上层液体呈橙红色,证明待测液中很Br- |
查看答案和解析>>
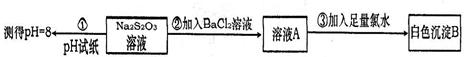
科目:高中化学 来源:不详 题型:单选题
| A.白色沉淀都是BaSO3 |
| B.①白色沉淀是BaSO3和S,②是BaSO3 |
| C.①白色沉淀是BaSO4,②是BaSO3 |
| D.①白色沉淀是FeSO3,②是BaSO3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
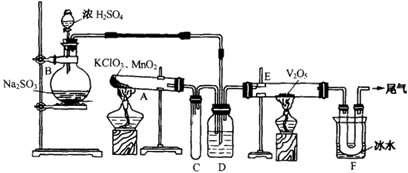
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
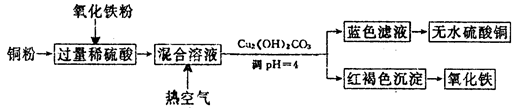
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
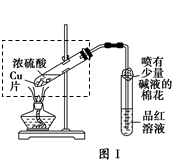
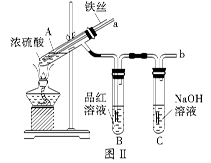
| 步骤 | 所选试剂 | 现象及结论 |
| 1 | | |
| 2 | | |
| 3 | | |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com