
【题目】在一支25mL的酸式滴定管中盛入0.1mol/L HCl溶液,其液面恰好在5mL的刻度处,若把滴定管中的溶液全部放入烧杯中,然后以0.1mol/L NaOH溶液进行滴定,则所需NaOH溶液的体积( )
A.大于20mL
B.小于20mL
C.等于20mL
D.等于5mL
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】物质爆炸都伴随着能量变化,请回答下列问题:
(1)氯酸钾、火药及磷等组成的混合物极易爆炸。由于KClO3受热分解释放出O2,引发白磷(P4,固体)的燃烧而导致火药爆炸。31 g P4完全燃烧生成五氧化二磷固体释放出a kJ热量。下列说法不正确的是________ (填字母)。
A.KClO3的分解过程中只有共价键断裂没有共价键生成
B.火药爆炸会使周围空气体积迅速膨胀
C.若白磷完全燃烧释放出8a kJ热量,则需要标准状况下的O2体积为224 L
D.易燃易爆物应远离火源
(2)天然气已经成为我国主要的民用清洁能源,但天然气与空气混合达到一定比例后遇明火会发生爆炸,所以安全使用天然气,防止发生爆炸是极为重要的。已知天然气的主要成分甲烷燃烧时的能量变化如图所示。
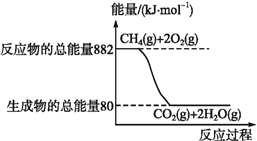
请回答下列问题:
①下列说法正确的是____(填字母)。
A.天然气属于清洁能源,所以它属于新能源
B.甲烷完全燃烧时化学能全部转化为热能
C.标准状况下44.8 L甲烷完全燃烧时有8 mol共价键断裂
D.用天然气做饭时,为使甲烷充分燃烧,通入的空气越多越好
②CH4(g)完全燃烧时生成18 g气态水放出的热量是____kJ。
③若家庭做饭需64160 kJ热量,假设天然气(按CH4算)的热效率为80%,则需要天然气(按CH4算)的质量为____g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有A、B、C三种化合物,各取40g相混合,完全反应后,得B18g,C49g,还有D生成。已知D的式量为106。现将22gA和11gB反应,能生成D
A.1molB.0.5molC.0.25molD.0.275mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向Na2CO3、NaHCO3混合溶液中逐滴加入稀盐酸,生成气体的量随盐酸加入量的变化关系如右图所示。则下列离子组在对应的溶液中一定能大量共存的是

A.a点对应的溶液中:Na+、AlO2-、SO42-、NO3-
B.b点对应的溶液中:Ba2+、K+、NO3-、Cl-
C.c点对应的溶液中:Na+、Ag+、Mg2+、NO3-
D.d点对应的溶液中:Cl-、NO3-、Fe2+、Na+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 金属氧化物都是碱性氧化物
B. 酸性氧化物都是非金属氧化物
C. 含有氧元素的化合物均为氧化物
D. 难溶于水的氢氧化物其对应的氧化物也难溶于水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将有机物完全燃烧,生成CO2和H2O.将12g该有机物完全燃烧后的产物通过浓H2SO4 , 浓H2SO4增重14.4g,再通过碱石灰,碱石灰增重26.4g.该有机物分子式为( )
A.C4H10
B.C2H6O
C.C3H8O
D.C2H4O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知NO2和N2O4可以相互转化:2NO2(g)N2O4(g)△H<0.在恒温条件下将一定量NO2和N2O4的混合气体通入一容积为2L的密闭容器中,反应物浓度随时间变化关系如图.下列说法不正确的是( ) 
A.图中的两条曲线,X表示NO2浓度随时间的变化曲线
B.前10 min内用v(N2O4)=0.02 mol/(Lmin)
C.25 min时,NO2转变为N2O4的反应速率增大,其原 因是将密闭容器的体积缩小为1L
D.该温度下反应的平衡常数 K=1.11 L/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中,一定条件下,进行如下反应:NO(g)+CO(g) ![]() N2(g)+CO2(g)△H=﹣373.2kJ/mol,达到平衡后,为提高该反应的速率和NO的转化率,采取的正确措施是( )
N2(g)+CO2(g)△H=﹣373.2kJ/mol,达到平衡后,为提高该反应的速率和NO的转化率,采取的正确措施是( )
A.加催化剂同时升高温度
B.加催化剂同时增大压强
C.升高温度同时充入N2
D.降低温度同时增大压强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙醛酸(HOOC-CHO)是有机合成的重要中间体。某同学组装了下图所示的电化学装置,电极材料Ⅰ~Ⅳ均为石墨,左池为氢氧燃料电池,右池为用“双极室成对电解法”生产乙醛酸,关闭K后,两极室均可产生乙醛酸,其中乙二醛与Ⅲ电极的产物反应生成乙醛酸。下列说法不正确的是( )
A.电极Ⅱ上的电极反应式:O2+4e-+2H2O=4OH-
B.电极Ⅳ上的电极反应式:HOOC-COOH+2e-+2H+=HOOC-CHO+H2O
C.乙二醛与Ⅲ电极的产物反应生成乙醛酸的化学方程式: Cl2 + OHC-CHO+ H2O = 2HCl+ HOOC-CHO
D.若有2 mol H+ 通过质子交换膜并完全参与反应,则该装置中生成的乙醛酸为1 mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com