
 C��SiԪ���ڻ�ѧ��ռ�м�����Ҫ�ĵ�λ��
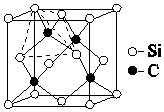
C��SiԪ���ڻ�ѧ��ռ�м�����Ҫ�ĵ�λ������ ��1��Siԭ�Ӻ��14�����ӣ������������ԭ����д�����Ų�ʽ��Ԫ�����ڱ�������Ԫ��Խ���ҡ�Խ���ϵ縺��Խ��F�ĵ縺�����Ϊ4.0����
��2��CO2����Ϊֱ���νṹ����֪̼ԭ�Ӳ�ȡsp�ӻ���ʽ��ԭ����Ŀ��ȡ��۵�������Ҳ��ȵ�����Ϊ�ȵ����壻
��3��Siԭ�ӱ�Cԭ�Ӱ뾶��Si��Oԭ�Ӽ����ϴ�
��4������ԭ�Ӿ����Ӳ�ȴ�ÿ��̼ԭ������4����ԭ�ӣ�ÿ����ԭ������������3��̼ԭ�ӣ��ݴ��ж�ÿ��Cԭ����Χ�����Cԭ����Ŀ���þ�����Cԭ�Ӹ���=8��$\frac{1}{8}$+6��$\frac{1}{2}$=4��Siԭ�Ӹ���Ϊ4�����ݦ�=$\frac{m}{V}$�������ܶȣ�
��� �⣺��1��Si��14��Ԫ�أ�Siԭ�Ӻ��14�����ӣ������������ԭ�����������������͵�1s��������������������������ϸߵĹ����������Ų�ʽΪ��1s22s22p63s23p2���ӵ縺�ԵĽǶȷ�����O��Cλ��ͬһ���ڣ��ǽ�����Oǿ��C��C��SiΪ��ͬһ���壬C�ķǽ�����ǿ��Si������ǿ����ΪO��C��Si��
�ʴ�Ϊ��1s22s22p63s23p2�� O��C��Si��
��2��CO2����Ϊֱ���νṹ����֪̼ԭ�Ӳ�ȡsp�ӻ���ʽ��ԭ����Ŀ��ȡ��۵�������Ҳ��ȵ�����Ϊ�ȵ����壬��CO2 ��Ϊ�ȵ��������������N2O��
�ʴ�Ϊ��ֱ���Σ�sp��N2O��
��3��CO2��C��Oԭ�Ӽ��γɦҼ��ͦм���SiO2��Si��Oԭ�Ӽ䲻�γ������м�������Siԭ�ӱ�Cԭ�Ӱ뾶��Si��Oԭ�Ӽ����ϴ�P-P����粢���ص��̶Ƚ�С�������γ������ȶ��Ħм����ʴ�Ϊ��Siԭ�ӱ�Cԭ�Ӱ뾶��Si��Oԭ�Ӽ����ϴ�P-P����粢���ص��̶Ƚ�С�������γ������ȶ��Ħм���
��4�����ɰ��SiC����Ӳ��Ϊ9.5������ԭ�Ӿ��壻ÿ��̼ԭ������4����ԭ�ӣ�ÿ����ԭ������������3��̼ԭ�ӣ�����ÿ��̼ԭ����Χ�����̼ԭ����ĿΪ3��4=12���þ�����Cԭ�Ӹ���=8��$\frac{1}{8}$+6��$\frac{1}{2}$=4��Siԭ�Ӹ���Ϊ4�������߳�=a��10-10cm�����V=��a��10-10cm��3����=$\frac{m}{V}$=$\frac{\frac{40��4}{N{\;}_{A}}}{��a��10{\;}^{-10}��^{3}}$g•cm3=$\frac{1.6��10{\;}^{32}}{N{\;}_{A}}$g•cm3��
�ʴ�Ϊ��ԭ�Ӿ��壻12��$\frac{1.6��10{\;}^{32}}{N{\;}_{A}}$��
���� ���⿼��λ�ýṹ���ʵ����ϵӦ�ã�Ϊ��Ƶ����ͳ������ͣ�������ѧ���ķ��������Ŀ��飬�漰�������㡢ԭ���ӻ��жϡ�ԭ�Ӻ�������Ų�ʽ����д��֪ʶ�㣬�ѵ��Ǿ������㣬��Ŀ�Ѷ��еȣ���ȷ�ƶ�Ԫ�ص�����Ϊ������Ĺؼ���ע��ԭ�ӽṹ��Ԫ�����ڱ��Ĺ�ϵ��


 ��ս�п�����ϵ�д�
��ս�п�����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
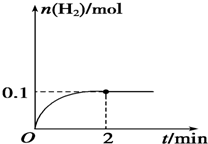 ��-��ѭ���ֽ�ˮ������Ҫ�漰���з�Ӧ��
��-��ѭ���ֽ�ˮ������Ҫ�漰���з�Ӧ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��������������������������зֱ���ȫȼ�գ��ų�����һ���� | |
| B�� | ��Ҫ���Ȳ��ܷ����ķ�Ӧһ�������ȷ�Ӧ | |
| C�� | ��101kpaʱ��2gH2��ȫȼ�գ�����Һ̬ˮ���ų�285.8kJ������������ȼ�յ��Ȼ�ѧ����ʽ��ʾΪ��2H2��g��+O2��g���T2H2O��l����H=-285.8kJ/mol | |
| D�� | ��ǿ��ǿ��ϡ��Һ�У�H+��aq��+OH-��aq��=H2O��l����H=-57.3kJ/mol��������1molNaOH����Һ�ͺ�0.5molH2SO4��Ũ�����ϣ��ų�����������57.3 kJ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
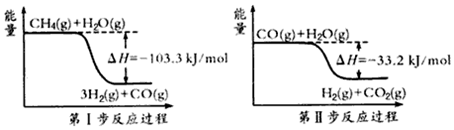
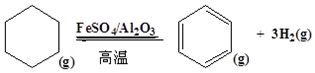
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| Fe2+ | Fe3+ | Cu2+ | |
| ��ʼ����ʱpH | |||
| ��ȫ����ʱpH | 8 | 3.2 | 6.7 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 200mL2mol/LMgCl2��Һ | B�� | 1000mL2.5mol/LNaCl��Һ | ||
| C�� | 300mL5mol/LFeCl3��Һ | D�� | 250mL lmol/L AlCl3��Һ |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com