
 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案科目:高中化学 来源:不详 题型:单选题
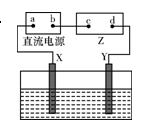
| A.接通电路后,水槽中溶液的pH不变 |
| B.b是正极,Y电极上发生氧化反应 |
| C.同温同压下,X、Y两电极上产生气体的体积相等 |
| D.d点显红色是因为接通电路后OH-向d点移动 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
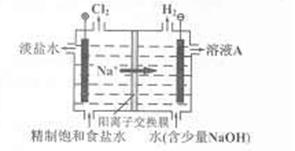
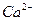 、
、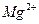 ,NH+3,
,NH+3,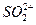 ,[
,[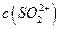 >
>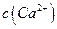 ]。
]。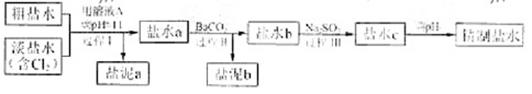
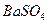 的溶解度比
的溶解度比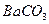 的小,过程Ⅱ中除去的离子有
的小,过程Ⅱ中除去的离子有 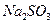 的含量小于5mg /l ,若盐水b中
的含量小于5mg /l ,若盐水b中 的含量是7.45 mg /l ,则处理10m3盐水b ,至多添加10%
的含量是7.45 mg /l ,则处理10m3盐水b ,至多添加10% 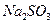 溶液 kg(溶液体积变化忽略不计)。
溶液 kg(溶液体积变化忽略不计)。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.稀NaOH溶液 | B.HCI溶液 | C.NaCl溶液 | D.酸性AgNO3溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.电解法制铝时一般是用熔融态的氧化铝进行电解,但也可用熔融态的A1C13 |
| B.电解法生产铝时,每转移3mol电子的时候,就能生产出1mol的铝。 |
| C.在电解饱和NaCl溶液中,电解池中的阴极产生的是H2,NaOH在阳极附近产生 |
| D.电解饱和NaCl溶液和金属钠的冶炼都用到了NaC1,在电解时它们的阴极都是C1-失电子 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 离子 | Cu2+ | Al3+ | NO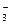 | Cl- |
| 物质的量浓度(mol/L) | 1 | 1 | 4 | a |
| A.电解后溶液的pH=" 0" | B.阳极与阴极析出的气体物质的量之比为1:2 |
| C.阳极电极反应:2Cl——2e—=Cl2 | D.阴极析出32g铜 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com