
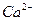 、
、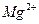 ,NH+3,
,NH+3,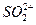 ,[
,[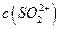 >
>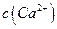 ]。
]。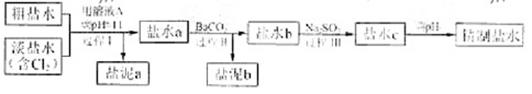
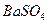 的溶解度比
的溶解度比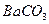 的小,过程Ⅱ中除去的离子有
的小,过程Ⅱ中除去的离子有 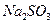 的含量小于5mg /l ,若盐水b中
的含量小于5mg /l ,若盐水b中 的含量是7.45 mg /l ,则处理10m3盐水b ,至多添加10%
的含量是7.45 mg /l ,则处理10m3盐水b ,至多添加10% 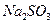 溶液 kg(溶液体积变化忽略不计)。
溶液 kg(溶液体积变化忽略不计)。科目:高中化学 来源:不详 题型:单选题
| A.电解液质量增加mg | B.阴极质量增加xg,x>m |
| C.阴极质量增加mg | D.阴极质量增加yg,y<m |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.c(Na+)>c(CH3COO-) | B.c(Na+)+c(H+)=c(OH-)+c(CH3COO-) |
| C.c(Na+)<c(CH3COO-) | D.c(Na+)<c(CH3COO-)+ c(OH-) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
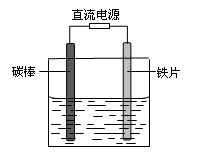
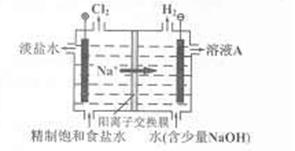
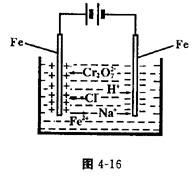
| A.碳棒接直流电源的负极 |
| B.碳棒上发生氧化反应 |
| C.铁片上的电极反应式为2Cl――2e-= Cl2↑ |
| D.铁片附近出现的浑浊物是Mg(OH)2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.71:2 | B.71:216 | C.8:1 | D.16:137 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 ( )
( )| A.1:2:3 | B.3:2:l | C.6:3:1 | D.6:3:2 |
| 物质 | K2O | MgO | Al2O3 | KCl | MgCl2 | AlCl3 |
| 熔点(℃) | 881 | 2852 | 2015 | 711 | 714 | 190(259KPa) |
| 沸点(℃) | -- | 3600 | 2980 | 1437 | 1412 | 181 |
 合材料二可推知氯化钾、氯化镁、氯化铝三种物质中有一种物质是不符合题意的,这种物质是 ,其理由是
合材料二可推知氯化钾、氯化镁、氯化铝三种物质中有一种物质是不符合题意的,这种物质是 ,其理由是 查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
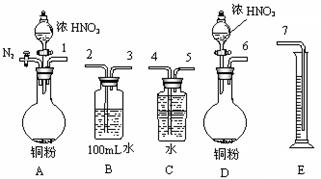
 设计了一个实验装置,也能使铜很快溶于稀盐酸.请在下面的方框中画出该装置:
设计了一个实验装置,也能使铜很快溶于稀盐酸.请在下面的方框中画出该装置:
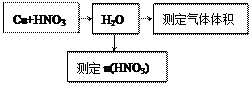 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com