
把7.4 g Na2CO3·10H2O 和 NaHCO3组成的混合物溶于水配成100mL溶液,其中c(Na+)=0.6mol/L。若把等质量的混合物加热至恒重,残留物的质量是
A.3.18g B.2.12g C.4.22g D.5.28g
 课时训练江苏人民出版社系列答案
课时训练江苏人民出版社系列答案科目:高中化学 来源: 题型:
研究和开发CO2和CO的创新利用是环境保护和资源利用双赢的课题。

(1)CO可用于合成甲醇。在体积可变的密闭容器
中充入4molCO和8molH2,在催化剂作用下合成甲醇:
CO(g)+2H2(g) CH3OH(g)(Ⅰ),平衡时CO
CH3OH(g)(Ⅰ),平衡时CO
的转化率与温度、压强的关系如右图所示:
①该反应的逆反应属于________反应;(填“吸热”或
“放热”)。
②在0.1Mpa 、100℃的条件下,该反应达到平衡时容
器体积为开始容器体积的_________倍。(结果保留两位小数点)
③在温度和容积不变的情况下,再向平衡体系中充入4molCO,8molH2,达到平衡时CO转化率_______(填“增大”,“不变”或“减小”), 平衡常数K_______(填“增大”,“不变”或“减小”)。
(2)在反应(Ⅰ)中需要用到H2做反应物,以甲烷为原料制取氢气是工业上常用的制氢方法。已知:
CH4(g)+ H2O(g)= CO(g)+3H2(g) △H=+206.2 kJ·mol-1
CH4(g)+ CO2(g)= 2CO(g)+2H2(g) △H=+247.4 kJ·mol-1
则CH4和H2O(g)反应生成CO2和H2的热化学方程式为: 。
(3)在反应(Ⅰ)中制得的CH3OH 即可以做燃料,还可以与氧气组成碱性燃料电池,电解质溶液是20%~30%的KOH溶液。则该燃料电池放电时:负极的电极反应式为_______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子在溶液中能大量共存的是
A.Fe3+、NH4+、SCN-、Cl- B.Ba2+、H+、NO3-、SO42-
C.Fe2+、Fe3+、Na+、NO3- D.Fe2+、NH4+、Cl-、OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
等体积、等物质的量浓度的盐酸、氢氧化钠溶液分别放在甲、乙两烧杯中,各加等质量的铝,生成氢气的体积比为5∶7,则甲、乙两烧杯中的反应情况可能分别是
A.甲、乙中都是铝过量
B.甲中铝过量,乙中碱过量
C.甲中酸过量,乙中铝过量
D.甲中酸过量,乙中碱过量
查看答案和解析>>
科目:高中化学 来源: 题型:
如图实验装置用于验证某些物质的性质.在试管A中装入足量的固体NaHCO3.试回答下列问题:

(1)在A试管内发生反应的化学方程式是_______________________________________________;
(2) B装置的作用是__________________________________________________;
(3)在双球干燥管内发生反应的化学方程式为___________________________________________;
(4)双球干燥管内观察到的实验现象是___ _____, 上述实验现象说明_________________ _;
(5)若将干燥管内的Na2O2换成Na2O,则双球干燥管内观察到的实验现象是______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下表是二种银盐的溶度积常数KSP(25℃).下列说法不正确的是

A.25℃时.二种银盐的饱和溶液中,c(Ag+)最大的是AgCl溶液
B.在AgCl的悬浊液中加入0.1mol·L—1的KI溶液,可能有黄色沉淀产生
C.25℃时.AgC1固体在等物质的量浓度的NaC1CaC1溶液中的溶度积相同
D.在AgBr的悬浊液中加入0.1mol·L-1的KI溶液.发生反应的离子方程式为

查看答案和解析>>
科目:高中化学 来源: 题型:
某研究所对含硫酸亚铁和硫酸铜的工业废料进行相关的研究。实验过程如下:
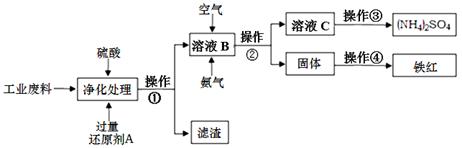
回答下列问题:
(1)滤渣的成分为 ,操作①的名称为 。
(2)上图溶液B中所发生反应的离子方程式为 。
(3)实验要求向溶液B中通入过量的空气,证明通入空气过量的方法是 。
(4)操作③第一步需要的仪器除了酒精灯、铁架台外,还需要 、 。
(5)某同学利用下面装置制备氢气并利用氢气还原某金属氧化物,根据要求回答问题。
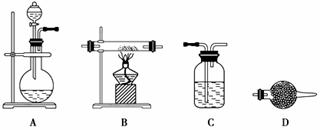
①请设计一个实验方案验证H2的还原性并检验其氧化产物,其装置连接顺序是A→_____→_____→_____→D(除D装置外,其它装置不能重复使用),最后D装置中所加药品为____________,其作用是___________________。
②点燃B处酒精灯之前必须进行的操作是____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
可逆反应A(g)+3B(g)  2C(g);△H= -QkJ/mol。有甲、乙两个容积相同且固定不变的密闭容器,向甲容器中加入1molA和3molB,在一定条件下达到平衡时放出热量为Q1kJ;在相同的条件下,向乙容器中加入2molC达到平衡后吸收热量为Q2kJ,已知Q1=2Q2。下列叙述正确的是
2C(g);△H= -QkJ/mol。有甲、乙两个容积相同且固定不变的密闭容器,向甲容器中加入1molA和3molB,在一定条件下达到平衡时放出热量为Q1kJ;在相同的条件下,向乙容器中加入2molC达到平衡后吸收热量为Q2kJ,已知Q1=2Q2。下列叙述正确的是
A.甲中A的转化率为75%
B.Q1 + Q2 < Q
C.达到平衡后,再向乙中加入1/3 molA、1 molB、4/3 molC,平衡向正反应方向移动
D.乙中热化学方程式为2C(g) A(g)+3B(g);△H= + Q2 kJ/mol
A(g)+3B(g);△H= + Q2 kJ/mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com