
【题目】将少量金属钠放入盛有CuSO4溶液的烧杯中,烧杯中发生的反应是
①2Na+CuSO4=Na2SO4+Cu
②Cu+2H2O=Cu(OH)2↓+H2↑
③2Na+2H2O=2NaOH+H2↑
④2NaOH+CuSO4=Cu(OH)2↓+Na2SO4
A.① B.①② C.③④ D.①③
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】下列关于化学反应与能量的说法正确的是( )
A. CO燃烧属于放热反应 B. H2SO4与NaOH反应属于吸热反应
C. 化学键断裂放出能量 D. 反应物总能量与生成物总能量一定相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A,B,C,D四种元素都是短周期元素.A元素的离子具有黄色的焰色反应.B元素的离子结构和Ne具有相同的电子层排布;5.8g B的氢氧化物恰好能与100mL 2mol/L盐酸完全反应;B原子核中质子数和中子数相等.H2在C单质中燃烧产生苍白色火焰.D元素原子的电子层结构里,最外层电子数是次外层电子数的3倍.根据上述条件,回答:
(1)元素C的最高价氧化物的化学式为 .
(2)写出元素名称A , B .
(3)A与D形成稳定的化合物的化学式为 .
(4)C元素的单质有毒,可用A的最高价氧化物对应的水化物的溶液吸收,其离子方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列变化过程中,属于放热反应的是( )
①液态水变成水蒸气 ②酸碱中和反应 ③浓H2SO4稀释 ④固体NaOH溶于水 ⑤H2在Cl2中燃烧 ⑥食物腐败 ⑦Ba(OH)2·8H2O与NH4Cl的反应
A.②⑤⑥B.②③④⑤C.①③⑤⑦D.②③④⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁的化合物在工业上有重要的应用.
(1)FeCl3净水的原理是(用离子方程式表示)_________________.FeCl3溶液腐蚀钢铁设备,除H+作用外,另一主要原因是(用离子方程式表示)________________.
(2)为节约成本,工业上用NaClO3 氧化酸性FeCl2废液得到FeCl3.
①若酸性FeCl2废液中c(Fe2+)=2.0×10﹣2molL﹣1,c(Fe3+)=1.0×10﹣3molL﹣1,c(Cl﹣)=5.3×10﹣2molL﹣1,则该溶液的PH约为_____.
②完成NaClO3 氧化FeCl2 的离子方程式:
ClO3﹣ +___Fe2+ +___ ____= __Cl﹣ + ___Fe3++ __ ____.
(3)高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂,且不会造成二次污染.已知高铁酸盐热稳定性差,工业上用湿法制备K2FeO4的流程如图1所示:反应③加入浓KOH溶液可析出高铁酸钾(K2FeO4),这说明__________________________.某温度下,将Cl2通入NaOH溶液中,反应后得到NaCl、NaClO、NaClO3的混合溶液,经测定ClO﹣与ClO3﹣离子的物质的量之比是1:2,则Cl2与氢氧化钠反应时,被还原的氯元素和被氧化的氯元素的物质的量之比为_____.
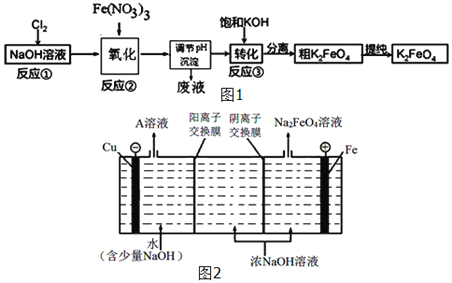
(4)工业上还可用通过电解浓NaOH溶液来制备Na2FeO4,其工作原理如图2所示:阳极的电极反应式为__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上铁冶炼是在中进行的.在冶炼过程中铁元素被还原,还原剂是 , 产生还原剂的化学方程式是、 . 用这种方法冶炼的铁是含碳2%~4.5%的 , 将它进一步冶炼,就可以得到用途广泛 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2013年1月3日晨,昆明长水国际机场出现大雾天气,导致大量航班延误。雾属于下列哪种分散系( )
A. 乳浊液 B. 溶液 C. 悬浊液 D. 胶体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在硫酸铁溶液中,加入a g铜完全溶解后再加入b g铁,充分反应后得到c g残余固体,且a>c,则下列说法中正确的是( )
A. 残余固体可能为铁和铜的混合物 B. 最后得到的溶液可能含有Fe3+
C. 最后得到的溶液中一定含有Fe2+,可能含有Cu2+ D. 残余固体一定全部是铜
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com