
| A、化学键是使离子或原子相结合的作用力 | B、气态单质的分子中不一定存在化学键 | C、Na20与Na202固体中的阳离子和阴离子数目之比都是2:1 | D、碳原子最外层有4个电子,能与其他原子形成4个离子键 |
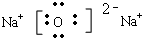 ,所以阳离子和阴离子数目之比都是2:1,Na202是由钠离子和过氧根离子构成的离子化合物,电子式为
,所以阳离子和阴离子数目之比都是2:1,Na202是由钠离子和过氧根离子构成的离子化合物,电子式为 ,阳离子和阴离子数目之比是2:1,故C正确;
,阳离子和阴离子数目之比是2:1,故C正确;

 快乐5加2金卷系列答案
快乐5加2金卷系列答案湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com